2020年,全球超过50万女性患上宫颈癌,大约34.2万名女性因宫颈癌死亡。我国正处于加速消除宫颈癌的关键时期,快速准确的筛查计划对于宫颈癌预防和早期发现,早期全球治疗年龄。
2021年7月6日,WHO发布了最新的宫颈癌前病变筛查和治疗指南,推荐HPV-DNA检测作为宫颈癌筛查的首选筛查方法。
在随后发布的《人乳头瘤病毒核酸检测用于宫颈癌筛查中国专家共识(2022)》、《中国子宫颈癌筛查指南(2023)》均推荐高危型HPV核酸作为初筛方法。
高危型HPV特指WHO确认的14种高危HPV亚型(HPV16、18、31、33、35、39、45、51、52、56、58、59、66、68)。推荐HPV16/18分型检测用于进一步风险人群的分层,检测应为定性检测。
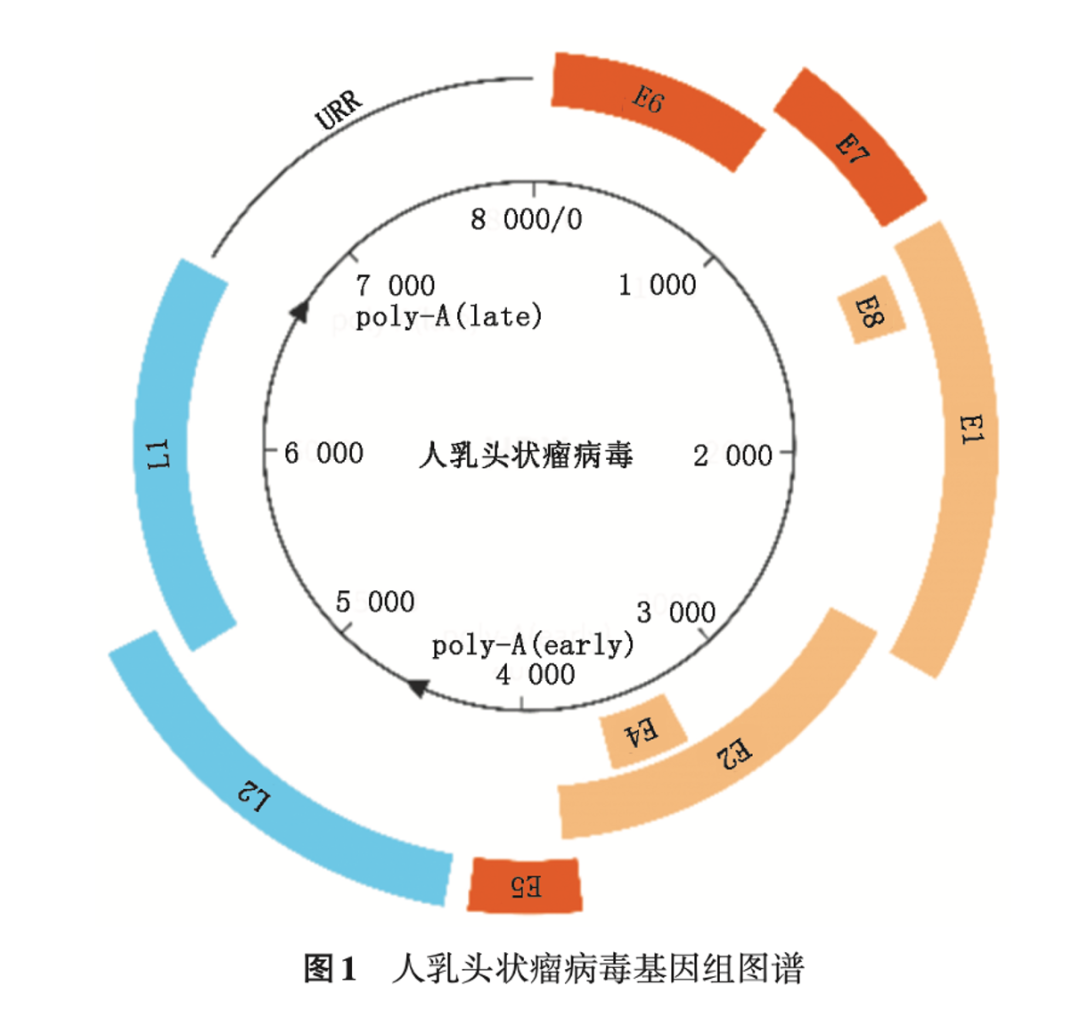
HPV核酸检测方法可以分为非扩增法和扩增法,这些方法可对HPV全基因组或某一片段(例如:以L1 DNA、E6/E7 DNA或mRNA等为检测靶点)进行有效检测。
尽管过去30年巴氏涂片筛查大幅降低了宫颈癌的发病率和死亡率,但是有一些人群可能由于个人偏好、宗教或文化信仰、创伤经历、残疾或医疗状况,无法接受常规的盆腔检查。
根据美国癌症协会今年早些发布的报告,30至40岁女性的宫颈癌发病率呈上升趋势,超过一半的确诊患者从未接受过筛查,或至少五年内没有筛查。此外,HPV疫苗接种率远低于推荐标准,表明筛查普及的障碍不仅仅在于检测本身。
传统宫颈抹片筛查的漏诊率超过40%,而新兴的HPV DNA检测逐步取代了这一方法。关于HPV检测方案的发展趋势,可以从美国FDA近20年批准的HPV检测技术和产品来做分析和预测。早在2003年,Qiagen的HC2检测产品获批,HC2检测13种高危型HPV病毒,不进行具体分型,这是因为高危型的HPV持续性感染易导至宫颈癌的必要条件。
2011年,Roche的Cobas HPV获得FDA批准,Cobas可以检测14种高危型HPV,并且对HPV 16/18型进行具体分型,众多基于HPV分型的研究结果表明:HPV16/18型的致癌风险最高,两者导至了70%的宫颈癌,因此需要对HPV16/18进行区分鉴别。
2011年,FDA批准了Holgic的HPV RNA E6E7检测产品,该产品可检测14种高危型HPV,对HPV 16及18/45单独检测,其他11种高危型不进行具体分型,该检测的设计是基于临床上出现了越来越多的HPV 45型感染导至的宫颈腺癌,HPV 45型的风险进一步被明确和证实。
2018年,FDA批准了BD公司的 Onclarity HPV检测产品,该产品可检测14种高危型HPV,对HPV16,18,45,31,51,52进行具体分型,另外8个型别采用分组显示结果。越来越多的证据表明:14种高危型HPV中,除了16和18型,其他高危型的致癌风险差异不一,需区别对待,比如HPV31和33型,其绝对风险与18型类似,未来可能直接转诊阴道镜;51/52/58等型别的风险较高,结合细胞学结果转诊阴道镜;其他较低风险的型别,可考虑一年后随访。

总体来说, 美国FDA批准的HPV产品从不分型、到部分分型(分16/18型)、再到拓展分型(分6个型),朝着精细化、精准化的方向在发展。随着检测技术的进步和临床研究数据的积累,预计未来FDA将批准HPV全分型以或HPV分型定量的相关产品。
近年来,大样本的研究成果都表明:HPV基因分型能在单一基因型水平上,从高风险到低风险进行风险分层,实现更精准的风险持续监测,能有效优化HPV阳性人群的分诊。
在今年的CSCCP大会上,美国匹兹堡医学中心的赵澄泉教授指出,中国的HPV检测技术已经全球领先,积累了丰富的研究数据。建议在制定宫颈癌筛查指南时,将HPV基因分型的指导作用纳入考量。
近年来,随着隐私性、可及性和自主性的提升,性传播疾病自我采样检测率显著上升。相较于女性在巴氏涂片检查中面临的挑战,自我采集技术更容易被接受,显著降低筛查障碍,提升未筛查女性的宫颈癌筛查率。自我采样技术通过简单的采集设备(如阴道拭子)获取宫颈阴道细胞样本用于高风险HPV检测。如果采用高灵敏度检测技术,自我采样的检测结果在灵敏度和特异性上与医生采集的结果相似。自我采样的优势在于无需初步的临床盆腔检查,样本采集可在家中等便捷场所完成,高危HPV阳性者可及时转诊进行进一步护理。
今年5月,美国FDA批准了BD Onclarity和Roche cobas两个宫颈癌筛查用HPV检测,均支持自我采样。如果患者无法或不愿接受盆腔检查,可以选择在医疗机构内进行自我采样。随着自我采样与精准的HPV检测技术的结合,宫颈癌筛查的普及率有望显著提升。
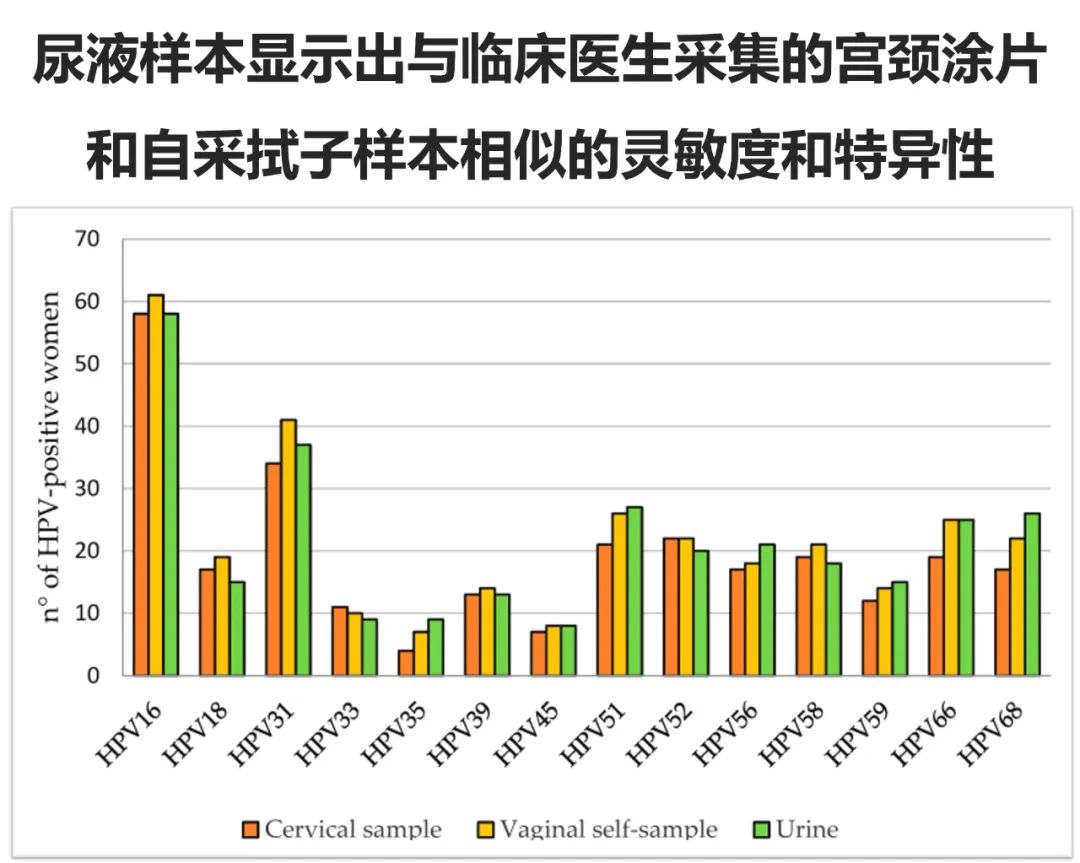
通常的自我采集依然是使用拭子提取阴道样本,但是今年研究发现尿液样本也是自我采集HPV检测的可替代选择,而且调查显示,与拭子自我采样方法相比,女性明显更倾向于以尿液作为样本类型,因为它是非侵入性的方式,并且更适合居家检测。
迈迪安推出了全新的可冻干基因分型尿液直扩qPCR预混液(MDX158),是专为从尿液样本中超灵敏地扩增SNPs和其他位点突变设计优化的即用型预混液,对样本中可能破坏DNA和抑制PCR反应的尿素和核酸酶具有超强耐受性。此外,该试剂既能用于液体体系也能通过冻干用于开发常温稳定的检测,是用于高通量HPV分型检测的理想选择。对HPV -16型的突变检测
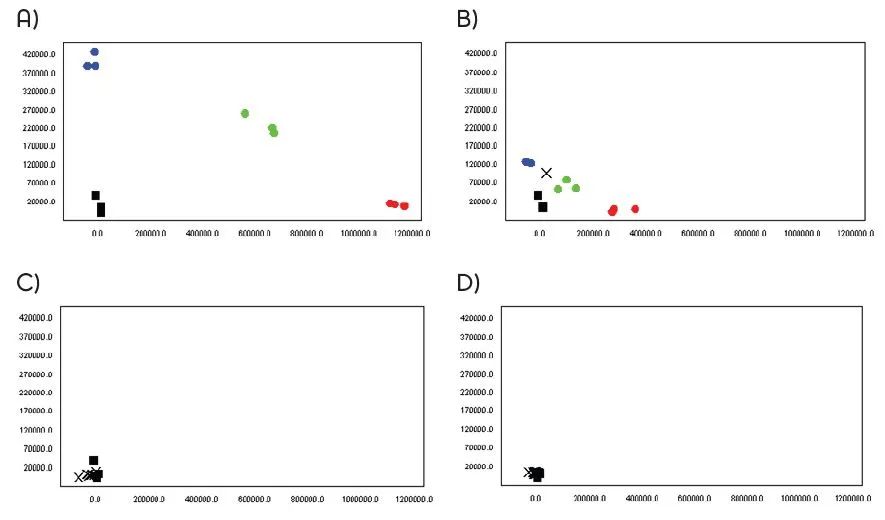
分别使用 A) Lyo-Ready™ 可冻干基因分型尿液直扩qPCR预混液 (MDX158), B/ KAPA Probe Force qPCR Mix (Roche), C) TaqPath™ ProAmp™ Multiplex Master Mix (ThermoFisher) 和 D) Type-it Fast SNP Probe PCR Kits (Qiagen) 对40% UTM样本中的人乳头瘤病毒(HPV)16型 E6-T350G突变进行检测。等位基因G(蓝色)和 等位基因T(红色)的纯合样本,等位基因G/T的杂合样本(绿色),与NTC(黑色)进行比对,图中x表示未确定。
结果显示,与对比试剂相比,Lyo-ReadyTM 可冻干基因分型尿液直扩qPCR预混液对UTM样本的直接检测具有更紧密的集群分布,对临床相关的突变位点具有更准确的分辨。
 /3
/3 