大多数癌症被发现时通常是晚期,此时治疗通常束手无策。而癌症越早被发现,治疗也会越容易。多癌检测能否实现早发现、降低死亡率?
本CA综述作者在很大程度上代表了美国国家癌症研究所(NCI)对多癌检测产品开发的观点。然而,在美国,FDA、CMS等联邦机构对多癌检测产品均有监管兴趣。多癌检测产品的临床应用不仅是技术革新的体现,更是风险最小化与收益最大化的缩影。
众所周知,CA杂志是史上影响因子最高的期刊,全称CA: A Cancer Journal for Clinicians(中文名《临床医师癌症杂志》,当前影响因子254.7),在2020年的影响因子高达508.702,被称为神刊CA。CA被誉为神刊,不仅因其定期发布全球癌症统计报告,拥有极高的学术影响力和引用率,还因其综述类文章发表量较少,使得每篇都显得尤为珍贵。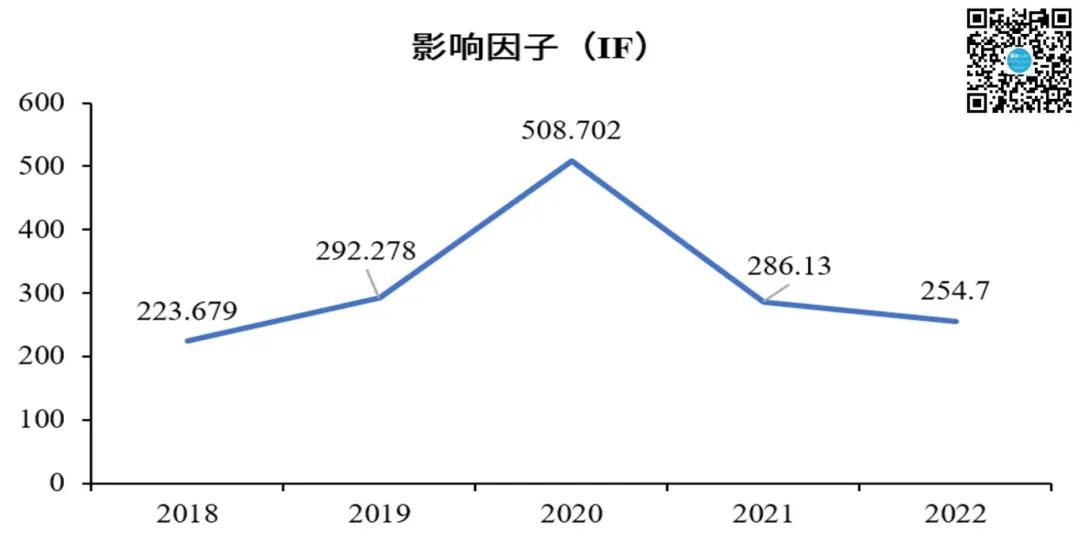
▲ 神刊CA:近5年的影响因子
2024年4月4日,美国癌症协会在CA杂志(IF=254.7)发布了最新的《2024年全球癌症统计报告》,文章指出,2022年全球约有2,000万新发癌症病例,同期约有970万人死于癌症。此外,预计到2050年,全球癌症新发病例数将达3,500万,死亡率可能翻一倍。1

▲ 神刊CA:2024年全球癌症统计报告
高死亡率的部分原因在于癌症的诊断往往滞后,这主要归咎于癌症通常在晚期才被发现。在晚期阶段,癌细胞的扩散往往使得治疗选择变得极为有限,从而大大降低了治愈的可能性。
正因如此,癌症早筛显得尤为重要。早筛意味着在癌症尚处于可控制、可治疗的早期阶段时,就能够发现它的踪迹,从而提高治愈率,降低死亡率。基于血液的多癌早检(MCED)概念引起了广泛关注,其中一个重要原因在于这种检测方法有望通过覆盖目前无法筛查的癌症类型,从而降低死亡率,而这些癌症占癌症死亡的65%。2
2024年3月22日,美国国家癌症研究所(NCI)癌症预防部门牵头在CA杂志(IF=254.7)上发表一篇题为“利用多癌检测(MCD)进行癌症筛查:转化科学综述”的综述文章,旨在探讨多癌筛查领域现状。3 此外,NCI也于2024年启动了新的癌症筛查研究网络(CSRN)项目,以评估使用多癌检测进行筛查癌症的好处是否利大于弊,以及它们是否能够及早发现癌症,从而降低死亡率,进而支持拜登政府“癌症登月计划”的癌症预防目标。4

▲ 神刊CA:多癌检测测试的癌症筛查综述
癌症筛查的目的是在更早、更容易治疗的阶段发现癌症,从而降低癌症死亡率。现代癌症筛查方法具有器官特异性(单癌检测),旨在早期发现常见癌症,并且具有高灵敏度。
多癌检测(MCD)顾名思义就是针对多种不同类型的癌症进行检测的技术或方法。这种检测旨在通过使用单一的、易于获得的生物样本来同时筛查多种癌症,从而提高癌症的早期发现率,为患者争取更好的治疗时机。多癌检测和单癌检测的诊断性能均受阳性预测值(PPV)影响,即检测阳性实际罹患癌症的概率。但多癌检测的PPV更依赖于特异性而非灵敏度,因为多癌检测中涵盖了众多低发病率癌症。5 这一特性使得多癌检测在癌症筛查中具有独特地位。
注意:实验研发时常使用多癌早检(MCED)这一术语,然而,关于其是否能有效发现无症状癌症并改善健康状况,目前仍存疑问。鉴于缺乏充分证据表明此类检测能以足够高的准确率捕捉早期癌症,或显著降低晚期疾病的发病率,因此,NCI倾向于将MCED(多癌早检)称为MCD(多癌检测)。多癌检测(MCD)不是简单的血液检测。相反,MCD是一种筛查检测,可在没有做出明确诊断的情况下评估癌症存在的可能性。当检测结果标明癌症的可能性增加时,有必要进行进一步的诊断检查。
因此,我们可以认为:多癌检测 ≈ 多癌筛查。
基于ctDNA的液体活检技术,为多癌检测开发提供了重要支持。ctDNA检测隐匿性恶性肿瘤的原理最初是在进行NIPT筛查的妇女中偶然检测到癌症而得到证实的。6
大多数多癌检测旨在评估ctDNA的多个特征,如突变谱、甲基化和片段化等特征。目前,多癌检测除ctDNA外还会使用其他生物标志物,如CTC、cfRNA、蛋白质、代谢物、多聚糖、细胞外囊泡(包括外泌体)、肿瘤诱导血小板和癌症干细胞等,它们存在于血液或其他体液中, 如尿液、唾液和脑脊液等。

▲ 用于开发MCD的分析物和技术
多癌检测依赖于不同组织癌细胞的共同生物学特性,通过检测血液或其他体液中释放的肿瘤成分作为癌症生物标志物。
多癌检测通常比较复杂,涉及多种分子标志物,并运用复杂的统计算法(包括AI和机器学习建模)来设定阳性和阴性阈值。通过对比癌症患者和非癌症患者的诊断结果,不断优化并完善训练集模型和验证集模型,以提升模型的准确性和可靠性。此外,AI和机器学习还可用于癌症溯源。
目前公开报道的多癌检测产品较多,根据实验室开发到临床应用实践主要分为5个阶段(NCI早期检测研究网络,EDRN)。现在大多数多癌检测都处于早期开发阶段,它们的诊断性能是根据回顾性研究进行训练和验证的。当前,有两个多癌检测产品(Grail/Galleri;Exact/CancerSeek)处于前瞻性筛查研究阶段(即EDRN第4阶段)。由于目前可用的多癌检测产品均未完成第5阶段的前瞻性临床效用验证(是否降低了死亡率?),因此,NCI集体评估认为,多癌检测尚未证明可以在普通人群中进行常规筛查。
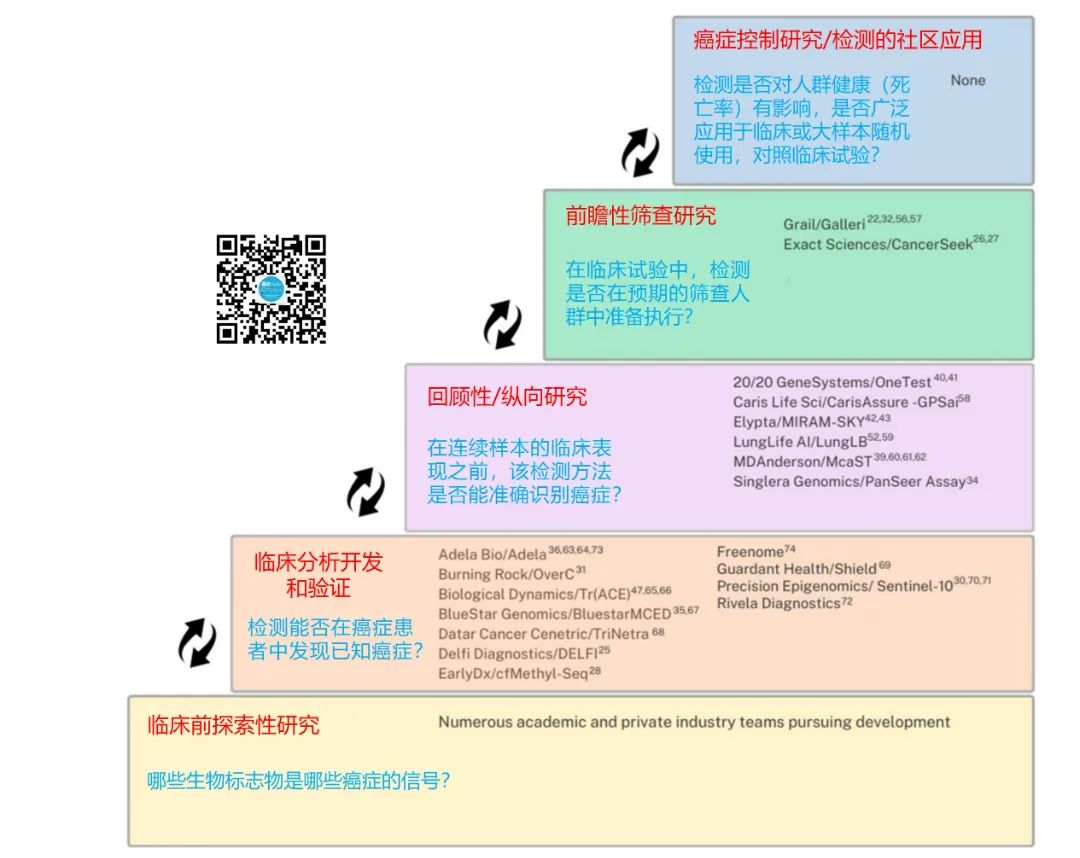
▲ MCD从实验室到临床实践转化的5个阶段(EDRN)
目前,多癌检测的非随机前瞻性研究包括Pathfinder和DETECT-A两项;唯一的随机对照试验(RCT)是英国国家医疗服务体系的Galleri试验,已招募超14万名受试者,主要研究终点是癌症早检率,次要研究终点是死亡率。
尽管关键试验正在进行中,但没有一项试验的主要目标是评估基于人群的多癌检测/筛查对癌症死亡率的影响。因此,NCI于2024年1月启动了一个新的癌症筛查研究网络(CSRN)项目,重点关注癌症筛查临床介入和观察研究。7 该项目将启动一项名为多癌症检测先锋研究(Vanguard研究)的试点研究,以解决在未来随机对照试验中使用多癌检测的可行性。该研究将招募多达24,000人,为更大规模的随机对照试验的设计提供信息。这项更大规模的试验将评估使用多癌检测进行筛查癌症的好处是否利大于弊,以及它们是否能够及早发现癌症,从而降低死亡率。
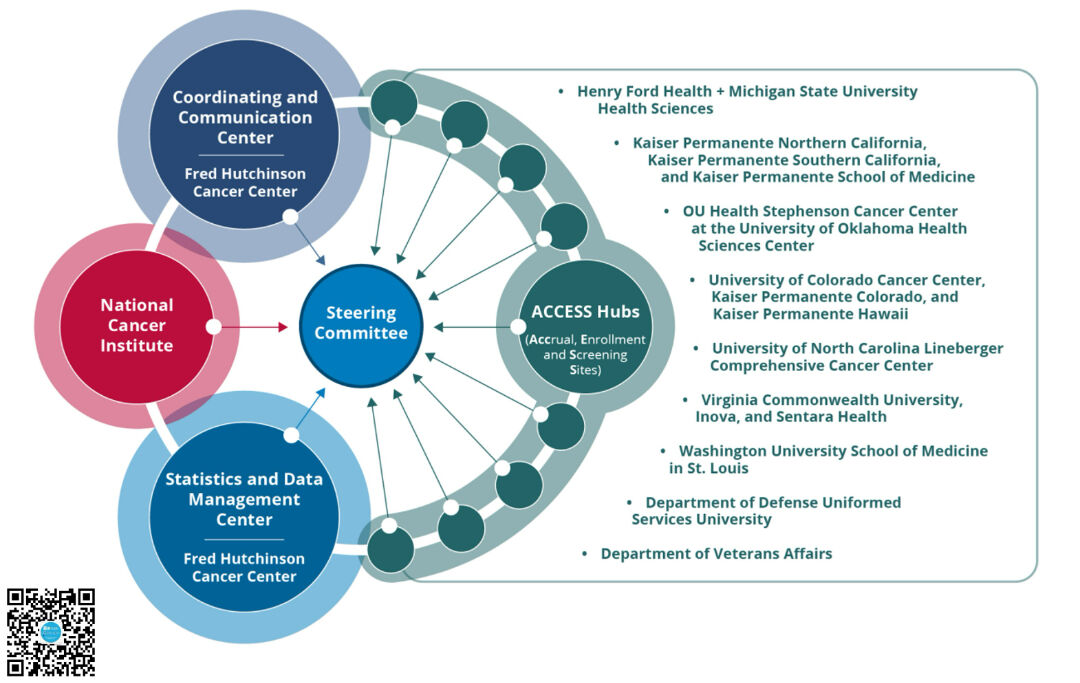
▲ NCI启动CSRN项目评估MCD临床效用
尽管多癌检测在癌症筛查上有望带来显著进步,但同时也伴随着新的挑战。
(1)【识别效能】多癌检测阳性信号并不能直接确诊癌症,还需额外的方法来溯源并做出病理诊断。这些方法可能包括全身影像等,但其效果并不完善。目前,评估多癌检测性能的临床证据框架仍在发展中,FDA也尚未发布相关指南。在无症状个体筛查中,真阳性的识别依赖于诊断检查的有效性,但部分真阳性结果可能因后续诊断不够灵敏而无法确认,导至结果的不确定性。此外,对于从阳性到癌症诊断的完整过程所需时间没有标准定义,且如何追踪诊断阴性患者及避免遗漏潜在癌症也存在不确定性。
(2)【疾病定义】多癌检测的灵敏度取决于疾病的定义,而疾病的定义在已发表的研究中有所不同。例如,疾病可以定义所有阶段检测到的所有癌症,也可以定义为所有阶段的单一癌症,也可以定义为可检测癌症的早期阶段,也可以定义为单一癌症的早期阶段。早期癌症的定义范围从癌症病变到症状前III期阶段,缺乏标准化定义限制了评估多癌检测的诊断性能能力。目前,大多数多癌检测设计具有高检测特异性,以减少因假阳性结果而进行的诊断评估。
(3)【临床效用】对于目前没有常规筛查的癌症,没有证据表明晚期疾病发生率降低与死亡率降低有关。一些试验表明晚期发病率有所降低,但死亡率并未降低。所以,基于癌症分期转变的绩效指标可能会人为地夸大使用多癌检测进行癌症筛查的价值。
(4)【灵敏度&特异性】目前,多癌检测对所有阶段检测到的所有类型癌症的灵敏度范围为27%~95% ,特异性为95%–99%。尽管多癌检测的目标是在早期发现更多的癌症,但与晚期癌症(III期约为60%-87%)相比,早期癌症(I期约为27%-62%)的灵敏度较低。此外,对于建议常规筛查的癌症,某些多癌检测产品的早期灵敏度远低于常规筛查手段(例如,I期乳腺癌5%,I期结直肠癌30%8),因此,仅使用多癌检测就会漏掉许多癌症。所以,无论多癌检测结果如何,都建议进行常规筛查。
(5)【过度诊断】筛查无症状个体可能会导至过度诊断——检测出缓慢生长的癌症,这些癌症不会导至发病或死亡,但却使患者面临无效或有害的治疗。例如,在韩国实施的甲状腺癌超声筛查,导至发病率增加了1500%,这是由生长较慢的亚型(乳头状甲状腺癌)驱动的,甲状腺癌的死亡率没有相应下降,但许多人暴露在侵入性手术的危害之下。9,10
多癌检测可筛查多种癌症,包括缺乏常规推荐筛查的癌症,具有潜在进步性。但在临床实践中应用前,需证明其健康获益。迄今为止,尚未有发布多癌检测使用的临床实践指南,FDA尚未授权营销任何多癌检测产品,健康计划的覆盖范围也有限。尽管如此,临床医生和广大公众现在仍面临着是否使用多癌检测的决定。同时,他们应认识到进行多癌检测的复杂性和不确定性。
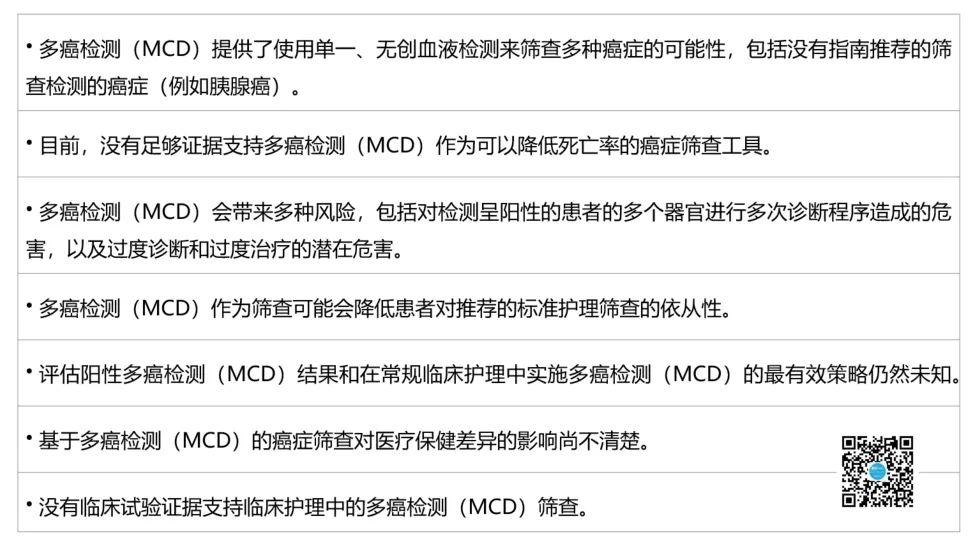
▲ 使用MCD进行癌症筛查的机会、证据差距和风险
NCI于2024年发起的Vanguard研究和未来的RCT研究将严格评估多癌检测技术作为癌症筛查工具的临床效用。通过这些研究和其他研究及利用真实世界数据的研究,医学界可以确定各种多癌检测是否适合实施并接受有关如何进行诊断检查的指导。
若多癌检测能更早识别患者,则需新疗法或改进现有方法降低死亡率。通过多癌检测无症状患者的肿瘤成分可能具有预后意义,并可能影响癌症分期。高风险人群,如遗传性癌症综合征或癌症病史者,或可从多癌检测的筛查中获益最多。随着有效、个性化癌症风险评估新方法的开发,在最佳时间点为每个人匹配最佳检测并根据他们的风险状况进行定制将有助于优化该技术的使用。
综合而言,多癌检测具有通过非侵入性筛查降低癌症发病率和死亡率的潜力。然而,实施前需前瞻性临床试验证明其有效性,评估诊断结果,并关注过度诊断、过度治疗及筛查依从性等问题。为此,NCI正资助启动了一个新的癌症筛查研究网络(CSRN)项目以填补知识空白,加速该领域的快速发展。
参考资料:
1.Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. Published online April 4, 2024.
2.Siegel RL, Miller KD, Wagle NS, Jemal A. Cancer statistics, 2023. CA Cancer J Clin. 2023; 73(1): 17-48.
3.Rubinstein WS, Patriotis C, Dickherber A, Han PKJ, Katki HA, LeeVan E, Pinsky PF, Prorok PC, Skarlupka AL, Temkin SM, Castle PE, Minasian LM. Cancer screening with multicancer detection tests: A translational science review. CA Cancer J Clin. 2024 Mar 22.
4.https://prevention.cancer.gov/major-programs/cancer-screening-research-network-csrn
5.Ahlquist DA. Universal cancer screening: revolutionary, rational, and realizable. NPJ Precis Oncol. 2018; 2(1): 23.
6.Bianchi DW, Chudova D, Sehnert AJ, et al. Noninvasive prenatal testing and incidental detection of occult maternal malignancies. JAMA. 2015; 314(2): 162-169.
7.National Institute of Cancer (NCI). Screening Research Network (CSRN). NCI Division of Cancer Prevention; 2024. Accessed February 2, 2024.
8.Liu MC, Oxnard GR, Klein EA, Swanton C, Seiden MV; CCGA Consortium. Sensitive and specific multi-cancer detection and localization using methylation signatures in cell-free DNA. Ann Oncol. 2020; 31(6): 745-759.
9.Park S, Oh CM, Cho H, et al. Association between screening and the thyroid cancer “epidemic” in South Korea: evidence from a nationwide study. BMJ. 2016; 355:i5745.
10.Ahn HS, Kim HJ, Welch HG. Korea's thyroid-cancer “epidemic”—screening and overdiagnosis. N Engl J Med. 2014; 371(19): 1765-1767.
 /3
/3 