金桔
金币
威望
贡献
回帖0
精华
在线时间 小时
|
??????这什么离谱新闻,村里刚通网吗?
众所周知,艾滋病病毒属于逆转录病毒,这种病毒会把自己的基因插入到宿主的基因组里,导致难以清除。
而目前主流的艾滋病治疗方法主要是抗逆转录病毒疗法,也就是说虽然我们不能阻止 HIV 病毒插入到患者的基因组,但我们可以让这个病毒不复制,降低患者体内的病毒载量,在降低到非常低的时候,就近似于治愈了。但这种办法治标不治本,需要长期服药,会有持续的副作用,以及可能的耐药性。
早在 CRISPR 技术诞生之初,甚至更早有基因敲除技术的时候,就有科学家提出过用基因敲除技术来治疗艾滋病。
毕竟 CRISPR 技术最容易应用的方法就是NHEJ,也就是非同源末端连接。道理很简单,用CRISPR 靶向一个重要的基因,将其切断,切断以后的基因会进行重组修复,而这种修复是随机的,修复好的基因大概概率跟以前的不一样,这从功能意义上来说就是破坏掉了这个基因,所以也可以叫做基因敲除。我们在实验室就经常运用这个方法来验证某些基因的功能性。
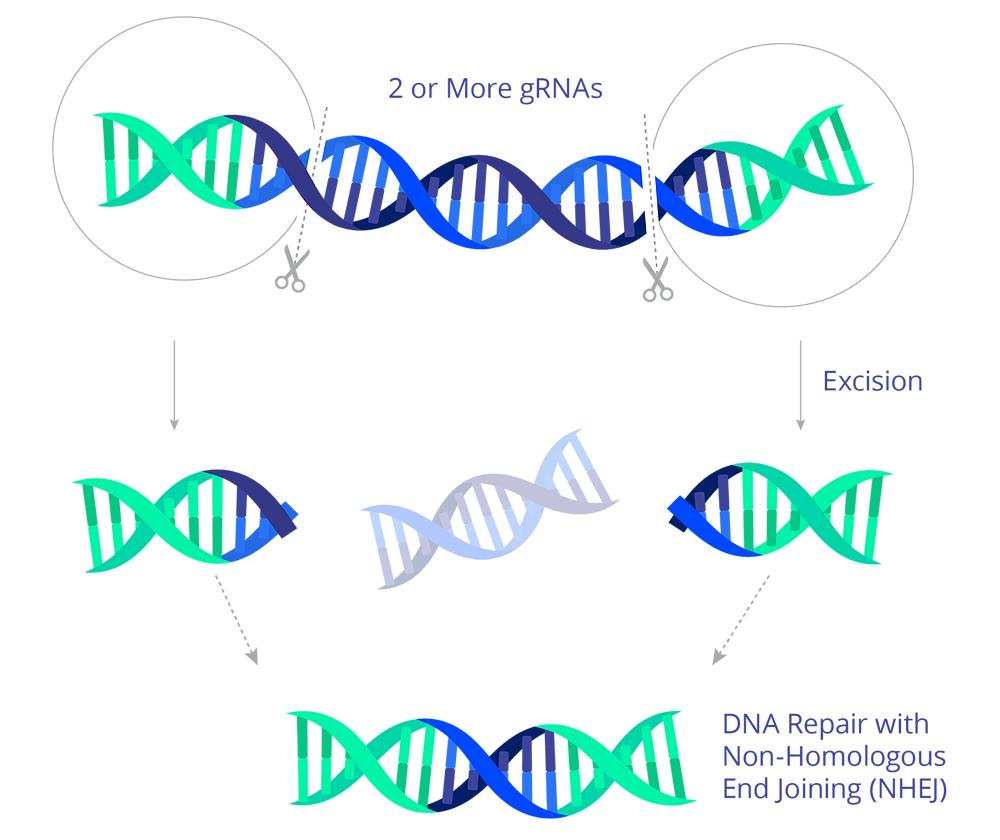
那针对于 HIV 病毒会把自己基因组插入到宿主的基因组,那是不是我们用类似的方法去剪HIV 插入到人体的基因以后,是不是就可以破坏掉 HIV 病毒了呢?
当然可以啊。而且这方面的研究在前些年就有了重要的突破。

就是这篇,估计很多做 CRISPR或者 HIV 治疗的同行都看过这篇论文
当时这个实在灵长类动物的体内切掉了 SIV-a病毒。SIV 病毒是猴免疫缺陷病毒,对,就是 HIV 的近亲。当时学界普遍认为,能用 CRISPR 切掉猴子体内的 SIV,那同理就可以切掉人体内的 HIV。
当时科学家担心一次切除不稳妥,他们还做了多个位点的反复切除。当然这也增加了脱靶的可能性。
但无论如何,这种在猴子的体内切除掉 SIV 的进展,比这个题目里说在人类体外细胞里切掉 HIV 的进展要高的多的多。而且,这是 20 年的论文了。
另外这事情不是发了个 paper 就完事了,还有后续。
Excision BioTherapeutics公司获得了这篇论文研究者的授权,开始着手把这项技术运用到人的身上来治疗艾滋病。 21 年底就获得了 FDA 的批准开启了临床。
而且这事情还有后续,在2023年10月25日,Excision BioTherapeutics在第30届欧洲基因与细胞治疗学会(ESGCT)年会上上介绍了正在进行EBT-101治疗艾滋病的1/2期临床试验的积极中期数据。
该公司表示,建立EBT-101的安全性和生物分布是临床计划中重要的第一步。在前三名临床试验参与者中,使用EBT-101治疗没有导致严重的不良事件或剂量限制毒性,所有报告的不良事件都是轻微和可逆的。此外,所有参与者的血液中检测到EBT-101,治疗产生了积极的生物分布。这些初步观察提供了重要的临床数据,支持将该临床试验推进到下一个剂量水平(从9.0x1011vg/kg提高到3.0x1012vg/kg)。
人家这技术已经到1/2期临床了,然后新闻里的这条才到体外细胞In vitro阶段,这差这十万八千里呢,就更别提评论里提到的那个“概念证明”阶段……但凡你在知乎上搜一下,也不能这么说啊,所以,我只能说这个新闻编辑村里刚通网吧。
<hr/>我刚才好奇去找了下信源,国内的主要是来自于环球时报科学板块对于 BBC 的报道的翻译,然后我去查了下 BBC 的原文。
Scientists say they can cut HIV out of cells
Scientists say they have successfully eliminated HIV from infected cells, using Nobel Prize-winning Crispr gene-editing technology.
Working like scissors, but at the molecular level, it cuts DNA so &#34;bad&#34; bits can be removed or inactivated.
The hope is to ultimately be able to rid the body entirely of the virus, although much more work is needed to check it would be safe and effective.
Existing HIV medicines can stop the virus but not eliminate it.
The University of Amsterdam team, presenting a synopsis, or abstract, of their early findings at a medical conference this week, stress their work remains merely &#34;proof of concept&#34; and will not become a cure for HIV any time soon.
And Dr James Dixon, stem-cell and gene-therapy technologies associate professor at the University of Nottingham, agrees, saying the full findings still require scrutiny.
&#34;Much more work will be needed to demonstrate results in these cell assays can happen in an entire body for a future therapy,&#34; he said.
&#34;There will be much more development needed before this could have impact on those with HIV.&#34;
&#39;Extremely challenging&#39;
Other scientists are also trying to use Crispr against HIV.
And Excision BioTherapeutics says after 48 weeks, three volunteers with HIV have no serious side effects.
But Dr Jonathan Stoye, a virus expert at the Francis Crick Institute, in London, said removing HIV from all the cells that might harbour it in the body was &#34;extremely challenging&#34;.
&#34;Off-target effects of the treatment, with possible long-term side effects, remain a concern,&#34; he said.
&#34;It therefore seems likely that many years will elapse before any such Crispr-based therapy becomes routine - even assuming that it can be shown to be effective.&#34;
HIV infects and attacks immune-system cells, using their own machinery to make copies of itself.
Even with effective treatment, some go into a resting, or latent, state - so they still contain the DNA, or genetic material, of HIV, even if not actively producing new virus.
Most people with HIV need life-long antiretroviral therapy. If they stop taking these drugs, the dormant virus can reawaken and cause problems again.
A rare few have been apparently &#34;cured&#34;, after aggressive cancer therapy wiped out some of their infected cells, but this would never be recommended purely to treat HIV. 嗯,人家原文的报道还是很正经的,本身这是一项发表在今年的ECCMID会议上的摘要,还看不到正式的结果,ECCMID是欧洲最大的感染学会议。在 BBC 的原报道中也提到了Excision BioTherapeutics的临床进展,还附上了链接。而且那个“概念证明”是阿姆斯特丹的研究小组自己的评价,他们自己认为自身的研究距离临床还比较远。
同时仔细的看了下他们的研究内容,也并不是像是题目中简单的提到的在体外细胞中清除掉 HIV 病毒,还是有很多重要的内容的,不然也上不了 ECCMID。
首先研究小组,在尝试缩小 CRISPR 递送系统的大小,这点是很重要的。很多时候基因编辑的难题都是卡在递送系统上了,能减小递送系统是很重要的,可以有效的提高递送的成功率。
另外研究团队评估了来自不同细菌的 Cas 系统在治疗 HIV 感染的 CD4+的 T 细胞方面的有效性,最后认为 saCas9 的效果是最好的。剪一个位置就可以灭活 HIV,如果剪 2 个不同的位置,就可以切除掉病毒插入在宿主体内的 DNA。
还有就是研究人员还关注这个疗法的的靶向性问题,这里的靶向性不是说对基因的靶向性,而是递送的靶向性。毕竟 HIV 病毒感染人体的细胞是特异性的,而非全身,所以如何靶向性的把基因编辑工具送到需要去编辑的细胞里也是很重要的,这个在减少脱靶以及其他的副作用下是非常有意义的。研究人员关注的是CD4+和CD32a+细胞表面的特定蛋白质来靶向隐藏的HIV储存细胞。
概括下来说就是,Elena Herrera-Carillo博士的团队已经开发了一种有效的组合CRISPR攻击,可以针对各种细胞中的HIV病毒及其可以隐藏在储库中的位置,并证明可以特异性地将治疗药物递送至感兴趣的细胞。这些发现代表了设计治疗策略的关键进展。
这比原新闻报道,甚至是 BBC 的报道的内容差异性差了很大。
另外关于 @麻瓜 老师提示的信息,该研究组在 2022 年的一篇关于使用基因编辑技术治疗 HIV 时可能造成 HIV 变异的问题的研究也很有趣,这种很可能会造成养蛊的情况。 |
|
 /3
/3 