金桔
金币
威望
贡献
回帖0
精华
在线时间 小时
|
登陆有奖并可浏览互动!
您需要 登录 才可以下载或查看,没有账号?立即注册


×
上一篇专栏是诺贝尔化学奖颁奖当天写的,比较匆忙,后来同学的师姐找我给Wiley旗下的Materials Views China写专栏,我就梳理了一下,系统地聊一下分子机器,写了六篇专栏文章,现全文转载。
本文请勿转载,如需转载请联系Materials Views China.
原文链接:
听诺奖弟子聊分子机器 | 分子机器是什么
听诺奖弟子聊分子机器 | Sauvage和他的金属离子配位合成索烃策略
听诺奖弟子聊分子机器 | Stoddart和他的分子梭与模板合成
听诺奖弟子聊分子机器 | Feringa和他的分子马达与纳米小车
听诺奖弟子聊分子机器 | 那些没得诺奖的人和他们的分子机器
听诺奖弟子聊分子机器 | 分子机器的研究现状和未来的挑战
以下是全文:
听诺奖弟子聊分子机器 | 分子机器是什么
2016年的诺贝尔化学奖颁给了Jean-Pierre Sauvage, J. Fraser Stoddart和Bernard L. Feringa, 表彰这三位科学家在设计与合成分子机器上做出的卓越贡献。在这之前,分子机器对于普通大众来说是非常陌生的名词,其实,即使是在学术界,相比于当下非常火热的领域如钙钛矿电池和石墨烯来说,分子机器也是一个相对小众的研究领域。因为分子机器属于基础研究,理念非常超前,而且极富挑战性,所以主攻该方向的研究者并不多。
那么分子机器是什么呢?这个概念最初是分子生物学的术语,因为过去半个世纪分子生物学家们向我们揭示了许多生命运转的秘密。许多生命活动和新陈代谢都在生物大分子如机器般的运转下实现。例如,1997年的诺贝尔化学奖颁发给了PaulD. Boyer, John E. Walker和Jens C. Skou以表彰他们在发现钠钾泵和ATP合成酶的工作机制上的贡献。钠钾泵可以利用ATP供能钾离子送进细胞并将钠离子送出细胞,维持细胞膜内外的离子浓度平衡,由于运输是逆浓度梯度的,和我们日常生活中的泵有相似之处,所以被称为钠钾泵。ATP合成酶则是镶嵌在线粒体内膜上利用呼吸链产生的膜间质子浓度梯度将ADP转化为ATP的酶。ATP合成酶工作的时候如同马达一样单向旋转,亦可以反向旋转水解ATP同时主动运输质子到高浓度处。除此之外,还有细菌鞭毛,驱动蛋白,核糖体等等一系列生物大分子机器,它们的协同工作造就了丰富多彩的生命世界。哈佛大学曾做过一个名为Inner Life of the Cell的视频动画描绘这些分子机器在细胞内的工作场景,如视频所示(来自优酷)。
The Inner life of the cell(中文字幕)—在线播放—优酷网,视频高清在线观看
http://v.youku.com/v_show/id_XMTMzMjk3MTc2.html
Youtube: https://www.youtube.com/watch?v=FzcTgrxMzZk
科学的发展往往遵循着理解自然,模拟自然,超越自然的规律。在生物学家们揭示了自然界中的分子机器的运转原理后,化学家们则想要通过设计人工合成的小分子来模拟这些大分子,最终希望能有超越自然的分子或材料被发明出来造福人类。自上个世纪八十年代开始,就有一批科学家致力于设计人工合成的小分子机器,他们通过有机合成构建一些内部可以相对运动的小分子来实现像机器一样的功能。Sauvage和Stoddart主要用机械互锁分子来实现分子中的相对运动,而Feringa则用的是位阻烯烃的顺反异构实现分子中的转动。笔者将在之后的专栏文章中分别介绍他们的工作。
分子机器中的一大部分都是机械互锁分子,所谓机械互锁分子就是指一个分子中有至少两个部分之间没有直接共价键相连,但却无法在不切断共价键的情况下将这些部分分开,维系这些部分的键被称为机械键。机械互锁分子最常见的两大类是索烃(Catenane)和轮烷(Rotaxane)。索烃是由两个或两个以上的环互相扣在一起,而轮烷则是一个环穿在一根两边封端的轴上。索烃和轮烷可以实现一些基本的机械式的运动,比如索烃中的一个环可以绕另一个环转动,而轮烷中的环可以沿着轴平移。
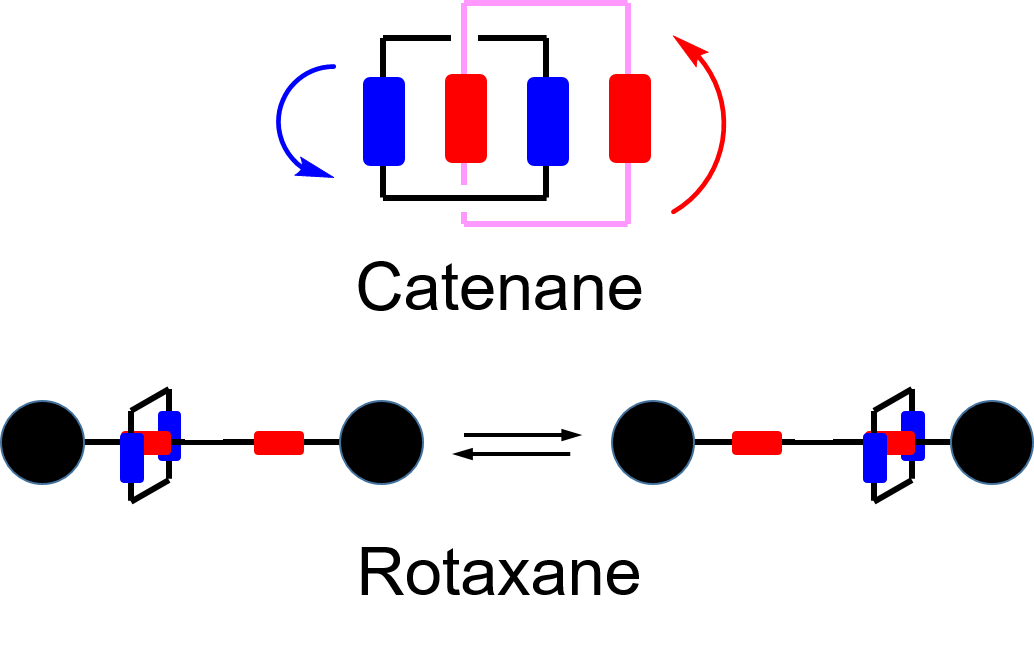
索烃和轮烷以及可实现的运动图示
此次诺贝尔化学奖颁布后,有不少人都认为这是超分子化学继1987年之后的第二次获奖,这种说法在笔者看来是不正确的。首先,虽然Sauvage和Stoddart都算是超分子化学家,所用到的机械互锁分子的模板合成也用了很多超分子化学的原理,但最终得到的索烃和轮烷都是分子而非超分子。其次,Feringa并不能算是超分子化学家,他应该是传统的有机化学家,而且他的分子马达也是经典的有机小分子,与超分子化学并无直接联系。
如果我们回看历史,机械互锁分子其实是独立于超分子化学起源的。早在上个世纪六十年代初,就有化学家用最原始的方法合成了索烃,在溶液中让一条链状分子靠几率穿过一个环状分子关环,能以极低的产率获得索烃。之后化学家们用共价键将链连在环上,合环后再切断连接的共价键得到索烃。直到上个世纪八十年代,才由Sauvage最早提出了用金属离子配位的方法来合成索烃,大大提高了合成的产率,之后Stoddart用基于给受体的主客体化学模板合成了大量的索烃和轮烷,极大拓宽了机械互锁分子的合成方法,这才将机械互锁分子与超分子化学紧密的结合起来。
所以说,机械互锁分子与超分子化学有深厚的渊源,但并不能说机械互锁分子是超分子化学的一个分支。超分子化学的非共价相互作用并不是机械互锁分子所必须的。况且,本次诺贝尔化学奖是颁发给分子机器并不是机械互锁分子,所以不能说这是超分子化学第二次获得诺贝尔奖。但是不得不说,基于超分子化学的合成方法大大提高了机械互锁分子的合成效率,这使得基于机械互锁分子的分子机器大大受益蓬勃发展。
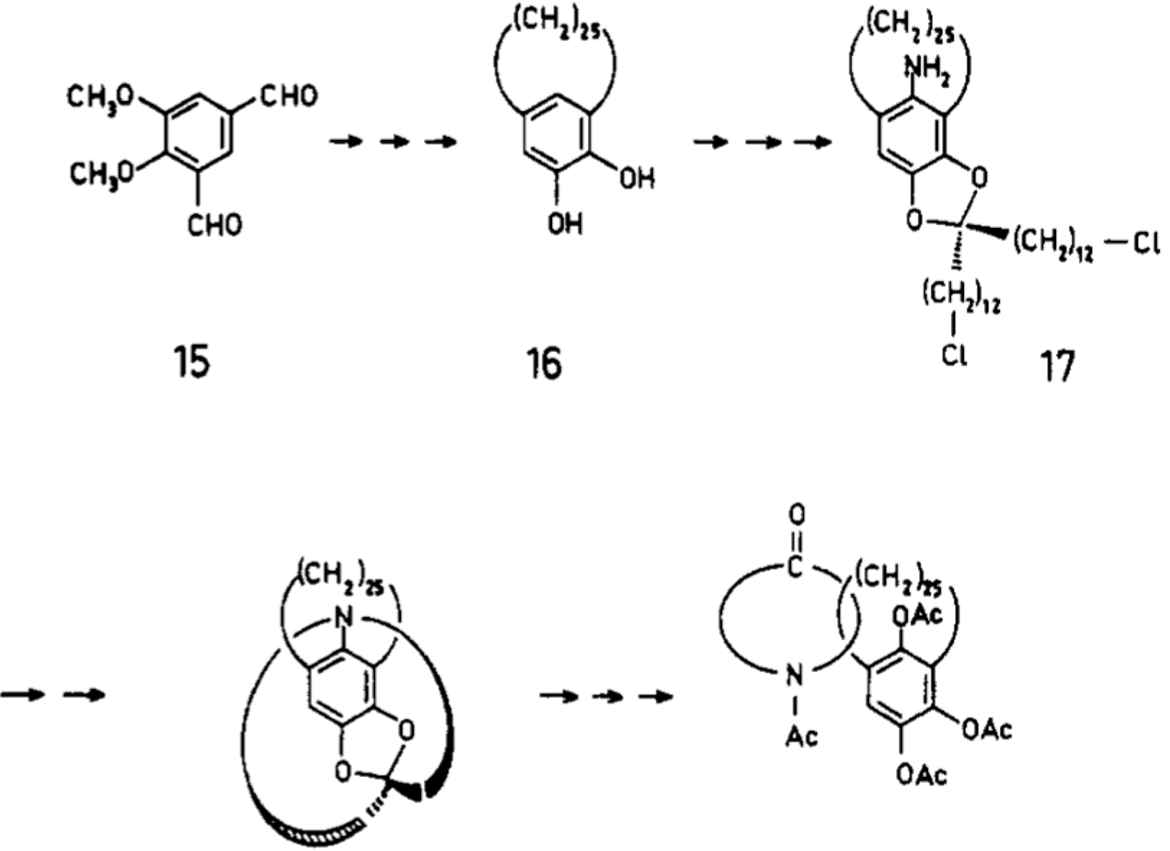
早期的共价键导向实现索烃合成的方法
参考文献:
1. ChristianeO. Dietrich-Buchecker, Jean-Pierre. Sauvage, Chem. Rev., 1987, 87, 795–810
2. Chuyang Cheng, J Fraser Stoddart, ChemPhysChem, 2016, 17, 1780–1793
听诺奖弟子聊分子机器 | Sauvage和他的金属离子配位合成索烃策略
此次诺贝尔奖的颁奖词是“设计与合成分子机器”,三人中Sauvage和Stoddart发展的分子机器都是基于机械互锁分子。关于机械互锁分子在上一篇专栏文章中已经有部分讨论,事实上Sauvage和Stoddart并不是最早做出机械互锁分子的科学家。早在1971年Schill就出版了一本机械互锁分子的专著,这年Sauvage才刚刚获得博士学位,我的导师Stoddart教授在给我们上课的时候把他称为“Schill the Grandfather”并且在获奖后的发布会也提到我们不应该忘了Schill这样的先驱。

图为1971年出版的Schill的专著
最早的机械互锁分子可以追溯到1960年的一篇JACS, 没有任何模板的情况下仅靠统计概率在溶液中让一条长链穿过一个环然后合环,得到了大概1%的两个环互锁的分子,应该是记载的第一个合成的索烃。
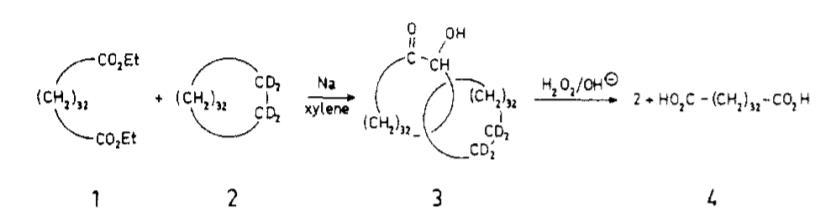
Wasserman在1960年合成的索烃
1964年Schill则采取了另一种策略,用共价键将需要机械互锁的两部分先连起来,合环后再切断连接的共价键,用这种方法合成了两个环的[2]索烃和三个环的[3]索烃. 但由于合成前体需要的步骤太长,最终产率很低,使得大量制备并不容易。
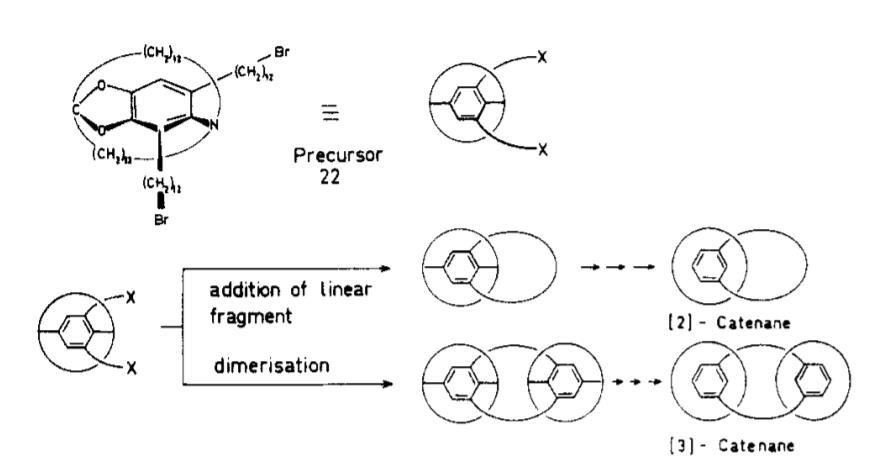
Schill用共价键导向策略合成的索烃
另一种可能性是用金属离子,在1961年和1972年分别由Wasserman和Sokolov提出过用金属离子配位将配体拉近的方法来合成索烃,然而最终实践的是Sauvage。在一篇1983年用法文发表在四面体快报上的四页的短文里,Sauvge提出了两种用金属离子配位合成索烃的方法,并成功地第一次实现了用铜离子配位合成索烃,用的是第二种策略,一步反应产率42%, 次年又以第一种策略一锅法27%产率得到同样的索烃。Sauvage的贡献是不言而喻的,他从当时商业可得的原料出发仅需三步就能以20%以上的产率得到索烃,克级以上的实验室制备成为了可能,这为机械互锁分子领域从那之后的发展奠定了坚实的基础。
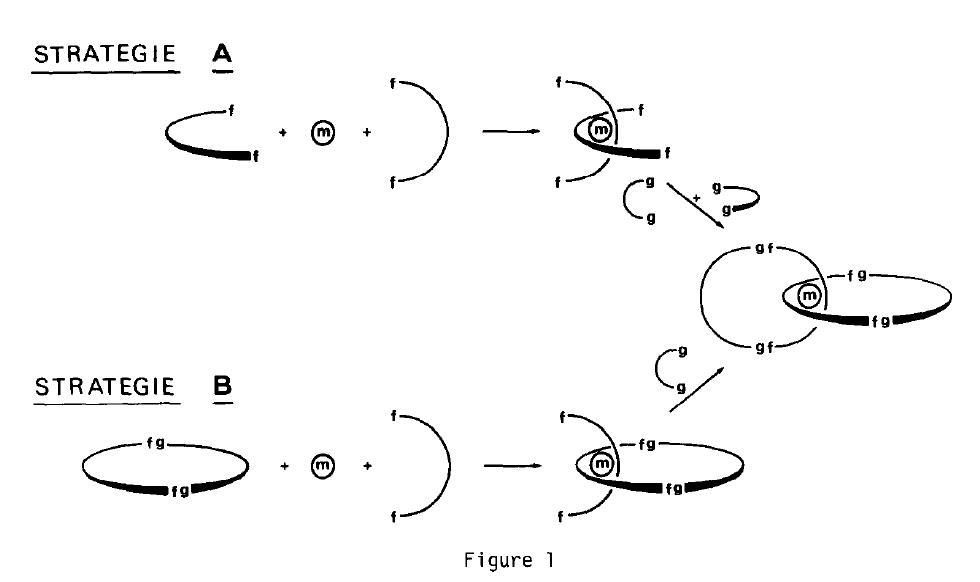
Sauvage在1983年提出的两种金属离子配位合成索烃的策略
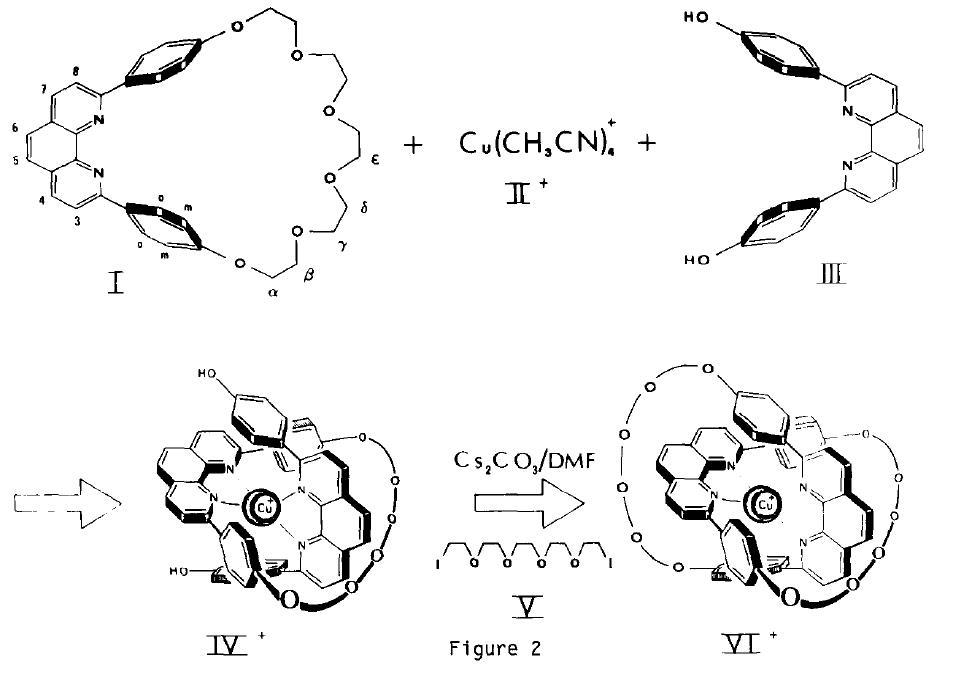
Sauvage用铜离子为模板合成的索烃
之后Sauvage一直活跃在机械互锁分子与分子机器领域直到大约2012年左右退休,做出了很多先驱性的工作,以下仅举几例。
1985年Sauvage的团队最早发表了索烃的晶体结构,包括铜离子配位和移除铜离子模板之后的结构,让人们“看到”了这种独特的分子。
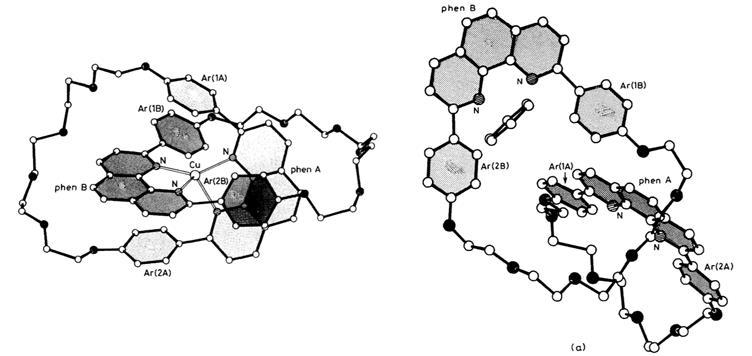
Sauvage于1985年发表的索烃的晶体结构
1989年Sauvage团队用同样的金属离子配位的策略合成了第一个分子三叶结。
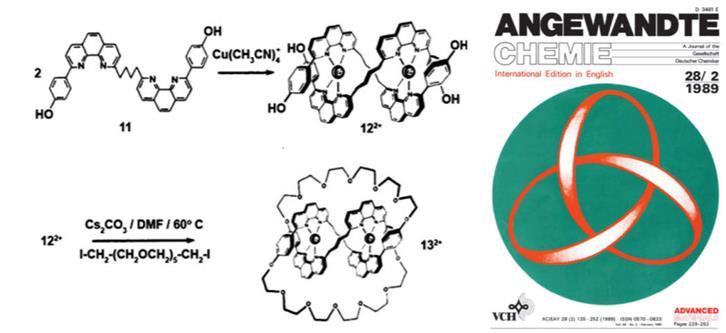
1989年Sauvage报导的分子三叶结和当期杂志的封面
1994年Sauvage团队通过在索烃的一个环中引入两个对一价铜和二价铜配位能力有选择性的基团实现了电化学控制索烃中一个环相对另一个环的摇摆运动。
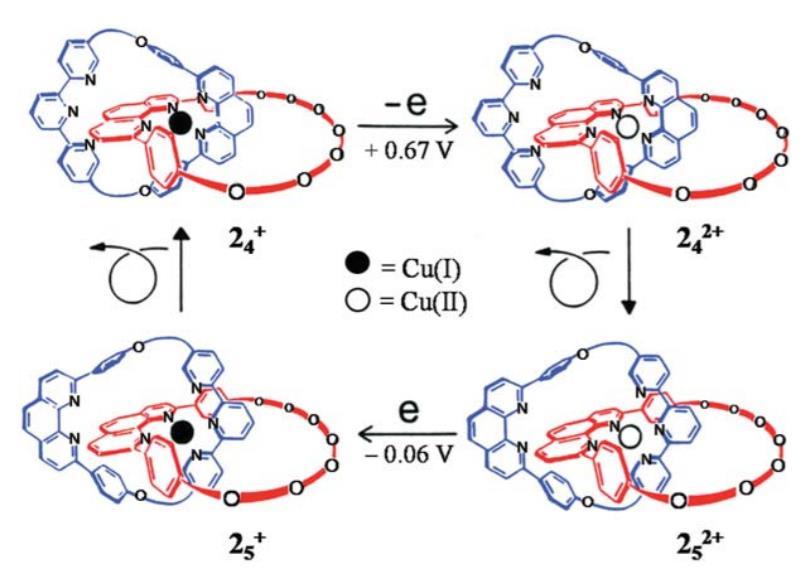
1994年报导的电化学控制索烃中大环的摇摆运动
2000年报导了可以压缩和舒张的轮烷二聚体,在加入不同的金属离子和配位剂的环境下可以实现缩短和伸长的运动,可以作为分子肌肉的原型!
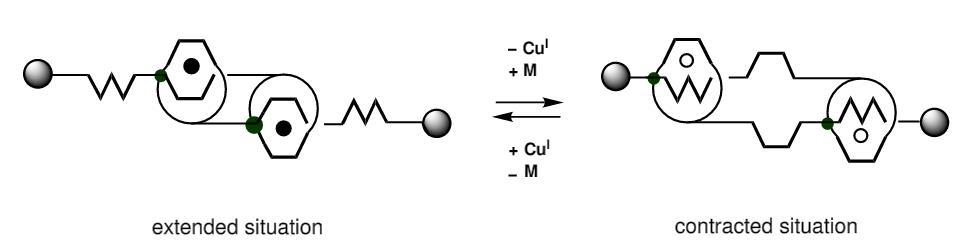
2000年报导的分子肌肉原型
最后,Sauvage的PhD导师是Jean-Marie Lehn,他1971年获得博士学位,是Lehn的第一个博士生,博士论文研究的是穴醚化合物的合成与性质, Lehn于1987年因对穴醚化合物的研究获得诺贝尔化学奖。所以这不单单是一个导师拿了诺贝尔化学奖,他的第一个学生也拿了诺贝尔化学奖的佳话,而是学生研究生期间的工作开启了导师拿诺奖的事业,自己当导师后开辟一片领域又拿了诺奖的传奇故事!

Sauvage展示索烃
参考文献:
- Christiane O. Dietrich-Buchecker, Jean-Pierre. Sauvage, Chem. Rev.,1987, 87, 795–810.
- Edel Wasserman, J.Am. Chem. Soc., 1960, 82, 4433–4434.
- O Dietrich-Buchecker, J.P Sauvage, J.P Kintzinger, Tetrahedron Lett. 1983, 5095
- Fraser Stoddart, Chem. Soc. Rev., 2009, 38, 1521-1529.
- Cesario, C. O. Dietrich-Buchecker, J. Guilhem, C. Pascard and J.-P. Sauvage, J. Chem. Soc., Chem. Commun., 1985, 244–247.
- Aude Livoreil, Christiane O. Dietrich-Buchecker, and Jean-Pierre Sauvage, J. Am. Chem. Soc., 1994, 116, 9399–9400
- Consuelo JimeÂnez, Christiane Dietrich-Buchecker,and Jean-Pierre Sauvage, Angew. Chem. Int. Ed.2000, 39, 3284–3287
听诺奖弟子聊分子机器 | Stoddart和他的分子梭与模板合成
上一篇介绍了Sauvage的工作,这一篇聊Stoddart,就不得不提到Sauvage和Stoddart的友谊。两人最早于1978年在意大利的一次会议上相识,自那之后一直保持了接近40年的密切的联系。笔者2011年开始在西北大学读博士,当时Sauvage还是西北的客座教授,每年都会来Stoddart的实验室访问数次和组里的研究人员讨论科学问题。

90年代的Sauvage和Stoddart
和Sauvage早年师从Lehn学习超分子化学,之后再研究机械互锁分子和分子机器不同,Stoddart算是半路出家大器晚成。Stoddart的祖师爷是Haworth(1937年诺贝尔化学奖得主,就是有机化学里学习糖化学的时候的Haworth结构式的发明人),研究生和早期工作都是研究糖的立体化学的。Stoddart在1971年的时候还写过一本《糖的立体化学》,所以现在Stoddart的论文里也会尽可能详尽的讨论机械互锁分子中的立体化学。

Stoddart于1971年发表的专著
70年代中期到80年代Stoddart的研究方向开始由糖化学转向研究冠醚的主客体化学,也算是比较早进入超分子化学领域的研究者。80年代末期研究了紫精环番和相关的主客体化学,并在之后的二十多年持续投入对紫精环番分子的研究。值得一提的是,Stoddart是推动文献彩色化的先驱者,上个世纪八十年代末期,Stoddart是最早在发表的纸质论文中使用彩图和用卡通表示化学结构的研究者之一。
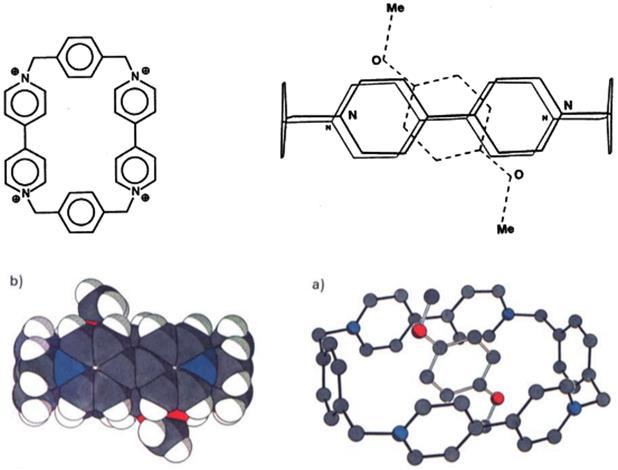
1988年发表的紫精环番的主客体化学研究
Sauvage使用金属离子配位将两个配体拉近合成机械互锁分子,而Stoddart则最早提出了基于给受体的模板合成。共轭的芳环体系中视其π电子云的密度可以分为富电子体和缺电子体。富电子体和缺电子体可以形成给受体复合物,拉近两个片段的距离。Stoddart利用这个原理在两端有大位阻封端基团的轴装分子中嵌入富电子的对苯二酚结构,使其和缺电子的紫精可以形成给受体复合物,再关环即可得到环锁在轴上的轮烷分子(rotaxane)。
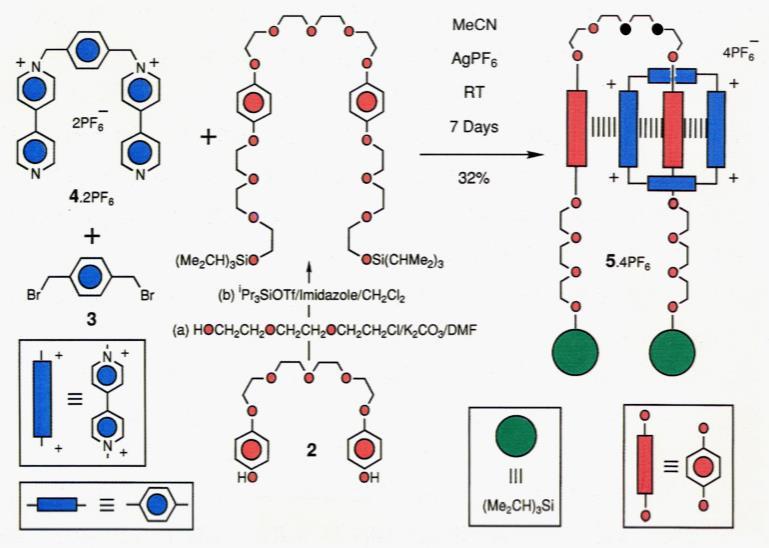
基于给受体模板合成轮烷
在这之前合成轮烷是很困难地,只能很小量地制备,比如1967年的一篇JACS将一个大环连在树脂上,让溶液中的长链在有封端剂的情况下反复反应和洗涤重复70次才得到了6%的轮烷。
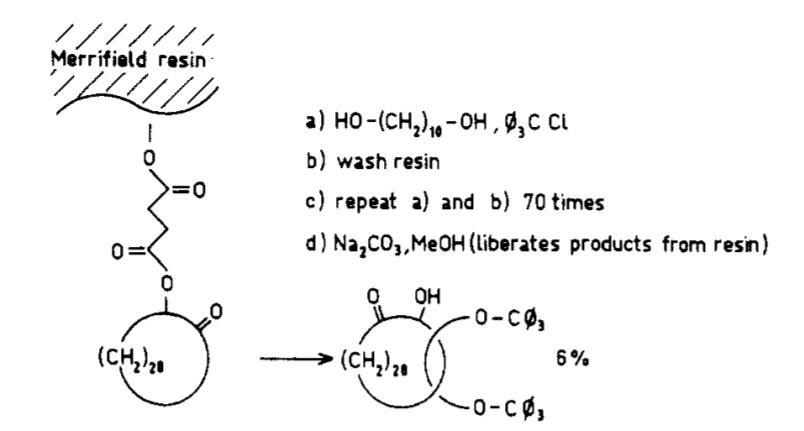
Harrison在1967年合成的轮烷
1991年Stoddart用模板合成制作了最早的分子机器,一根轴上有两个一样的富电子对苯二酚,于是缺电子的紫精环番可以自由地在两个站间往返,室温下速度往返速度超过1000次每秒,所以被命名为分子梭。
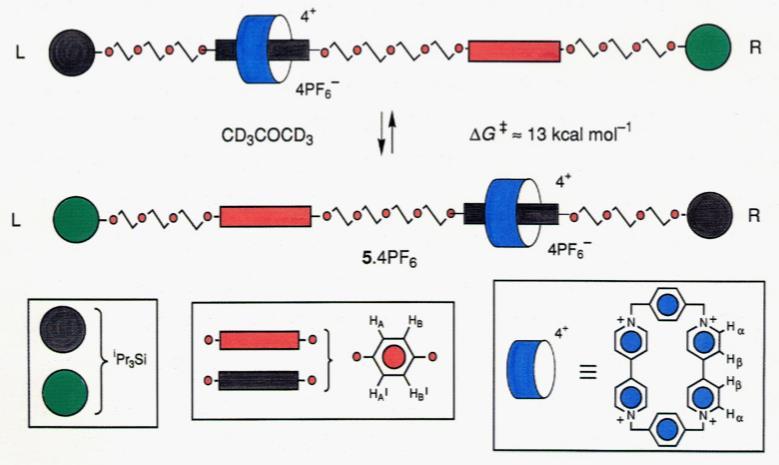
Stoddart于1991年发表的分子梭
上述由环境热驱动的分子梭是最早的分子机器原型,之后大约在同一时间,Sauvage和Stoddart都报导了引入外部刺激响应的分子机器。Sauvage的工作已经在上篇中提到是通过引入与一价铜和二价铜配位能力不同的基团控制索烃中大环的摇摆运动,而Stoddart则是将分子梭中轴上的两个等价基团换为不等价且可通过外部刺激控制其中一个和紫精环番的结合力。两个基团一个被换为了联苯二酚,另一个被换为了联苯二胺,由于连苯二胺更富电子,所以正常情况下紫精环番大部分都在联苯二胺上。当加入酸后质子化的联苯二铵变成缺电子基团,紫精环番将位移到联苯二酚上。同样的过程也可由电化学控制实现。
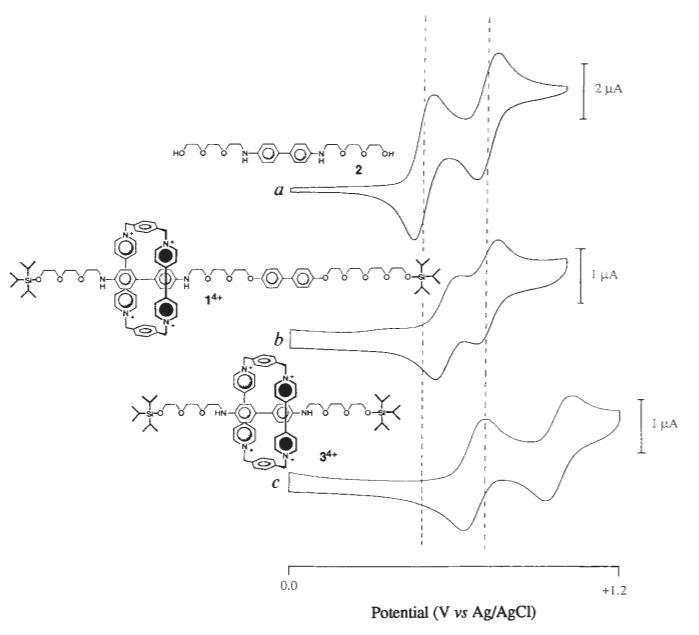
1994年发表的电化学控制的分子梭
这种可控地能在两个状态相互转化地分子之后被作为分子开关进一步深入研究,Stoddart从90年代末期开始联合James Heath等人做了许多相关的分子电子学研究,发展了一系列的分子逻辑门,其中最突出的工作是在2007年发表的基于轮烷的高密度存储器件,今天的商业存储设备的存储密度也没有赶上当年的结果。
分子开关是分子机器中的一大类,其特点是可以在外界刺激下在多个热力学平衡态下相互转化。外界输入能量,分子开关弛豫到新的热力学最稳态,所以本身只能记录状态并不能对外做功。而分子马达则要求在外界能量输入下有一定的能量转化为功对外输出,需要动力学控制。Stoddart于2010年发现紫精环番与紫精在还原时形成三自由基复合物,之后将其引入分子机器的设计,于2015年报导了可以将两个紫精环番从溶液中富集到烷基链上的分子泵。设计利用了还原时自由基相互吸引,氧化时同种电荷相互排斥,巧妙布置库伦和位阻能垒构建了一个能量棘轮。两个紫精环番分子从溶液中被“泵”到烷基链上是熵和焓都不利的过程,升高的自由能来自于分子泵转化的氧化还原化学能,分子泵做了功。这个工作正是笔者的博士论文内容。
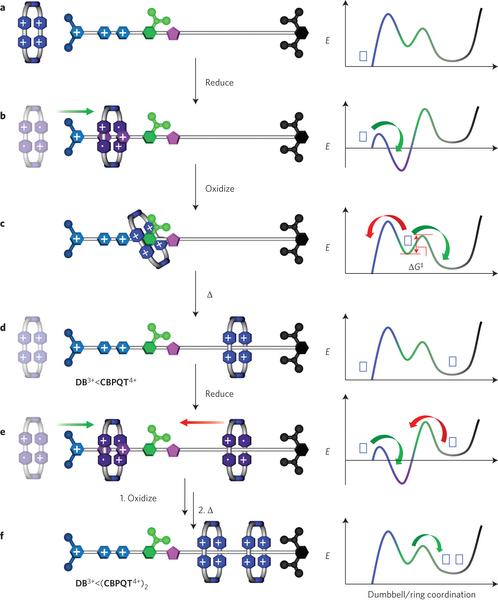
2015年报导的分子泵
Wiley出版社11月将出版Stoddart的专著《机械键的本质:从分子到机器》,这本书是我的师兄CarsonBruns和老爷子一起花了大约两年时间写成的,记录了这个领域几乎所有的发展历史,里面的图片和结构式全部重新绘制,风格统一非常精美。纸板书再过两周应该就可以见到了,目前可以在googlebooks上预览电子版的部分内容(国内需翻墙:https://books.google.com/books?id=8oY9DQAAQBAJ&pg=PA0#v=onepage&q&f=false)。Stoddart目前发表了超过1100篇论文,但却只写了两部专著,一本是他初出茅庐时撰写自己青年时代和前人对自然的解构,另一本则是三十五载后记录自己和同时代的开拓者们对自然的超越,一眼望去就是一个在人类认知前沿孜孜不倦地耕耘了半个世纪的科学家所记录的两个时代,关于人类挑战未知世界的故事。

2016年出版的详述机械键的专著 参考文献
- PeterR. Ashton, Barbara Odell, Mark V. Reddington, Alexandra M. Z. Slawin, J. FraserStoddart, David J. Williams, Angew. Chem.Int. Ed. Engl. 1988, 27, 1550–1553.
- J.Fraser Stoddart, Chem. Soc. Rev., 2009, 38, 1802-1820
- PierLucio Anelli, Neil Spencer, J. Fraser Stoddart, J. Am. Chem. Soc., 1991, 113, 5131–5133
- IanThomas. Harrison, Shuyen. Harrison, J. Am. Chem. Soc., 1967, 89, 5723–5724
- RichardA. Bissell, Emilio Cordova, Angel E. Kaifer, J. Fraser Stoddart, Nature 1994, 369, 133 – 137
- J.E. Green, J. W. Choi, A. Boukai, Y. Bunimovich, E. Johnston-Halprin, E.DeIonno, Y. Luo, B. A. Sheriff, K. Xu, Y. S. Shin, H. -R. Tseng, J. F. Stoddart, J. R. Heath, Nature 2007, 445, 414-417.
- Chuyang Cheng, Paul R. McGonigal, Severin T. Schneebeli, Hao Li, Nicolaas A. Vermeulen, Chenfeng Ke, J. Fraser Stoddart, Nature Nanotechnology2015, 10, 547–553
听诺奖弟子聊分子机器 | Feringa和他的分子马达与纳米小车
今年获化学奖的三位科学家里,Sauvage应该是在学术界从头干到尾,Stoddart在三十多岁的时候有过一段三年的工业界经历,而Feringa则是PhD毕业就投身工业界,在Shell公司工作了六年,在阿姆斯特丹的研发实验室从事过合成、催化、光化学、生物有机等项目的研发工作,做到了projectleader之后退出了工业界,在格罗林根大学获得教职,开始独立的学术工作。Feringa应该算是一个传统的有机化学家,他发表的论文里有相当一部分是有机合成与催化,包括不对称合成和新的催化方法学等等。他还对生物有机化学有兴趣,可以看出这些研究方向与他早年在工业界的研究内容有很大的重合,而他对光化学的兴趣则造就了人类目前为止能制作的最小的马达,也为他带来了诺贝尔奖的荣誉!
烯烃在光激发下的顺反异构是很早就被科学家们所知道的,Feringa最初应该是想基于此做一些光响应的分子开关。他使用了一些大位阻的烯烃,比如1996年就在Science上报导了用不同手性的圆偏振光来控制一对消旋体状态。和学糖化学起家的Stoddart一样,Feringa也对立体化学有敏锐的直觉,他很快在这个新生的分子开关里引入了更多的立体化学中心来控制分子在不同状态的稳定性。1999年Nature上发表了一篇注定会被载入史册的文章,标题为“Light-drivenmonodirectional molecular rotor”。这篇文章里的分子双键的一端在紫外光照下可以经过两个顺反异构和两个热弛豫过程绕双键相对另一端完成单向360度旋转!虽然文章很谨慎的称其为rotor(转子),但其实现了将光能和热能转化为机械能的特性,是一个大小不到1nm的motor(马达)。
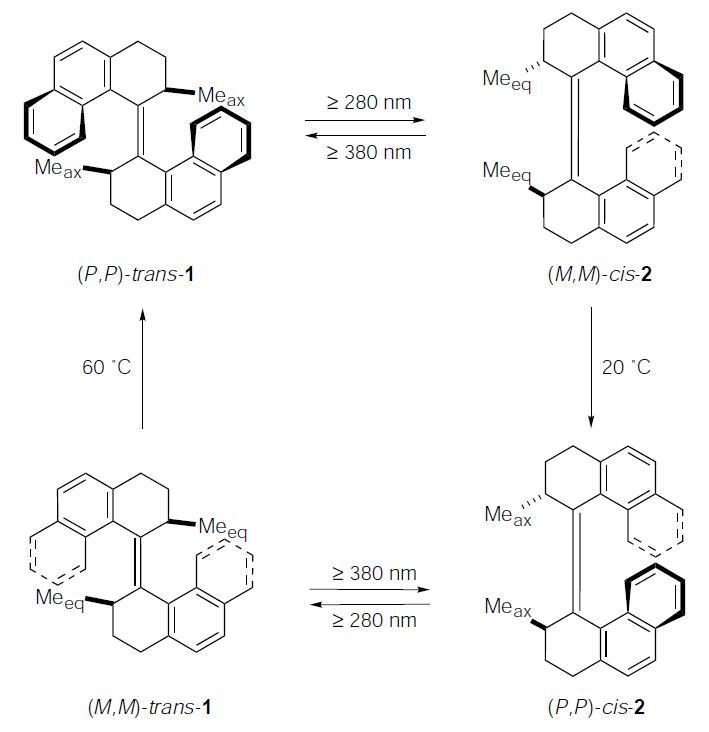
1999年报导的光驱动单向分子马达
该体系的合成并不复杂,双键两端可分别合成,再由偶联反应(如Barton–Kellogg反应)连接成烯烃。得益于易实现的模块化合成,可以很轻易的对分子各个部分的结构进行微调和扩展,Feringa对此分子马达的研究一直持续到今天,做出了许多连续性的突破工作。比如2005年将双键一边固定在金表面,则马达的两部分分别是转子和定子,溶液中的分子马达被固定到了表面上。
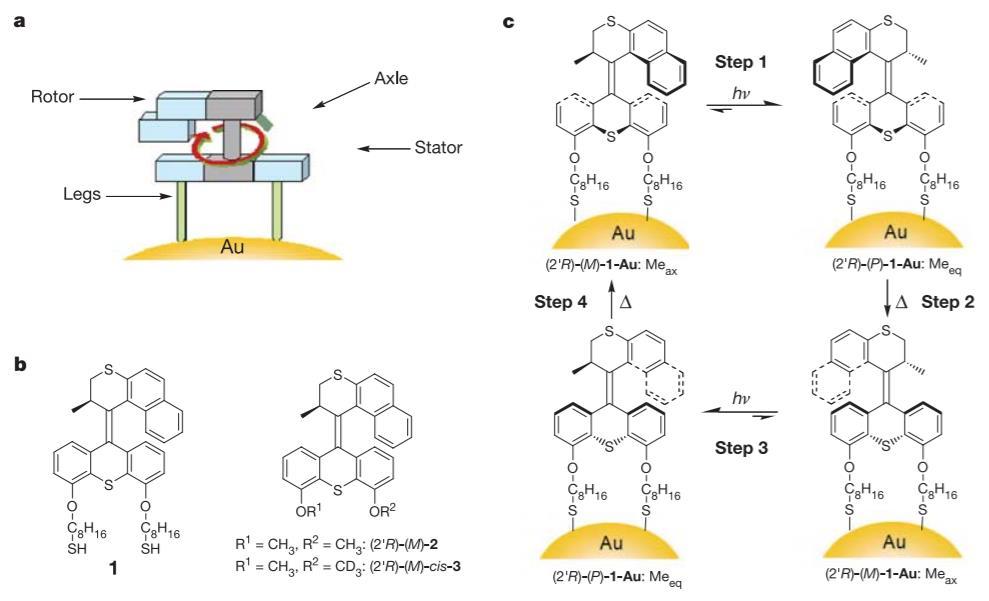
2005年报导的固定在金表面的分子马达
之后又将马达分子参入液晶中,仅1%的马达分子就能带动整个液晶体相分子的转动,同时驱动了一个比分子大数千倍的微米级的玻璃棒的转动,实现了微观分子驱动宏观物体的目标,清晰的展示了分子机器将光能转化为机械能的过程。
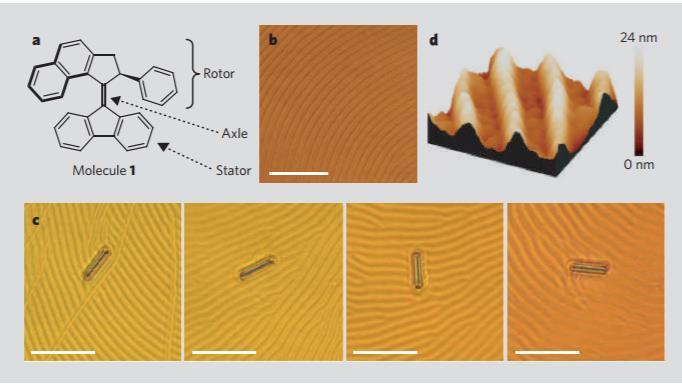
2006年报导的分子马达驱动宏观物体
最有趣的应该是2011年Feringa的小组报到的纳米小车了,他们设计了一个四轮小车模样的有机分子,这个小车的四个轮子是两组对称性不同的分子马达,因此在注入电子的情况下可以向同一方向转动,他们在STM下观测到单分子大致延一个方向运动的现象。而作为对照组的四个轮子对称性相同,于是左右两侧的马达一边向前一边向后,小车只能原地打转。这种将马达和轮子整合的设计思路和现在的电动汽车颇有异曲同工之妙!
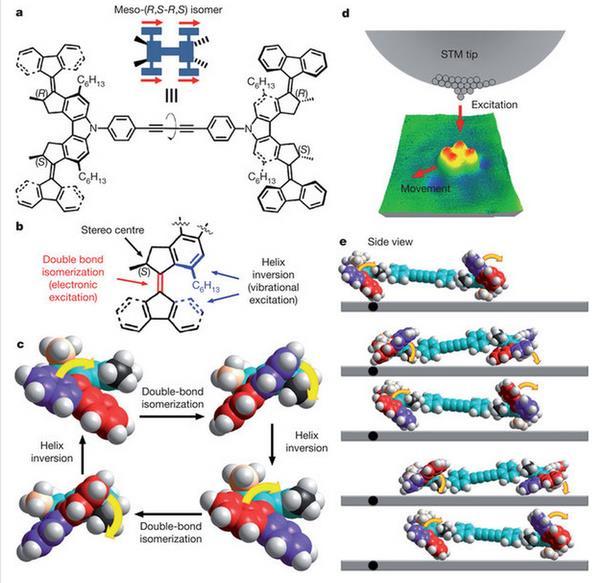
2011年报道的四轮驱动纳米小车
除了作为马达以外,这个大位阻烯烃还可以做分子开关,2011年Feringa设计了一个整合了该分子开关的有机小分子催化剂,通过光照分子开关,控制起催化作用的两个片段的相对位置,实现了同一个分子既能催化不对称反应生成左旋的产物也能生成右旋的产物。
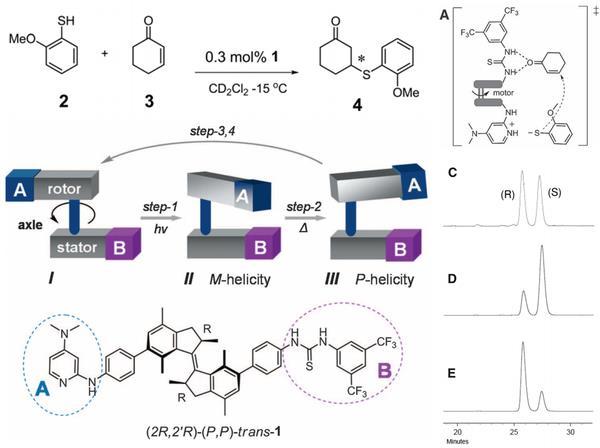
2011年报道的可控制产物构型的有机小分子催化剂
Feringa的这个大位阻烯烃体系发展了二十年,最大的优势就是可以通过分子结构的微调和扩展来实现分子功能和性质的调节,不但能调节马达的转速(周期从数年到数个纳秒),甚至能够反向转动,还可以通过有机合成设计整合进别的体系。Feringa也是今年三位化学诺贝尔奖里最年轻的,我们期待他的分子马达能为分子机器领域做出更多更大的贡献!
参考文献
- Nina P. M. Huck, Wolter F. Jager, Ben de Lange, Ben L. Feringa, Science 1996, 273, 1686-1688.
- Nobuyuki Harada, Nagatoshi Koumura, Ben L.Feringa, J. Am. Chem. Soc.1997, 119, 7256–7264.
- Nagatoshi Koumura, Robert W. J. Zijlstra, Richard A. van Delden, Nobuyuki Harada, Ben L. Feringa, Nature 1999, 401, 152-155.
- Richard A. van Delden, Matthijs K. J. ter Wiel, Michael M. Pollard, Javier Vicario, Nagatoshi Koumura, Ben L. Feringa, Nature 2005, 437, 1337-1340.
- Javier Vicario, Nathalie Katsonis, Blanca SerranoRamon, Cees W. M. Bastiaansen, Dirk J. Broer, Ben L. Feringa, Nature 2006, 440, 163.
- Tibor Kudernac, Nopporn Ruangsupapichat, Manfred Parschau, Beatriz Maciá, Nathalie Katsonis, SyuzannaR. Harutyunyan, Karl-Heinz Ernst, Ben L. Feringa, Nature, 2011, 479, 208-211.
- Jiaobing Wang, Ben L. Feringa, Science 2011, 331, 1429.
听诺奖弟子聊分子机器 | 那些没得诺奖的人和他们的分子机器
今年的诺贝尔化学奖颁给了Sauvage, Stoddart和Feringa以表彰他们在分子机器设计领域的杰出贡献。这三位科学家自然是这个领域的奠基人和开拓者,但同时有许多其他的科学家们和他们一起撑起了这整个领域,这篇专栏文章就来盘点其中的几位。
David Leigh
今年的化学奖颁给分子机器后不少人为David Leigh可惜,因为他也是分子机器领域的一位大师,这次颁奖几乎表示他这辈子再无可能问鼎诺贝尔奖。至于他为什么这次不能拿奖,只能说他晚生了几年。首先,他是Stoddart的博士生,1987年获得博士学位,研究生期间在做大环化学的合成与相关的主客体化学研究。他做了两年博后之后开始了自己的独立教职,从他早期发表的文章来看,90年代他研究过一段时间的C60和超分子化学,90年代中期进入机械互锁分子领域,而他做出的分子机器领域突破性的工作都在2000年以后,而今年获奖的三位科学家的最初突破都在2000年以前,所以从时效性来说他的工作晚于今年的三位获奖者。其次,他的工作同样是基于索烃和轮烷,虽然有他的个人特色,但是前有索烃和轮烷的集大成者Sauvage和Stoddart,所以很遗憾排不到他。但这并不妨碍他成为这个领域的大师,笔者本人也非常喜欢他的工作,这里先介绍几个代表作。
Sauvage在1994年报导了控制索烃中一个环相对另一个环的转动,但是却无法控制环转动的方向,即这个转动方向完全是随机的。Leigh在2003年则首次报导了索烃中的单向转动,虽然所用的方法略显复杂,但确实是个不小的突破。他设计了一个[3]索烃,即两个环套在另一个大环上,大环上有四个不同的结合位点,可以调控它们与两个环的相对结合能力。通过其中一个环挡住另一个环往一个方向的前进路线造成了另一个环单向运动的结果。
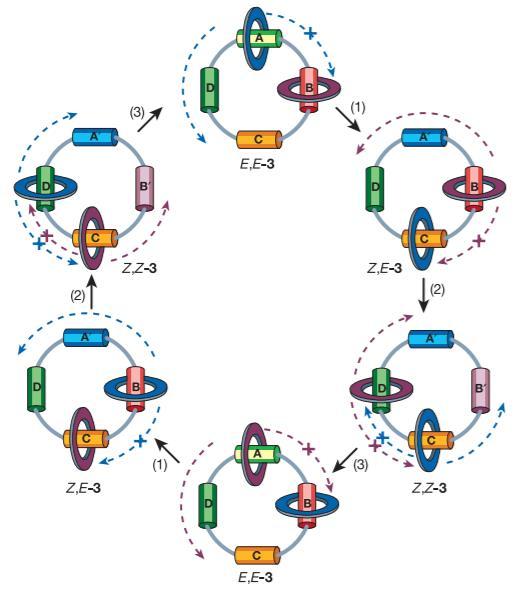
2003年Leigh报导索烃中大环的单向转动
第二年Leigh又报导了另一种策略,即在两个结合位点中间加入两个不同的可控打开和关闭的“大门”,转换结合位点的相对结合能力之后,选择性的打开其中一个“大门”则大环只能从一边转到另一个结合位点上,关上“大门”之后再次切换结合位点的相对结合能力再打开另一个“大门”则完成一次单向旋转。
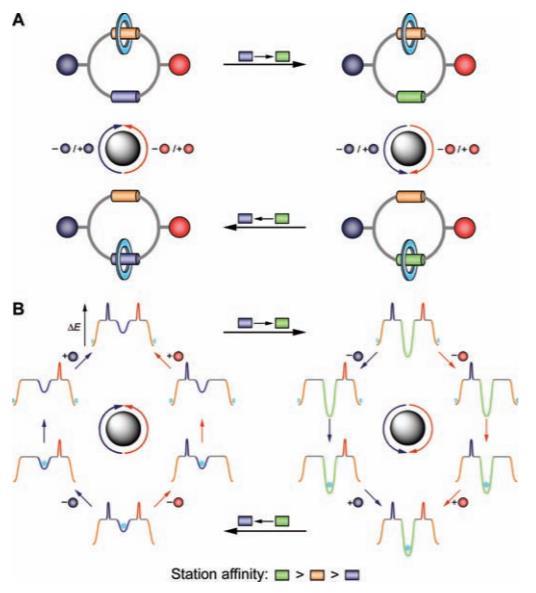
2004年Leigh报导的另一种索烃中的单向旋转策略
Leigh没有满足于这种需要分步加入试剂调控的分子机器,今年他设计了一个索烃,可以在加入“燃料分子”到消耗完全之前让其中的一个环沿着另一个环单向旋转。其中的原理是,在两个等同的结合位点的同一个方向上有一个不停开启关闭的“大门”,开启和关闭消耗溶液中的“燃料分子”。当一个结合位点上有大环的时候,由于位阻效应会减慢大门关上的速度,因此有更多的机会穿过大门,最终统计的结果就是向一个方向旋转的大环多于向另一个方向旋转的大环,实现了自动的单向旋转。
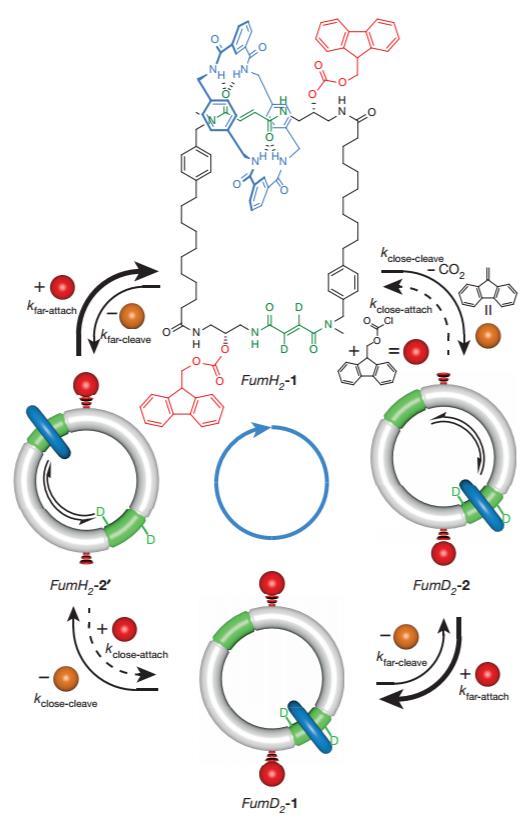
2016年Leigh发表的自动单向旋转的索烃
除了单向旋转的索烃外,Leigh还有许多非常漂亮的分子机器的工作,下一篇专栏还会继续讨论。
James Tour
Feringa把他的分子马达安上小车成功的驱动了纳米小车前进,其实在他之前还有另一个人做了好多个版本的纳米小车,这个人就是JamesTour。与Feringa先花十来年研究马达,再把马达装上车子一次成功不同,Tour走了先研究车架子再往上装马达的研发路线,从三轮车,四轮车,到六轮甚至“纳米火车”,连轮子都研发了三代,有富勒烯,碳硼烷,金属配合物。
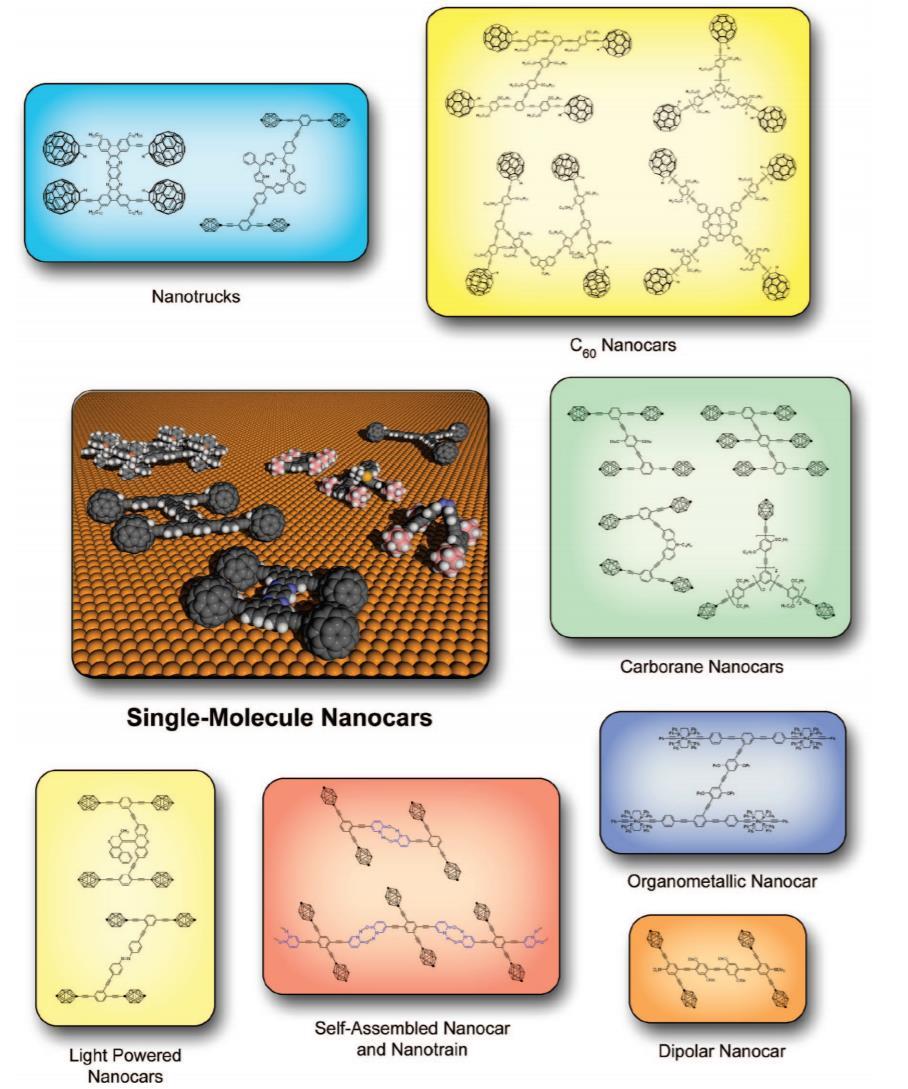
Tour设计的形形色色的纳米小车
最开始Tour的纳米车都是只有轮子没有马达只能在表面靠环境热驱动的无动力车,从轮子的布局大概能限制小车随机扩散的路劲。比如三轮车大多数情况只能原地打转,而四轮车则更倾向于沿着轮轴转动的方向运动。之后Tour尝试给小车加入可控的动力装置,比如在车体中加入偶氮苯基团,希望通过光激发的顺反异构让小车像毛毛虫那样拱行,但并没有相关的表明设计成功的实验报导。
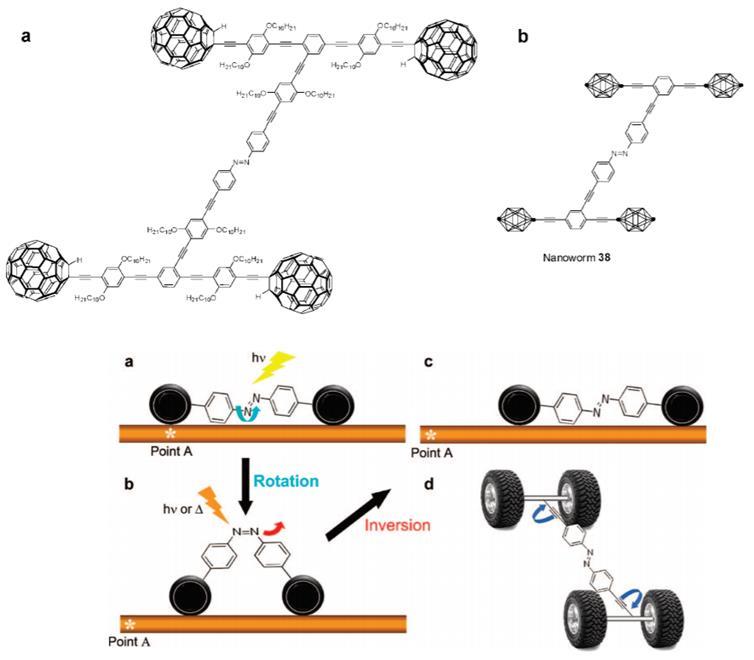
Tour设计的引入光控偶氮苯的纳米小车
Tour也曾尝试过将Feringa的分子马达引入纳米小车的骨架,让马达驱动小车前进,遗憾的是我们同样没能看到相关的驱动成功的实验报导。但是三年后Feringa报导了第一个由分子马达驱动的纳米小车,Tour虽然没有成功,但他的文章为Feringa纳米小车的成功提供了宝贵的经验。也许正是他将马达放在车架中不成功的结果才使得Feringa提出了直接将马达与轮子整合的设计。
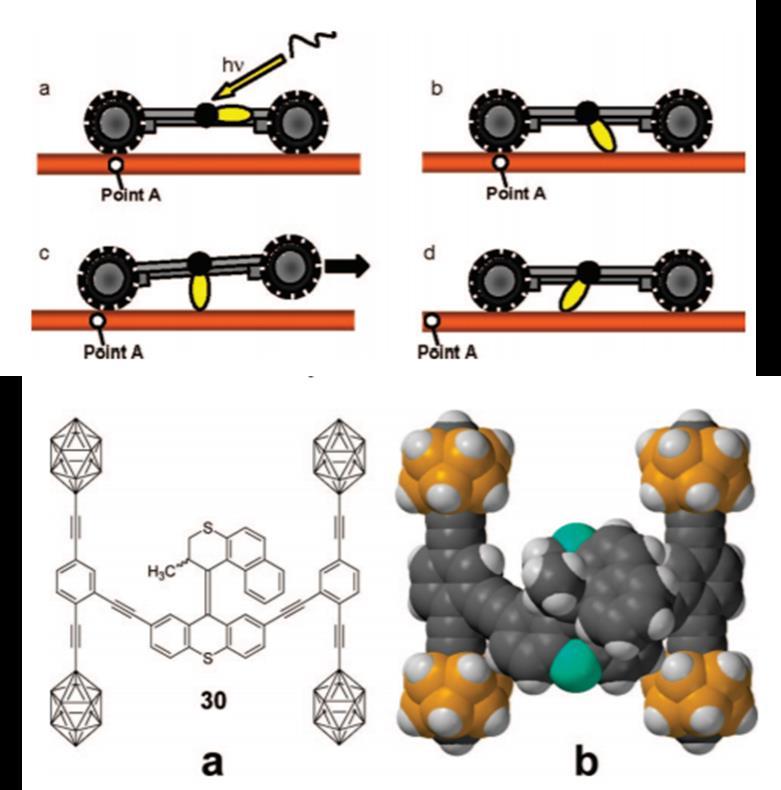
Tour将Feringa的分子马达引入纳米小车设计
虽然在纳米小车的设计上Tour没有成功,但是我们还是很欣慰地看到了之后成功地案例,而且Tour后来的主业是石墨烯碳纳米管等碳纳米材料的研究。
T. Ross Kelly
上一篇专栏提到1999年Nature上发表的Feringa的分子马达注定要载入史册,其实就在这篇文章的前面还有一篇分子马达的文章,两篇文章back-to-back.而相比之下,这篇文章背后的故事显然就略显遗憾了。Kelly和Stoddart生日相差不到一个月,是一名天然产物全合成有机化学家,祖师爷是Woodward,但让他在晚年声名大噪的确是非天然产物的设计与全合成。
1994年Kelly在JACS上发表了一篇叫做分子刹车片的文章。分子中的三蝶烯通过一根单键连接到2,2’-联吡啶上可以随机地自由旋转,当加入金属离子配位固定联吡啶后由于一个吡啶环插入三蝶烯产生位阻使得旋转停止。
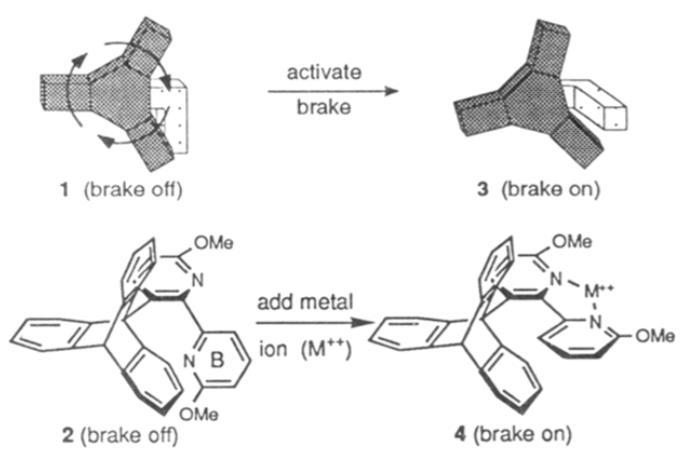
Kelly在1994年报导的分子刹车片
之后Kelly将手性的四螺苯替换了联吡啶,企图用手性构建能量棘轮,诱导三蝶烯单向旋转,在1999年的Nature上发表了初步成果,分子马达的120度单向旋转。三蝶烯的一个叶片上引入氨基,四螺苯末端接有醇羟基,加入燃料光气连接氨基和羟基诱导叶片跨过四螺苯能垒实现120度单向旋转。
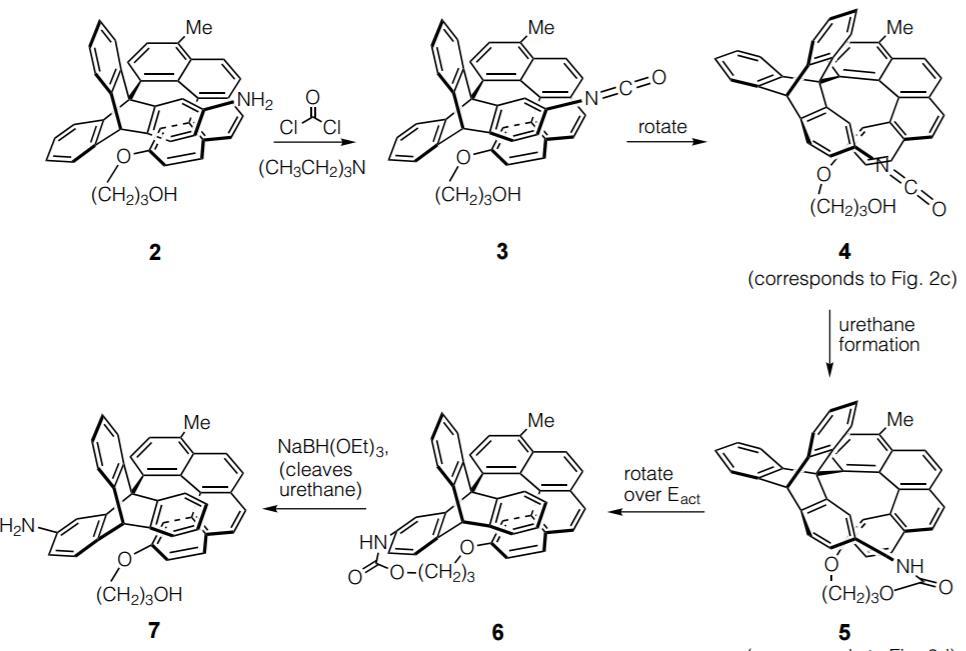
Kelly于1999年发表的120度单向旋转分子马达
这个分子马达设计通过单键旋转,直观上的体会更接近我们所了解的“马达”,可惜之后很长一段时间再也没有关于这个体系的报导。直到八年后的一篇JACS,Kelly才发表了他关于这个分子马达的努力,然而结局却令人不慎惋惜。为了实现360度旋转,Kelly在三蝶烯三个叶片上都引入了氨基,同时在四螺苯上引入了能催化光气与氨基反应的吡啶,希望通过催化剂定向将燃料分子输送到最近的一个氨基上,重复三次即可完成一周的旋转。设计非常精巧大胆,但是事实很无情,Kelly的团队经过各种尝试之后都不work,最终宣布失败告终。
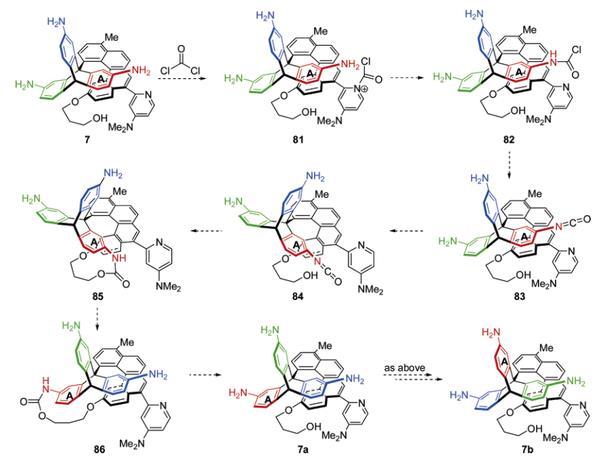
Kelly于2007年发表的不成功的360度旋转尝试
难以想象,这项工作在十来名科研人员的八年的尝试后以失败告终。联系到Kelly的全合成背景,非常善于设计步骤很长的合成路线,但却不能不考虑到分子的合成路线太长,一旦发现不work需要修改结构的时候,时间和人力成本太高,难以进行大量的尝试。Kelly是不幸的,也许成功的那个结构就只需要修改一个碳链的长度,或者一个取代基的位置,但是很遗憾,我们也许永远都不会知道了。但Kelly又是幸运的,虽然在这篇文章之后他便淡出了学术圈,虽然他的分子马达最终没有成功,但毫无疑问他在人类挑战未知的前沿留下了浓墨重彩的一笔,因为有太多失败的科研故事,甚至都没有让世界知道的机会。
参考文献
- David A. Leigh, Jenny K. Y. Wong, Franc¸oisDehez, Francesco Zerbetto, Nature, 2003, 424, 174-179.
- Jose´ V. Herna´ndez, Euan R. Kay, David A. Leigh, Science, 2004, 306, 1532-1537.
- Miriam R. Wilson, Jordi Solà, Armando Carlone,Stephen M. Goldup, Nathalie Lebrasseur, David A. Leigh, Nature, 2016, 534, 235-240.
- Guillaume Vives, James M. Tour, Acc. Chem. Res., 2009, 42, 473–487.
- T. R. Kelly, H. De Silva and R.A. Silva, Nature 1999, 401, 150-152.
- T. Ross Kelly, Michael C. Bowyer, K. VijayaBhaskar, David Bebbington, Albert Garcia, Fengrui Lang, Min H. Kim, Michael P.Jette, J. Am. Chem. Soc., 1994, 116, 3657-3658
- T. Ross Kelly, Jose´ Pe´rez Sestelo, ImanolTellitu, J. Org. Chem. 1998, 63, 3655-3665.
- T. Ross Kelly , Xiaolu Cai , Fehmi Damkaci ,Sreeletha B. Panicker , Bin Tu , Simon M. Bushell , Ivan Cornella , Matthew J.Piggott , Richard Salives , Marta Cavero , Yajun Zhao , Serge Jasmin, J. Am. Chem. Soc., 2007, 129, 376.
听诺奖弟子聊分子机器 | 分子机器的研究现状和未来的挑战
如果从费曼第一次为分子机器的未来画蓝图的1959年开始算起,分子机器的发展已经走过了半个世纪;如果从Sauvage报导金属离子模板合成索烃的1983年算起,分子机器的发展也已经走过了三十多年了。上个世纪90年代以前Sauvage和Stoddart等先驱者在黑暗中摸索,之后的十年先驱者们为可控的分子机器添砖加瓦,Feringa造出了第一台分子马达,而2000年后更多的人参与到分子马达的研发中来。就像乐高积木一样,最开始我们只有最简单的零件,科学家们在前三十年发现了越来越多的可用于拼图的零件,而现在我们在探索更多零件的同时还要想办法将已有的零件组合起来,让分子机器去完成任务,让分子机器来做功。
2013年的时候David Leigh在Science上发表了一个可以按顺序组装氨基酸成多肽的小分子机器,这相当于模拟了核糖体的功能,虽然目前这个体系有诸多限制,比如氨基酸序列是在合成的时候预先设定的很难后期编码,合成的多肽不可能太长,前期的合成投入太大等等。但是我们毕竟在向着用分子机器做功完成任务的方向迈出了重要的一步。
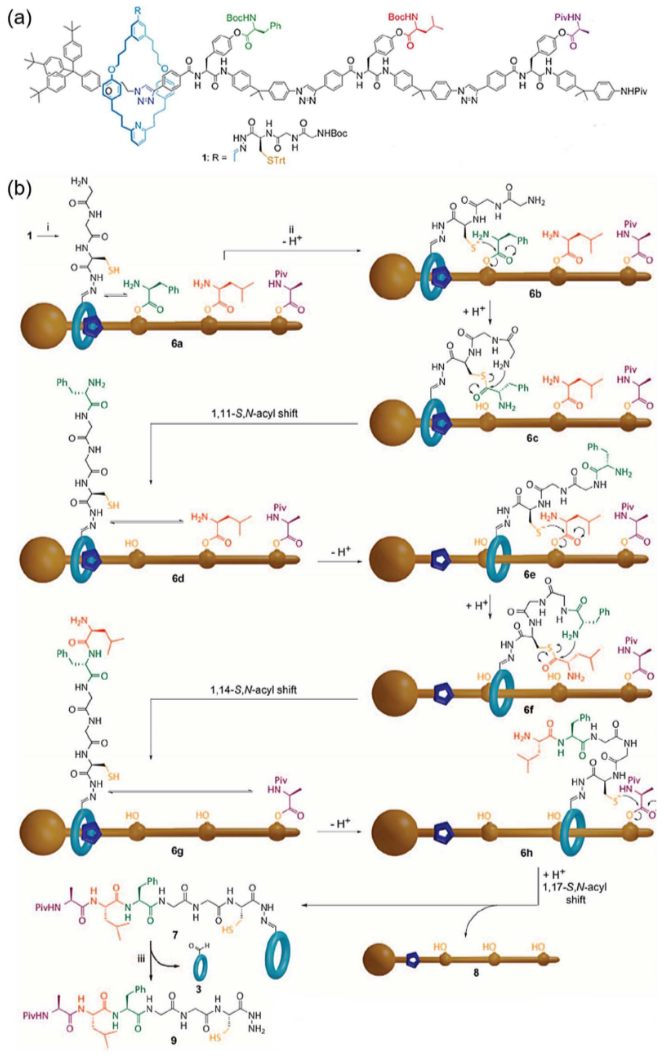
2013年Leigh发表的人工核糖体
Leigh组从2010年起发展了一套“能行走的分子”,即在一个预定的“轨道”上让一小段分子头尾交替地自由移动。最初是随机无方向控制的过程,之后在一端引入热力学低谷,则可以从轨道一端行走到另一端。2016年的时候则更进一步,在分子中引入主动控制的“机械臂”。用酸碱和氧化还原控制机械臂的旋转和抓取与放下货物,可以实现在一边抓起货物,然后在另一边放下货物。也许以后我们可以发展出分子级的流水生产线,可以选择性地合成复杂的分子。
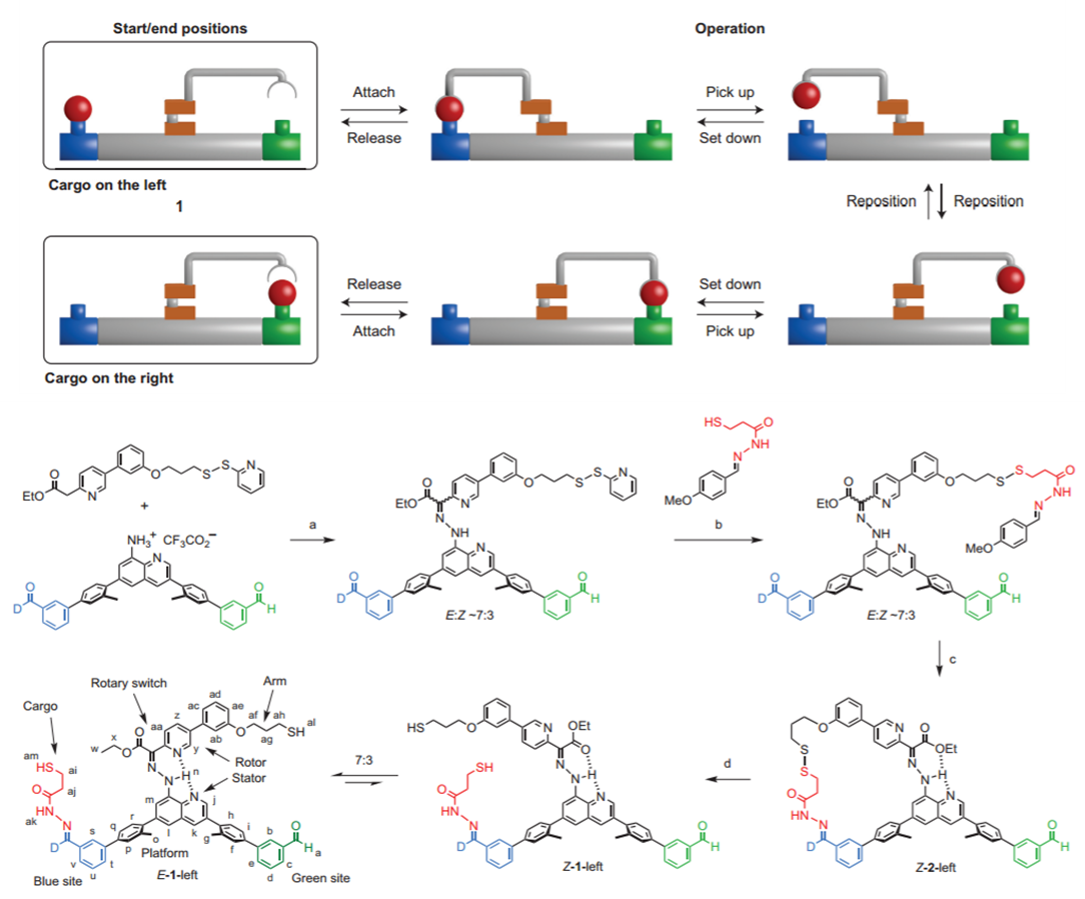
2016年Leigh发表的分子机械臂
如果分别以轮烷和索烃做关键词检索文献可以发现,关于索烃的研究论文数量已经进入平台期,而轮烷仍然在快速增长。其中的原因不但有轮烷更方便合成,性质更可预测外,还有基于轮烷的应用更多。之前的专栏提到用分子机器做催化剂,而轮烷的结构为某一种特殊的催化剂提供了得天独厚的优势——processive catalysis. 自然界的许多催化剂都会形成类似大环或半环的结构依附在DNA或者RNA这样的长链上,一边延长链前进,一边完成催化功能。这样的好处是催化效率高,一个催化剂分子就可以完成一大段长链上需要催化的反应,很适合线性高分子的反应。例如下图是两例基于轮烷的催化剂,一例可以沿着聚丁二烯长链移动并将链中的不饱和键氧化为环氧乙烷结构,另一例则可以催化环戊内酯开环聚合。
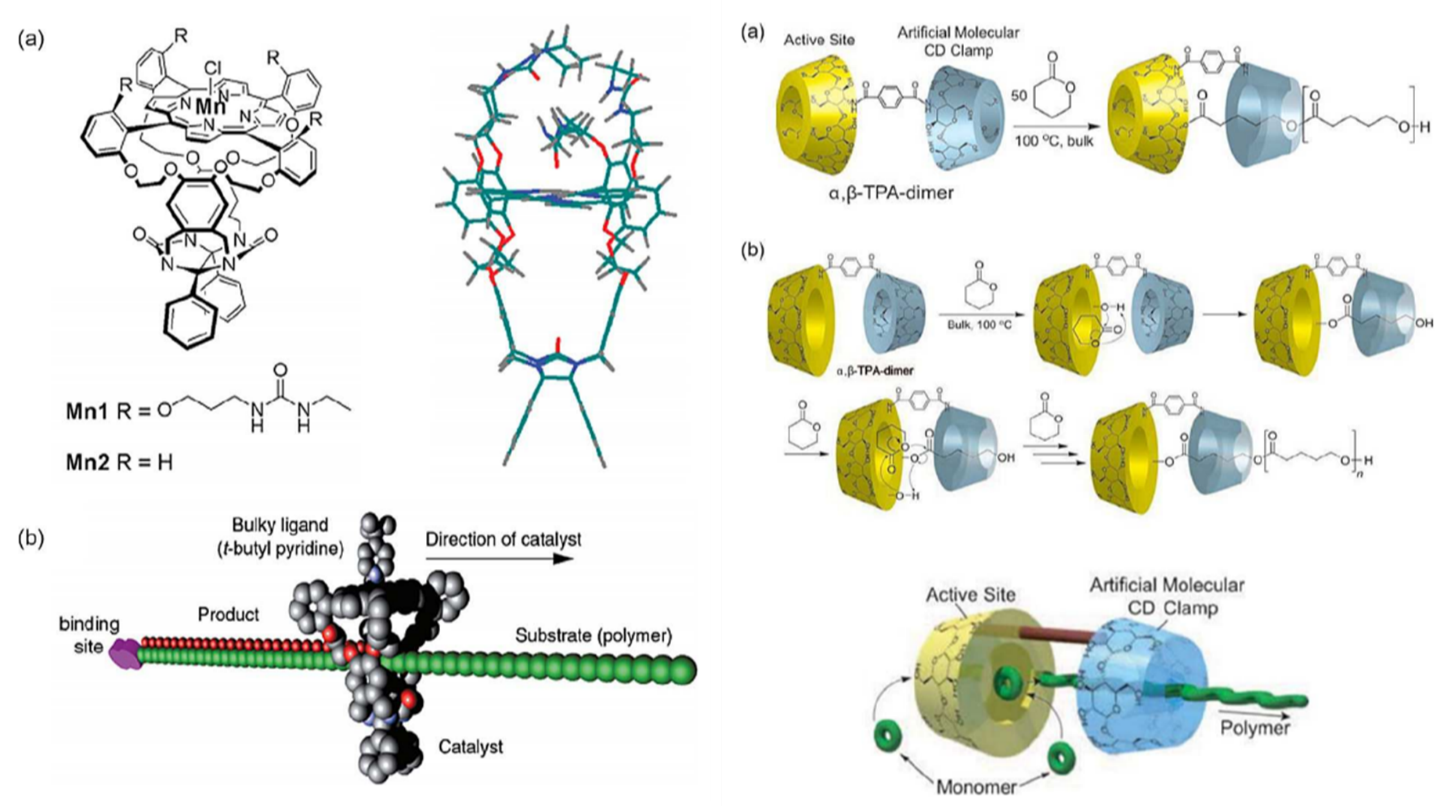
两例基于轮烷结构的催化剂
除了用分子机器完成分子层面的任务外,另一个方向是将分子机器整合到功能材料的设计里,让分子机器从分子层面上来改变或者控制材料的宏观特性。比如Leigh曾经在表面修饰上一个一端含氟代烷的轮烷,通过光照让大环遮住或者暴露这一段氟代烷从而达到改变材料表面亲疏水性使得液滴在光照下爬升。
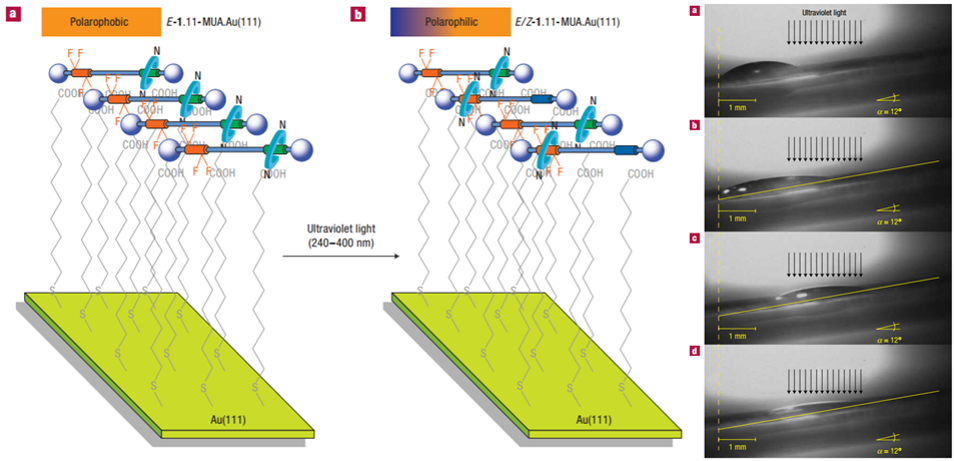
通过轮烷开关改变材料的表面性质
Feringa的分子马达也曾被一个法国的研究小组做到高分子材料中。Giuseppone将分子马达的两边连上高分子链嵌入到交联高分子中,光照下分子马达转动,高分子就像线团一样越绕越紧,导致宏观材料体积不断缩小。
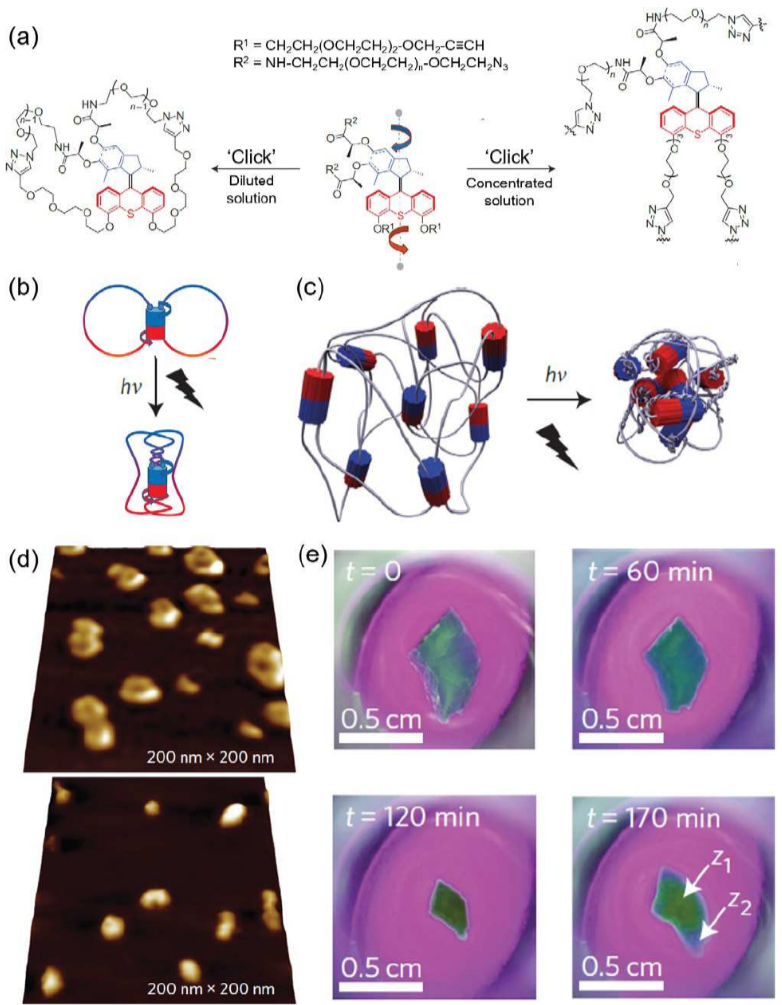
分子马达转动导致材料形变
在未来将会有越来越多的类似的工作出现,将已有的分子机器整合到材料中,让分子机器在微观层面做功改变材料的宏观性质,而需要解决的一个重要问题就是怎样才能让分子机器有序的整合到一起。第一个能做分子肌肉的原型Sauvage在2000年左右就发表了,而Stoddart在2005年将分子肌肉做到了表面上用分子肌肉收缩使得表面产生形变,Giuseppone则在2012年将其整合到高分子链中,又在2016年发表了这种高分子材料的分层自组装,我们期待能在不久的将来看到用这种整合了分子肌肉的高分子材料制成的器件。
此次诺贝尔化学奖颁给了尚无广泛实际应用的分子机器,笔者相信这是在传达一个信息,让人们重视基础研究,正如诺贝尔颁奖委员会所说,分子机器也许开启了人类在一个新的维度的创造力,带给未来无限可能。最后,笔者以David Leigh在颁奖后在发表在Angew上的一篇评论结束此专栏:“这个诺贝尔奖不是颁给治愈癌症(还没有),也不是颁给神奇的材料(还没有),亦不是颁给从太阳富集能量(还没有)。这是一次颁给巨大的科学创造力的诺贝尔奖,这是一次颁给鼓舞人心的科学的诺贝尔奖,这是一次颁给让你梦想“如果”的科学的诺贝尔奖!这是一个关于未来能带来什么并呼吁人们接受挑战的诺贝尔奖!费曼一定会批准的!”
参考文献
- Bartosz Lewandowski, Guillaume De Bo, John W. Ward, Marcus Papmeyer, Sonja Kuschel, María J. Aldegunde, Philipp M. E. Gramlich, Dominik Heckmann, Stephen M. Goldup, Daniel M. D’Souza, Antony E. Fernandes, David A. Leigh, Science, 2013, 339, 189-193.
- Salma Kassem, Alan T. L. Lee, David A. Leigh, Augustinas Markevicius, Jordi Solà, Nature Chemistry, 2016, 8, 138–143.
- van Dongen, Stijn F. M.; Elemans, Johannes A. A. W.; Rowan, Alan E.; Nolte, Roeland J. M. Angewandte Chemie International Edition, 2014, 53, 11420-11428.
- J Berná, D A Leigh, M Lubomska, S M Mendoza, E M Pérez, P Rudolf, G Teobaldi, F Zerbetto, Nature Mater., 2005, 4, 704-710
- Guangyan Du, Emilie Moulin, Nicolas Jouault, Eric Buhler, Nicolas Giuseppone, Angew. Chem. Int. Ed.2012, 51, 12504–12508
- Antoine Goujon, Guangyan Du, Emilie Moulin, Gad Fuks, Mounir Maaloum, Eric Buhler, Nicolas Giuseppone, Angew. Chem. Int .Ed. 2016, 55, 703 –707.
- David A. Leigh, Angew. Chem. Int. Ed. DOI: 10.1002/anie.201609841
原文地址:https://zhuanlan.zhihu.com/p/23496315 |
|
 /3
/3 