登陆有奖并可浏览互动!
您需要 登录 才可以下载或查看,没有账号?立即注册


×
全世界有大约8%的人携带ALDH2基因突变(主要是东亚人群),ALDH2基因突变导至乙醛脱氢酶2的活性大大降低,从而导至酒精的中间代谢产物乙醛的积累,进而导至面部发红等症状,所以携带ALDH2基因突变的人在喝酒或饮用含酒精饮料时,会出现面部发红的症状。因此,喝酒脸红的现象有时也被称为“亚洲红”。除了导至喝酒脸红,之前的研究显示,携带这种基因突变的人患冠状动脉疾病的风险显著上升。
2023年1月25日,斯坦福大学吴庆明(Joseph C. Wu)团队在Science子刊Science Translational Medicine上发表了题为:SGLT2 inhibitor ameliorates endothelial dysfunction associated with the common ALDH2 alcohol flushing variant 的研究论文。 该研究表明,导至喝酒后面部发红的ALDH2基因突变通过诱导内皮细胞功能障碍,从而增加冠状动脉疾病(CAD)风险。更重要的是,该研究还发现了一种已获得FDA批准上市的药物SGLT2抑制剂Empagliflozin(恩格列净,2型糖尿病药物)能够预防和治疗ALDH2基因突变相关内皮细胞功能障碍。
ALDH2基因与冠状动脉疾病的关系 冠状动脉疾病(CAD)是全球死亡的主要原因,每年约900万人死亡,且CAD的全球患病率正在上升。CAD是一种由多种遗传和环境因素相互作用引起的复杂疾病。通过全基因组关联研究(GWAS),已有数百个基因组位点与CAD相关。乙醛脱氢酶2 (ALDH2)基因中的单核苷酸多态性(SNP) ALDH2*2,也称为rs671,与正常的ALDH2*1等位基因相比,导至谷氨酸在504位取代赖氨酸(E504K),从而改变了底物对ALDH2催化活性位点的访问。ALDH2是酒精代谢第二步中的关键酶。它在解毒有毒的醛,如氧化应激衍生的醛和酒精衍生的乙醛中至关重要。ALDH2*2携带者降低了ALDH2酶活性,这种缺乏与各种神经、心血管和皮肤疾病有关;药物代谢异常。最近一项对12项病例-对照研究(3305例病例和5016例对照)的荟萃分析显示,ALDH2*2与CAD风险增加48%相关。 然而,迄今为止,ALDH2*2与CAD发病之间的潜在机制仍不清楚,这为预防和治疗ALDH2*2相关的CAD创造了障碍。此外,饮酒是冠心病的一个众所周知的危险因素。尽管在非亚洲人的研究中,乙醇不是导至CAD的主要因素,但它可能对亚洲血统的ALDH2*2携带者有重大影响。因此,确定ALDH2*2和饮酒对CAD的联合影响,以制定预防策略,降低ALDH2*2携带者的CAD风险是很重要的。 文献主要内容 内皮细胞(ECs)是血管壁的重要组成部分,通过调节血管张力和结构在维持心血管稳态中发挥重要作用。EC功能障碍涉及多种人类心血管疾病。冠状动脉EC功能障碍发生在CAD发展的早期,可影响疾病的所有阶段,从发病到动脉粥样硬化性血栓并发症。ALDH2*2通过核因子κB (nuclear factor κB,NF-κB)、c-Jun和丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)通路增加炎症与EC功能障碍相关;通过二甲基精氨酸二甲胺水解酶-1 (dimethylarginine dimethylaminohydrolase-1,DDAH1)和不对称二甲基精氨酸(asymmetric dimethylarginine,ADMA)途径减少一氧化氮(NO)的产生,以及通过活性氧(ROS)和有毒醛如4-羟基壬烯醛(4-hydroxynonenal,4-HNE)增加氧化损伤。然而,ALDH2*2引起EC功能障碍的具体机制尚不清楚。 在这项研究中,研究人员利用内皮功能的临床评估显示,携带ALDH2*2的人类参与者在轻度饮酒后表现出血管舒张受损。利用人诱导的多能干细胞来源的ECs (induced pluripotent stem cell–derived ECs, iPSC-ECs)和CRISPR-Cas9校正的ALDH2*2 iPSC-ECs,研究在体外模拟了ALDH2*2诱导的EC功能障碍,结果显示氧化应激和炎症标志物增加,一氧化氮(nitric oxide,NO)产生和管形成能力下降,乙醇暴露进一步加剧了这一情况。随后发现钠-葡萄糖共转运蛋白2抑制剂(sodium-glucose cotransporter 2 inhibitors, SGLT2i),如empagliflozin缓解了ALDH2*2相关的EC功能障碍。 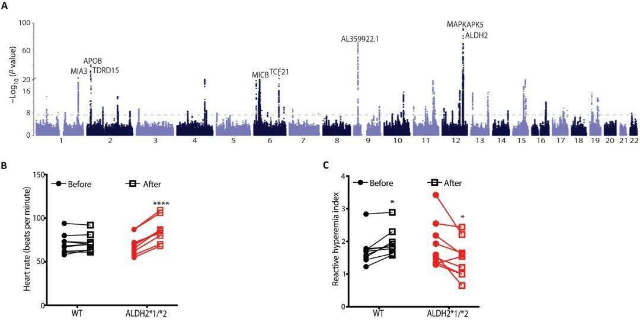 图1. ALDH2*2与冠状动脉疾病(CAD)密切相关,并诱导内皮功能障碍(图源自 Science Translational Medicine ) 通过对ALDH2*2敲入小鼠的研究进一步证明,empagliflozin可在体内减弱ALDH2*2介导的血管功能障碍。在机制上,empagliflozin抑制Na+/H+-交换器1 (Na+/H+-exchanger 1, NHE-1),激活AKT激酶和内皮NO合成酶(endothelial NO synthase, eNOS)通路,改善ALDH2*2诱导的EC功能障碍。 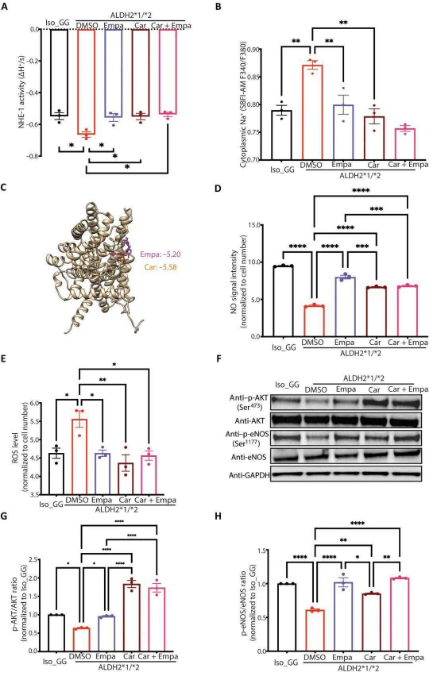 图2. Empagliflozin通过NHE-1/AKT/eNOS通路改善ALDH2*2相关内皮功能障碍(图源自 Science Translational Medicine ) 总体而言,这项研究发现即使少量饮酒也会损害ALDH2*2等位基因人类参与者的内皮功能。Empagliflozin通过抑制NHE-1活性和恢复AKT和eNOS信号,在体外和小鼠实验中改善了这种功能障碍。鉴于内皮在血管功能中的重要作用,这些结果表明,靶向ALDH2*2活性及其下游效应可能是限制ALDH2*2携带者血管疾病的有效策略。
|
 /3
/3 