登陆有奖并可浏览互动!
您需要 登录 才可以下载或查看,没有账号?立即注册


×
作者简介
奚苏静 《中国体外诊断产业发展蓝皮书》编委 海肽生物科技(上海)有限公司总经理 HyTest 全球战略发展团队成员
浙江大学,上海交通大学工商管理硕士 专注上游原料领域服务诊断产业十余载。
2011年开始筹办HyTest 中国全资子公司,经过数年的悉心经营,海肽生物已经成长为国内免疫诊断原料的领先企业之一。
1引言
体外诊断产品的质量很大程度上是由上游的核心原材料决定的。
广义的原材料包括仪器上游的核心元部件和试剂上游的生物活性/非生物活性材料。狭义的诊断试剂原料一般仅指生化、免疫或分子诊断试剂的反应体系原料,包括核心反应体系、信号体系、载体,以及反应环境等。其中,核心反应体系原料如诊断酶、引物、抗原、抗体等,是体外诊断试剂产业上游最重要的战略节点,其质量是决定体外诊断试剂质量的最重要因素。信号体系如胶体金、酶底物系统、发光物质等是将不可见的生物反应过程和结果变成可视、可读的结果的实现环节。反应体系载体如NC膜、酶标板、磁珠等提供了生物化学反应发生的场所,并因各种材料的迥异性能,使得诊断试剂具有快速、高通量、均相等丰富特性。反应环境是由各种生物活性材料和精细化学原料,包括牛血清白蛋白、阻断剂、氯化钠、碳酸钠和各种氨基酸以及有机酸等调配而成的体外诊断试剂缓冲溶液,为试剂的反应排除干扰、为储存提供了稳定性,保障反应得以顺利进行。
本章重点讨论核心反应体系原料、信号体系、载体,以及阻断剂等。有机无机化学原料对诊断试剂品质也有不可忽略的影响,但因原料本身的质量控制和判断相对简单,本章不展开。
2诊断试剂原料的国际发展状况
原料的重要性使得有能力为体外诊断工业提供创新、优质、稳定、大批量的原料的公司异军突起,越来越受到体外诊断试剂厂商的重视和青睐。不同于科研试剂供应商动辄数十万产品的“大而全”,体外诊断试剂原料供应商往往“小而美”,这是行业特点决定的。首先,“原料”概念跨度较大,抗原抗体、酶底物、膜材微粒等,涉及完全不同的领域,原料供应商穷究几十年也往往只精通其中一个领域,比如HyTest主攻单抗,MBC和IIC专做多抗,Genzyme以酶为业,Millipore因膜闻名……。其次,目前被批准使用于临床检验的项目不过千余种(《医疗机构临床检验项目目录2013版》收录检验项目约1500个),从原料角度进行方法学归类,则无非化学反应、酶底物反应、抗原抗体反应、PCR反应等数种原理,因而,原料公司的产品数量都相对有限,以国内产品种类数量最多、涉足领域最广的体外诊断核心原料供应商菲鹏为例,2016年财报显示经数十年的技术革新和发展,目前已拥有700余小类的抗原抗体产品——比起科研抗体供应商,这十数年积累的产品数量可说是精选严选的产物。再次,体外诊断涉及的疾病范围广泛,传染病、肿瘤、心血管、代谢等每一类疾病都代表独立的学科,作为抗原抗体原料供应商,只有对该疾病和疾病标志物进行长期、专注的研究,才能研发优质的原料应用于疾病诊断,这进一步使得免疫原料的源头供应商通常仅专精于少数几个疾病领域,如HyTest拥有毋庸置疑的心血管原料第一品牌定位,BioVentix以Vit D闻达于业界,而Microbix则凭ToRCH抗原独树一帜。
当然,随着频繁的并购活动,原料供应商中也不乏“巨无霸”的身影,如Merck,BBI,ThermoFisher,Meridian等,产品线横跨多个领域,为体外诊断工业提供更为完善的解决方案;还有一些公司,如Fitzgerald,Abcam等,拥有超长产品线,他们既服务于工业客户,也服务于科研客户。
2009-2016年国内体外诊断市场规模的复合增速为16.60%,预计2016年达到370亿元。如果按照诊断试剂原料市场规模约占体外诊断试剂市场规模10%左右计算,我国诊断试剂原料市场规模约37亿元。
高速增长的中国体外诊断市场受到国际原料厂商的高度重视,Merck、Roche、东洋纺、HyTest等较早在国内设立子公司,专为中国市场服务;2016年新进入或正在设立中国子公司的有Medix、Meridian、BBI等。其他未进入中国的原料企业,其产品在国内也均可通过代理商如佰桥瑞景和雅为世纪较方便地获得。而国内的明星原料企业如菲鹏生物,2016年在新三板上市,年销售额超过1.5亿元人民币,已然跻身国际品牌行列,共同为中国体外诊断试剂工业服务。
可以这么说,中国体外诊断工业,在核心原料这一环节,正与世界同步。
3诊断试剂原料
1 核心反应体系(抗原、抗体、酶)
1. 抗原抗体 抗原抗体广泛应用于以免疫反应为基本原理的诊断试剂中。抗原抗体反应具有可逆性、最适比例、特异性和敏感性等特点。
(1)可逆性:抗原与抗体结合形成抗原抗体复合物的过程是一种动态平衡,抗原抗体复合物的解离程度与抗体的亲和力K值有关。高亲和力抗体的抗原结合点与抗原的决定簇在空间构型上非常适合,两者结合牢固,不易解离。
(2)最适比例:在恒定量的抗体中加入递增量的抗原形成免疫复合物(沉淀)的量见图4.9-1。曲线的高峰部分是抗原抗体比例最合适的范围,称为等价带(zone of equivalence)。在等价带前后分别为抗体过剩带和抗原过剩带。如果抗原或抗体极度过剩,则无沉淀物形成,在免疫测定中称为带现象(zone phenomenon)。抗体过量称为前带(prezone),抗原过量称为后带(postzone)。在用免疫学方法测定抗原时,应使反应系统中有足够的抗体量,否则测得的量会小于实际含量,甚至出现假阴性。
(3)特异性:抗原抗体的结合实质上只发生在抗原的抗原决定簇与抗体的抗原结合位点之间。由于两者在化学结构和空间构型上呈互补关系,所以抗原抗体反应具有高度的特异性。例如乙肝病毒中的表面抗原(HBsAg)、e抗原(HBeAg)和核心抗体(HBcAg),虽来源于同一病毒,但仅与其相应的抗体结合,而不与另外两种抗体反应。抗原抗体反应的这种特异性使免疫测定能在非常复杂的蛋白质化合物(例如血清)中测定某一特定的物质,而不需先分离待检物。
但是这种特异性也不是绝对的。假使两种化合物有着部分相同的结构,在抗原抗体反应中可出现交叉反应。例如:绒毛膜促性腺激素(hCG)和黄体生成激素(LH)均由α和β两个亚单位组成,其结构的不同处在β亚单位,而两者的α亚单位是同类的。用hCG免疫动物所得的抗血清中含有抗α-hCG和抗β-hCG两种抗体,抗α-hCG抗体将与LH中的α酶位发生交叉反应。在临床检验中,如用抗hCG抗血清作为妊娠诊断试剂检定尿液中hCG,只能用于hCG浓度较高的试验,否则妇女生理性排泄入尿液中的微量LH将与之发生交叉反应。因此在作为早孕诊断的试剂中必须应用只对hCG特异的抗β-hCG,以避免与其它激素的交叉反应的发生。
(4)敏感性:在测定血清中某一物质的含量时,化学比色法的敏感度为mg/ml水平,酶反应测定法的敏感度约为5~10μg/ml,免疫测定中凝胶扩散法和浊度法的敏感度与酶反应法相仿。标记的免疫测定的敏感度可提高数千倍,达ng/ml甚至pg/ml水平。
因此,抗原抗体反应中原料的灵敏度、特异性、效价和亲和力是决定试剂盒性能的关键因素,也是试剂生产商对原料性能考核的重点参数。
抗体,也叫免疫球蛋白(immunoglobulin),是一种能特异性结合抗原的糖蛋白,而抗原则是在易感染动物体内引发抗体产生的物质。抗体的结构如图4.9-2所示,一个抗体分子上的两个抗原结合部位是相同的,位于两臂末端称抗原结合片段(antigen-binding fragment,Fab)。“Y”的柄部称结晶片段(crystalline fragment,FC),糖结合在FC上。另外,FC片段具有抗原性,可被其他抗体或抗体片段所识别。 根据“Y”形结构的数量和重链种类的不同,哺乳动物体内的抗体可以分为5类:IgG、IgM、IgA、IgD、IgE。其中IgM是5聚体,而IgA有二聚体三聚体等多种形式。各类抗体在生物学特性、功能区域以及结合不同抗原的能力上有所不同,这里不再赘述。值得一提的是目前在免疫学检测试剂开发中,主要使用的抗体为IgG,IgM次之。
关于抗体的应用,早在几百年前便有记载。公元16世纪我国已有关于种痘预防天花的记载;18世纪后叶,英国人Jenner也通过接种牛痘预防天花。而随着疫苗的应用,抗体的靶向作用也被应用到了更多领域。1890年,白喉毒素的发现,开创了抗体制药领域;1975年,来源于小鼠B淋巴杂交瘤细胞的第一代单克隆抗体诞生,使得抗体作为疾病诊断和治疗的应用范围有了更大范围的扩展。
随着抗体在疾病诊断方面的应用发展,目前主要应用的抗体以鼠、羊和兔子等动物来源的单克隆抗体和多克隆抗体为主。关于单抗和多抗,其定义如下:抗原上可以引起机体产生抗体的分子结构叫做抗原决定簇,也称为抗原表位。一个抗原可以有许多不同的抗原决定簇,因此,机体也可以产生多种不同的抗体。由单一B淋巴细胞克隆产生的高度均一、仅识别某一特定抗原表位的抗体,称为单克隆抗体。而由多个B淋巴细胞克隆产生的、受到多种抗原决定簇刺激并可以与多种抗原表位结合的抗体就是多克隆抗体。从某种角度而言,多抗是多种单抗的混合物。
除了定义不同之外,两者在制备上也有区别。经过特定抗原处理过的B淋巴细胞与骨髓瘤细胞通过细胞融合的方法得到杂交瘤细胞,经HAT培养基筛选、ELISA检测效价后就可得到阳性克隆株,最后进行细胞培养或将细胞注入到动物(一般为balb/c小鼠)腹腔中用腹水培养,收集上清/腹水纯化后就能得到单克隆抗体。而制备多克隆抗体工艺相比于单克隆抗体则简单许多,只需将抗原(纯度越高越好)直接注入到动物体内进行免疫,经过3~4次免疫,ELISA测其效价合格后,收集血液离心得到上清,纯化后即能得到多克隆抗体。因此制备多克隆抗体的周期相比单克隆抗体要短,而且首次制备价格也比单抗要低。
在应用方面,单抗和多抗都有各自鲜明的特点与优势。单克隆抗体的特异性高,一旦制备成功就可以永续的生产完全一致的抗体,因此可以对其特异性进行全面、系统地验证。但如果所识别的抗原表位被破坏,实验的结果将会受到很大的影响,这也是单抗的缺点之一。而多克隆抗体的特异性较差,即使是使用相同的抗原制备多抗,不同批次间也会存在差异,因而在特异性、一致性方面有很大的局限。所以在用多抗做免疫检测时,更容易造成本底过高的现象。虽然多抗存在交叉反应的问题,但由于多抗识别多个抗原表位,即使是有少数几个抗原表位被破坏或者抗原构象改变,实验的结果也不会受到影响。因此在相同条件下,使用多抗可以提高检测的灵敏度,对于丰度偏低的蛋白也更容易检出。
除了完整的抗体蛋白之外,抗体的功能性片段也被广泛应用于疾病检测领域。抗体的功能性片段是指经过特定的蛋白酶酶切之后获得的功能性片段。抗体FC段由于具有抗原性,可被其他抗体所识别,如小鼠单克隆抗体可被类风湿因子、HAMA等异嗜性抗体所识别,从而影响检测结果。因此目前在体外诊断领域中去除抗体FC段的主要目的是去除异嗜性抗体引起的非特异性反应。常用的功能性片段有Fab(由木瓜蛋白酶酶切而得)和F(ab’)2(由胃蛋白酶酶切而得)。
由于动物源性的抗体在疾病诊断应用中往往会受到不同种异嗜性抗体的影响,因此在未来,嵌合抗体(人源化)、基因工程重组抗体将会成为抗体发展的主要趋势。嵌合抗体是将不同物种的抗体片段进行组合后获得的改造抗体,如将小鼠抗体的FC片段替换为人抗体FC片段,这样便可以免除HAMA的影响。重组抗体是通过经免疫淋巴细胞而提取的抗体轻链和重链基因片段(mRNA),经逆转录后导入基因工程载体,然后进行体外表达。该方法获得的抗体,在产量、生产周期和多样性等方面相比于传统的杂交瘤方法均有明显优势。此外,该方法还可以跳过免疫系统,在不经过免疫动物的情况下直接获得特定的抗体。关于单克隆抗体,多克隆抗体和重组抗体的对比如下表。
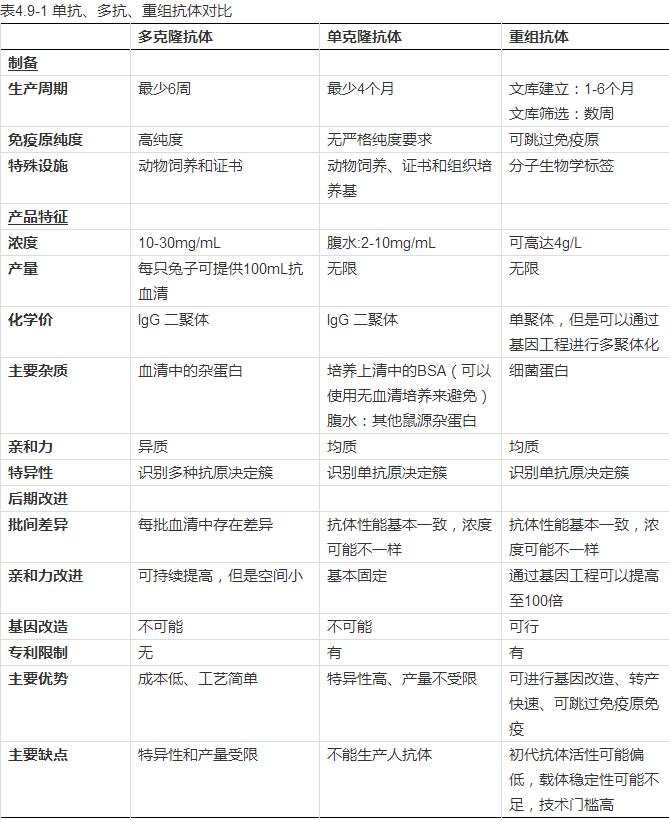
在疾病诊断领域,抗体是体外诊断试剂的核心原料。根据技术平台和检测方法的不同,应用也略有不同。目前主要的应用平台有放射免疫分析、酶联免疫分析、化学发光免疫分析、胶体金侧向层析、荧光免疫侧向层析、免疫比浊、蛋白免疫印迹、免疫组化和直接酶联免疫分析等。在不同平台中,抗体通过修饰偶联于不同的标记物和固相介质。其中,抗体与标记物组成的偶联物称为检测系统(产生信号),而抗体与固相介质的偶联物则称为分离系统。这两个系统最终形成了完整的体外诊断免疫学试剂。关于标记物,目前常用的有放射性同位素标记、酶标记(辣根过氧化物酶和碱性磷酸酶等)、直接荧光标记、时间分辨荧光标记、直接化学发光(吖啶酯)、生物发光标记、电化学发光标记、磷光标记、微球标记、链霉亲和素-生物素标记等。关于固相介质,目前主要应用的有聚苯乙烯微孔板、玻璃/聚苯乙烯乳胶微球、磁微粒、硝酸纤维膜等。
关于偶联的方法,主要有静电吸附、生物偶联(链霉亲和素-生物素、二抗、ProteinA/G等)和化学偶联。在主要的三种偶联方法中,最重要的是化学偶联。主要原理是通过将抗体分子中的活性基团与偶联物的活性功能基团通过化学反应进行交联,因此制备工艺和反应途径会对抗体活性乃至整个试剂的性能产生重要的影响。目前应用的主要活性基团有氨基、巯基、羧基和糖基等。针对于蛋白质,主要的交联反应有过碘酸钠法、同型双功能交联剂法、异型双功能交联剂法等。而针对于半抗原等小分子,主要交联方法有碳二亚胺法、碳二亚胺-NHS法、混合酸酐法和曼尼希反应等。关于不同交联方法的具体反应原理,可参考相关书籍,这里不再赘述。
在不同的检测方法中,抗体起到了多种关键的功能作用。目前常用的检测方法有双抗体夹心法、双抗原夹心法、间接法、抗体竞争法、抗原竞争法和捕获法等。在双抗体夹心法中,待测物为抗原(蛋白质和多肽为主),捕获抗体和检测抗体分别与固相介质和标记物偶联,通过与抗原形成三明治免疫复合物从而实现对抗原的检测;在双抗原夹心法中,待测物为抗体,因此抗体在试剂盒中扮演的角色为校准品或质控品,不同抗原分别与固相介质和标记物偶联,通过与待测抗体形成三明治免疫复合物从而实现对抗体的检测;在间接法中,待测物为抗体,抗原与固相介质进行偶联对待测抗体进行捕获,抗人IgG特异性抗体作为检测抗体;在抗原竞争法中,待测物为抗原(通常是小分子抗原,主要原因在于小分子上至多只有一个抗原决定簇,因此不能形成夹心复合物),捕获抗体与固相介质偶联,抗原和待测抗原竞争性地被捕获抗体捕获,从而实现对抗原的检测;在抗体竞争法中,待测物为抗体,抗原与固相介质偶联,抗体与标记物偶联,与待测抗体竞争性地与捕获抗原反应,从而实现对抗体的检测,同时,抗体还可作为校准品和质控品;在捕获法中,待测物为IgM抗体,抗IgM抗体作为捕获抗体与固相介质偶联,IgM对应的抗原的特异性抗体作为检测抗体与标记物偶联,通过形成抗IgM抗体-IgM-IgM抗原-抗IgM抗原特异性抗体的复合物对待测IgM进行检测。除上述的经典免疫学检测方法外,免疫比浊法也是目前体外诊断行业中应用非常广泛的方法。该方法中,抗体与胶乳微球进行偶联,当待测物中有抗原存在时,会引起胶乳溶液的浊度变化,从而实现对抗原的检测。关于不同检测方法的详细原理,这里不再赘述,可参考其他相关书籍。
除上述的常见方法外,蛋白免疫印迹、免疫组化和直接酶联免疫分析在科研领域应用广泛,在体外诊断领域也有一定程度的应用。其中抗体作为检测抗体可直接与待测抗原反应。
如前所述,作为主要的核心原材料,抗体对于整个免疫检测分析系统有着至关重要的影响。因此除去试剂制备工艺外,抗体自身的性能可在很大程度上决定着检测试剂的质量。目前,衡量抗体质量的技术指标仍然没有统一标准,但是可以大概总结为活性/效价/亲和力、线性范围、特异性、纯度、重复性/批间差和稳定性等。
活性/效价/亲和力,是反应抗体与抗原之间反应性的直接指标,但是目前关于该指标的测定没有标准和统一方法。现阶段,大多数抗体供应商对于效价的检测是在ELISA平台上通过重组或者天然抗原对抗体进行测试,通过信号值对抗体的活性进行考察。检测方法以直接ELISA为主,即抗原包被于聚苯乙烯微孔板后,用标记的抗体直接与抗原进行反应。这里值得注意的是,并不是高亲和力的抗体就一定对应为高性能的免疫检测分析系统。针对不同种类的标志物,对于亲和力的要求有一定区别,具体讨论将在线性指标中详细展开讨论。
线性范围是指分析方法在给定范围内获取与样品中待测物浓度成正比的试验结果的能力。该指标是反映分析方法检测范围和准确性的直接指标。线性范围的测试是在抗体配对组成基本的免疫检测分析系统后进行的,因此可以理解为是抗体性能的间接指标。正如前文所述,高亲和力抗体并不代表高性能试剂,针对不同种类的标志物,对于亲和力的需求有一定差异。当待测标志物在外周循环中存在的浓度范围很宽时,如果使用了高亲和力的抗体,那么会导至钩状效应的过早出现(钩状效应或HOOK效应,是指由于抗原抗体比例不合适而导至假阴性的现象,产生的主要原因是当抗体亲和力很强,同时抗原浓度很高时,可用抗体全部被抗原中和,导至了反应提前进入平台期甚至信号下降。),从而严重影响到了试剂盒的线性范围,导至了高浓度样本被严重低估,甚至可能导至医疗事故的产生。典型的宽浓度范围的标志物,如人绒毛膜促性腺激素(hCG)、肌红蛋白(MYO)和C反应蛋白(CRP)等。但是对于微量存在即可提示某种疾病的且浓度范围并不是很宽的标志物而言,高亲和力的抗体便显得尤为重要,因为低值样本的检出能力或称为灵敏度直接与抗体亲和力挂钩。典型的低浓度具有重要意义的标志物,如肌钙蛋白(TnI,目前市场上已经有超敏肌钙蛋白检测试剂了)和降钙素原(PCT)等,均对试剂灵敏度有很高要求。
特异性指抗体单一性识别某种特定抗原的能力。该指标虽然不直接影响试剂整体反应性,但是却对于检测结果有着很重要的影响。外周循环中除了待测标志物之外,还存在许多其他分子。这些分子可能和待测物具有类似的结构或构象;也可能与待测物存在共同的氨基酸片段。而抗体所识别的位点主要分为线性表位和构象表位。当抗体所识别的线性表位的氨基酸序列或者构象表位的结构域存在于其他分子中时,便会导至测试结果的假阳性或者假阴性。这既是抗体特异性差所导至的结果,也可以理解为抗体识别的抗原表位不够专一所致。不同分子间具有相同的抗原表位往往见于同源蛋白中,如心肌肌钙蛋白和骨骼肌肌钙蛋白直接存在多段相同的氨基酸序列;促甲状腺激素、促卵泡生成激素、促黄体生成激素和人绒毛膜促性腺激素存在共同的α亚基等。肌红蛋白与血红蛋白均具有血红素核心、地高辛和洋地黄毒苷具有类似的糖苷结构、糖抗原CA50和CA19-9均有Lewis-A糖抗原等。因此,抗体的识别位点是决定抗原特异性的关键性因素。
关于纯度,在体外诊断试剂制备过程中,往往需要先将抗体进行修饰,当抗体纯度不够时,会导至其他杂蛋白被一起偶联于固相介质或者标记物上,从而影响了试剂的反应性能,如特异性、反应信号、背景值等。抗体的纯度通常由细胞培养工艺和抗体纯化工艺所决定。使用无血清培养基可以很大程度上去除血清培养基中带来的杂质蛋白,而稳定精密的蛋白质纯化工艺则可以进一步将抗体中绝大多数杂质去除。目前,抗体的纯度测定主要有SDS-PAGE电泳后的条带扫描和HPLC测试等。值得一提的是,目前国内抗体生产厂家普遍存在的批间差问题,可以尝试从细胞培养和蛋白质纯化控制方面着手改善。
重复性/批间差,是指每批次产品的可重复性。之前所述的一系列抗体性能对于体外诊断试剂的性能有直接影响,而重复性则是保证体外诊断试剂降低批间差异并且稳定生产的前提条件。另外,如前所述,重复性和生产工艺密切挂钩,因此也是体现抗体质量的关键指标。
稳定性是指在特定的储存条件下,一定时间内抗体保持其活性的能力。值得注意的是,这里所指出的稳定性仅代表抗体在进行修饰/偶联之前的稳定性。抗体在进行修饰后,结构会根据工艺的不同产生的不同的变化,而后续的稳定性也很程度上取决于制备工艺,在制备成半成品试剂之后的稳定性并不能代表抗体的真实稳定性。抗体的保存条件对于抗体的稳定性至关重要,目前多数供应商提供的抗体的储存条件为4或-20℃;常规抗体的稀释液大多数为不含有其他蛋白和保护剂的缓冲液(抗体中若含有其他蛋白或者保护剂,会影响抗体的后续偶联)。关于37℃下的加速稳定性,目前大多数体外诊断生产公司倾向于使用37℃的加速破坏试验以模拟抗体的长期稳定性。其原理主要基于阿伦尼乌斯的经验公式推理而得,但是实际上加速稳定性并不能体现抗体的真实稳定性,其参考意义并不大。
随着我国体外诊断行业的迅速发展,相应的抗体产业也在迅速增长。但是由于我国相关行业起步较晚,因此国内抗体制造行业依然处于相对落后的阶段。现阶段,国内大多数免疫检测试剂依然以使用进口原料为主。目前主要的抗原抗体进口厂商有HyTest、Medix、Meridian和Biospacific等,这些公司均有着数十年的发展历史,对于抗体的研发生产和质量管理均有着系统化的控制。国内著名的原料生产企业有菲鹏等。随着中国体外诊断试剂行业的不断发展,中国市场越来越受到国际原料厂商的重视,可以说,除了少数因专利或特供限制不能商品化销售的原料外,国内IVD厂家与国际巨头在原料的获取渠道上已没有明显差距。
抗体的质量控制是保证体外诊断试剂质量的重要环节。目前,关于抗体质量控制尚没有国际公认的检验标准。不同的原料生产厂商的出厂检验也略有差异。其中,主要的检验指标有外观、纯度、浓度、分子量、活性、等电点等。此外,除上述常见的质检参数外,根据用户需求不同,可能会进行更多特殊的检测,如手性测试、质谱和糖谱测试等,这里不再赘述。
关于外观,一般情况下纯化后且没有杂质的单抗通过肉眼观察基本为均一澄清的溶液。而纯化工艺出现问题,导至蛋白质变性等则会引起溶液浑浊、蛋白质聚集沉淀等现象的产生。部分特殊抗体或者多抗可能不可避免地会出现轻微的沉淀或者浑浊,供应商一般会加以说明。此外,抗体冻干粉基本为白色粉末。关于纯度,如前所述是抗体重要的性能指标。目前的检测方法基本为SDS-PAGE电泳后的条带扫描和HPLC检测。理论上,抗体纯度越高,其偶联效率和活性就越高。对于不同生产批次抗体的纯度控制,是体现产品质量非常重要的一环。关于浓度,抗体的浓度对于抗体偶联具有重要的指导意义,是计算交联剂分子比例的关键参数。主要测定方法为Lowry法和OD280nm光吸收法等。目前,对于浓度的控制并没有严格要求,每次纯化后所获得浓度差异属于正常现象。针对目前大多数的抗体偶联工艺,浓度高于2mg/mL可基本满足要求。另外,若抗体浓度过低可以通过透析或者超滤进行浓缩;若浓度过高则可以用缓冲液进行稀释。关于分子量,目前体外诊断试剂所使用的抗体主要为IgG抗体,通过还原性SDS-PAGE电泳可以看到重链和轻链的电泳条带,从而根据其位置判断重链轻链的分子量。理论上,IgG重链的分子量约为55 KD左右,轻链约为25 KD左右,不同IgG之间可能会存在细微差异。若分子量差异较大,则提示抗体构象可能遭到了破坏。关于活性,对每一批生产出的抗体进行活性测试,是反映批间差异最直接的指标。细胞株保存、传代、培养、纯化工艺的过程控制,都会对抗体活性产生重要影响。因此活性差异的控制可以理解为是抗体质量控制的核心环节。目前,关于抗体活性测试的方法,主要是通过抗原与抗体反应的信号值来进行判断,反应平台以ELISA为主。关于等电点,在抗体偶联时,pH值是影响偶联反应的重要参数,而pH设定的依据则是根据抗体等电点。一般情况,在没有经过任何特殊修饰的情况下,不同抗体等电点差异不大。另外,随着蛋白质保存时间的推移,等电点可能会出现一定程度的偏移,因此等电点的测试对于质量控制并非关键性因素。
上述讨论内容为目前原料供应商对于原料的质控参数,而对于生产过程的控制则是获得理想质控参数的前提条件。根据抗体整个生产流程,可以将过程控制分为原料质量控制、细胞库质量控制和生产纯化质量控制三个环节。首先,高质量的原料是获得高质量产品的保障,其中包括对于动物源品质的控制、培养基质量的控制、生物安全性检测等。由于行业竞争激烈,目前部分生产厂商为了压缩生产成本从而降低了原料的质量控制,这也是我国目前抗体生产行业质量参差不齐的重要因素。其次关于细胞库质量控制,细胞库的系统化管理、合理的细胞储存、传代、培养是保证高质量抗体的前提。杂交瘤细胞在数次传代后会出现活力逐步下降现象,当细胞活力不足时会导至所生产的抗体活性大打折扣。另外,若细胞株保存不善受到污染,将会造成不可设想的严重后果。因此细胞株科学的保存、复苏及传代是非常必要的。关于生产和纯化,目前单克隆抗体的生产方式主要分为体内培养和体外培养两种。体内培养是通过小鼠腹水培养而得,而体外培养则是通过生物反应器而得。两种培养方式均对原料有着很高的要求,同时,在培养过程中细胞培养工艺的控制也十分重要。值得一提的是,由于动物保护问题和动物个体间的潜在差异,在未来体外培养生产抗体可能会成为主要的生产方式。在获得培养产物后(体内培养为小鼠腹水、体外培养为悬浮培养液),通过一定的纯化步骤便可获得最终的抗体。目前纯化方式主要为亲和层析和离子交换层析,对于单抗而言,主要以protein A/G 的亲和层析为主;而对于多抗,则以高纯度的抗原亲和层析为主。为进一步获得更高纯度的抗体,则可以选择在亲和层析之前进行离子交换层析。在纯化过程中,保证各项参数和原料的稳定是降低纯化后抗体的批间差的重要因素。此外,不同抗体在使用同样纯化工艺纯化时,所得的产物可能会出质量差异。因此,对于不同的抗体选择针对性的纯化方式是非常重要且必须的。
抗体经过出厂质检合格并到达体外诊断试剂生产商手中后,根据我国体外诊断试剂生产及质量控制技术的指导原则,需要对抗体进行入库检定。一般情况下,质检的指标主要包括:外观——肉眼观察,大部分生物原料为澄清均一的液体,不含异物、浑浊或摇不散的沉淀或颗粒;或为白色粉末且不含有其他杂质;特殊抗体应具备相应外观标准。纯度和分子量——主要方法是SDS-PAGE电泳后经考马斯亮蓝或者银染色法进行染色,然后对条带进行扫描分析。此外,高效液相层析也可以用于纯度和分子量测定。蛋白浓度——主要测定方法为Lowry法、OD280nm光吸收法和双缩脲法等。需要注意的是,不同方法学之间的结果存在一定差异,因此建议可以采取与原料厂商一致的方法进行验证。效价——一般在相应试剂平台上通过待测抗原进行测定。功能性——除上述抗体固有的性质之外,功能性结果可以直接反应该原料用于实际生产的效果。一般考查使用该原料的试剂的灵敏度、特异性、稳定性以及和上一批的平行对照等。这里值得指出的是,为了更严谨地对抗体批间差异进行验证,对于合格抗体的留样是非常有必要的。此外,还可根据实际情况定制或修改相应的其他功能性质检标准。
最后,关于抗体性能和质量与试剂性能和质量的关系。好的抗体是能做出好的试剂的前提,高品质抗体在最适的试剂制备条件下能够发挥出最佳性能。但是抗体在经过修饰偶联后形成最终的免疫检测分析系统则需要经过多种复杂工艺,其中任何一环的变化都会对最终的试剂性能产生影响。目前,我国体外诊断行业处于快速发展阶段,大量试剂质量已臻完善,但仍有许多项目或平台的制备工艺需不断优化及验证。抗体与试剂制备工艺在优秀的诊断试剂体系中相辅相成,对特定工艺而言,公认的好抗体却可能是“汝之蜜糖,彼之砒霜”,广泛筛选最适抗体是提升国产试剂质量和性能的关键一环。
在我国体外诊断行业快速发展的过程中,我们已经取得了巨大的成就,但与国际巨头之间仍有不小的差距。对于我国抗体生产厂商而言,需要更加系统且严谨地认识抗体的质量控制,从原材料到最后的生产纯化都必须严格把关,为中国体外诊断试剂厂商做好坚实后盾,共同推动我国体外诊断行业走上更加健康的发展道路。
来源:CAIVD
|
 /3
/3 