每隔3秒,全世界就会多一位阿尔茨海默病患者。全球60岁以上人群中约有5-8%患有阿尔茨海默症。随着人口老龄化,患病人数持续增加。 尽管自世界上首次发现、记录该病以来,人类已经同阿尔茨海默病斗争了110多个年头,然而在人口迅速老龄化的当下,该病仍是全球医疗界最大的挑战之一。 2023年9月21日,是第30个“世界阿尔茨海默病日”, 阿尔茨海默症的确切发病机制仍然不完全清楚,但研究表明,多种因素可能与其发病有关。其中,蛋白质异常积累被认为是一个关键因素。阿尔茨海默症患者的大脑中常出现β淀粉样蛋白和tau蛋白的异常积累,这些蛋白质聚集成堆积物,被称为β淀粉样斑块和tau蛋白缠结。这些斑块和缠结干扰了神经元正常的信号传递和功能,导至大脑细胞逐渐死亡,最终导至认知能力丧失。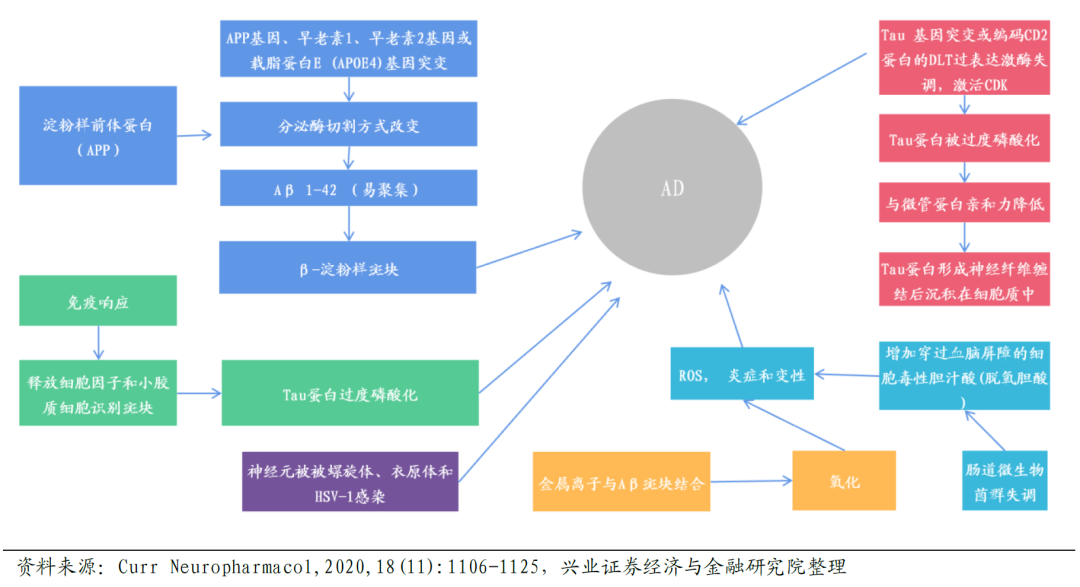 可喜的是,随着技术的发展,对于机制的研究越来越清晰,2023年7月6日,FDA宣布,将阿尔茨海默病新药lecanemab(商品名Leqembi)转为传统批准。据悉,这是首款靶向β-淀粉样蛋白、且由加速批准转为传统批准的阿尔茨海默病药物,也是20年来首款获得FDA完全批准的阿尔茨海默病新药。 不仅如此,随着检验手段的提高,越来越多的检测指标将会被写入到AD诊断指南中去,国际临床医生和研究人员委员会在2023年7月16日发布了新修订的阿尔茨海默病诊断指南草案(NIA AA Revised Clinical Guidelines for Alzheimer Alzheimer’ss),其中包括在临床设置中使用基于血液生物标志物检测的建议。
AD起病隐匿,临床主要变现为认知障碍、精神行为异常、社会生活功能减退,是一种病情进行性发展的神经退行性疾病。根据患者病情,AD通常分为临床前期、轻度认知障碍(mild cognitive impairment,MCI)、轻度、中度、重度AD,临床确诊时患者通常处于后3个阶段。在临床前期和MCI阶段,虽然患者症状不明显,但生物标志物指标已有异常。 来源:《自然评论-神经病学》、申万宏源和高禾投资研究中心
Aβ42是淀粉样蛋白的主要成分之一。近年多个大样本研究发现,阿尔兹海默症患者血清Aβ42水平较正常对照群体显著降低(Ashton, 2021;Jia, 2018)。这可能是因为Aβ42在阿尔兹海默症患者脑组织中聚集沉积所致。Aβ42水平的降低,与认知功能损害程度密切相关(Jia, 2018)。因此血清Aβ42是评估阿尔兹海默症病情进展的重要指标。 t-tau是反映神经元损伤的重要指标。一项包含2917例患者的大样本研究发现,t-tau升高水平与阿尔兹海默症高度相关(Ashton, 2021)。t-tau升高也与认知功能下降相关(Zhou, 2020)。 p-tau反映神经纤维缠结的生成。Meta分析显示p-tau显著升高是鉴别阿尔兹海默症的重要血清标志物(Wang, 2019)。p-tau与病情进展和脑组织损伤程度相关(Wang, 2019)。
蓝怡科技作为一家专注体外诊断仪器和试剂开发的厂家,目前的产品线已经覆盖在生化,免疫,过敏原,以及糖化、流水线等五大领域,蓝怡目前上市的AI3000全自动化学发光分析仪,即将推出配套的阿尔兹海默症检测试剂,未来蓝怡将持续布局阿尔兹海默症检测领域,给到中国市场更加优质的检测服务和体验。
文献来源: Jia L, Quan M, Fu Y, et al. Decreased serum β-amyloid 42 and increased tau levels are associated with cognitive impairment in patients with Alzheimer's disease. Frontiers in aging neuroscience. 2018;10:16. Ashton NJ, Pascoal TA, Karikari TK, et al. Plasma p-tau231: a new biomarker for incipient Alzheimer's disease pathology. Acta neuropathologica. 2021 Jan;141(5):709-24. Ashton NJ, Pascoal TA, Karikari TK, et al. Plasma p-tau231: a new biomarker for incipient Alzheimer's disease pathology. Acta neuropathologica. 2021 Jan;141(5):709-24. Wang M, Li Y, Niu F, et al. Diagnostic validity of plasma phosphorylated tau181 in Alzheimer's disease: a systematic review and meta-analysis. Journal of Alzheimer's Disease. 2019;67(2):675-87.
|
 /3
/3 