| CRISPR诊断被称为下一代分子诊断技术,美国FDA和中国NMPA都颁发过CRISPR诊断平台的新冠诊断EUA授权,上海伯杰医疗“恒温CRISPR法新冠快检试剂盒”获批的消息进一步激发了大家对CRISPR诊断的热情。CRISPR诊断主要包含样本前处理(含预扩增)、靶标识别、信号释放和检测几部分。本文将主要介绍CRISPR诊断方法所采用的侧向层析信号报告系统CRISPR技术被用于分子诊断主要因为特异性:在向导RNA的引导下,CRISPR-Cas蛋白识别靶标序列的特异性极佳,甚至可以精确区分单碱基差异。另外,Cas蛋白接触靶标序列后会被激活出无差别的反式切割活性,无差别的一阵刀光剑影,将周围一切可切割的核酸序列高效切割,从而起到放大信号的作用。 同时具备特异性识别和无差别切割特征的CRISPR诊断系统简直就是一把装着瞄准器的霰弹枪。 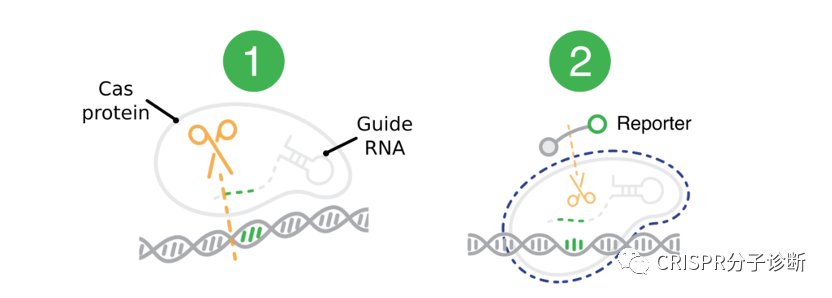 图1. Cas蛋白识别和切割靶标序列的示意图。图片摘自猛犸生物的官方网站。Cas蛋白通过向导RNA特异性识别并结合靶标序列(对于dsDNA靶标,则需要PAM序列),形成三元复合物,在顺式切割靶标序列的同时也激发出反式切割活性,将周围的核酸序列进行无差别的切割。目前,鉴定的有顺式和反式切割活性的Cas蛋白主要集中在Cas12和Cas13两类蛋白,分别识别(/切割)DNA序列和RNA序列。由于Cas蛋白只有在特异地识别和结合靶标序列后才切割周围的核酸序列,因此通过检测报告序列是否被切割就可以判定待检体系中是否存在靶标序列。几乎所有的CRISPR诊断方法都通过向体系中加入某些可被检测的外源探针来完成诊断的流程。张峰团队推出了SHERLOCKv2,引入核酸试纸条作为信号报告系统,非常便于POCT使用。他们在探针的两端分别引入两个小分子标记物FAM和生物素。而他们使用的商品化核酸试纸条将抗FAM抗体用胶体金标记,NC膜上检测线处包被有可结合生物素的链霉亲和素,这种试纸条的原本用途是通过夹心法检测同时含有FAM和生物素的核酸扩增产物。张锋团队则开创性地改变了试纸条本身的判读方式,将这种夹心法试纸条的质控线作为检测线来检测探针是否被切割。他们调整探针浓度,保证在探针未被切割时,所有胶体金都集中在下面那条线,而一旦探针被切割,就会有胶体金越过下面的线到达上面的线显色。 图2. 侧向流层析试纸条工作原理。图片摘自Milenia公司官网。该试纸条开发的最初用途是检测同时含有FAM和Biotin的产品(如上图),在张锋开发出其CRISPR用途后,Milenia公司也在官网展示了其CRISPR诊断方向的用途。图3. CRISPR诊断侧向层析法的工作原理。图片摘自SHERLOCKv2系统
将这种夹心法的试纸条通过竞争法方式进行判读的设计,非常巧妙。好处在于摆脱对仪器的依赖,可以更好地走向POCT。前段时间James Collins团队开发的、火爆全网的、可以检测新冠的口罩系统,也是采用这种方式。但是这种试纸条弊端,必须调整探针浓度适应试纸条。另外,通过这种方式也很难做多指标检测,难以在检测的同时添加内质控,不过这方面已经有一些新进展了。图4. CRISPR诊断侧向层析法的结果解读。图片摘自SHERLOCKv2系统。如上图最右条检测条带所示,在检测阴性样本时,也会出现淡淡的T线,从而会给检测结果的判读带来困扰。 |  /3
/3 