金桔
金币
威望
贡献
回帖0
精华
在线时间 小时
|
它们的基本原理是一样的:
不同的溶质,在固定相上吸附的牢固程度是不同的。
不同的溶剂,把同一种溶质从同一种固定相上洗脱的难易程度也是不同的。
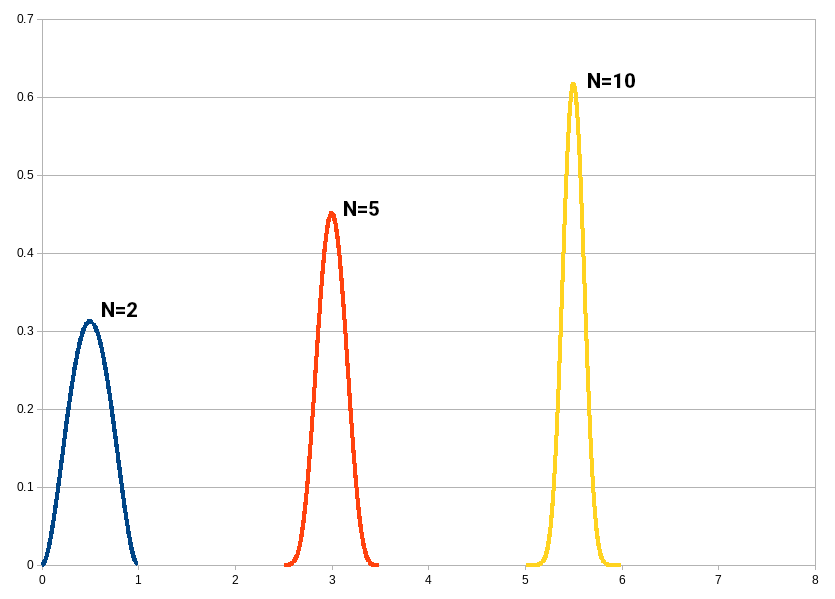
溶质首先是吸附在固定相上,然后被溶剂 (流动相) 洗脱,洗脱后又被下游的固定相吸附,然后再次被洗脱。这样层析过程实际上是无数个吸附/洗脱过程的组合 (热力学上用塔板数 N 描述),因此扩大了不同溶质的吸附/洗脱难易程度的差异,使之得到分离。
因为固定相会有不均匀性,溶质会因为浓度梯度而扩散,吸附/洗脱过程并不是瞬间达到平衡而是有传质阻抗,所以如果柱子短,流动相是良溶剂,加压,塔板数就少,洗脱峰就会很宽;增加塔板数,洗脱峰就会变窄。
实验室用的固定相一般是硅胶或者三氧化二铝。在上柱层析前,通常用薄层色谱 (爬板子) 来确定合适的流动相。流动相洗脱能力太强容易分不开,就是所有点都爬得很高,甚至爬到顶上了;太弱则都爬不起来,也分不开。
为了确定溶质在薄层色谱上的位置,点样的位置通常用铅笔圈出来;结束测试时流动相前锋的位置则用铅笔画一横线。
现在需要让板子上的溶质显色。如果溶质能被紫外线激发荧光,就可以用紫外灯照射薄层色谱 (板子) 或玻璃色谱柱来察看溶质的位置。如果没有荧光,但溶质能吸附 I2,可以放在碘瓶里用碘蒸汽着色。如果能被氧化显色,可以用高锰酸钾。 |
|
 /3
/3 