登陆有奖并可浏览互动!
您需要 登录 才可以下载或查看,没有账号?立即注册


×
衰老与健康状况整体下降、虚弱程度增加有关,是多种分子和细胞损伤随时间累积的结果[1][2]。多个信号通路在调节机体老化中扮演重要角色,如 PI3K/AKT, mTOR, AMPK, Sirtuins (SIRTs) 蛋白。其中,Sirtuins 被称为具有多种功能的蛋白质家族,如代谢控制,表观遗传修饰和寿命延长[3][4]。 Sirtuins (SIRTs) 蛋白家族是 NAD+ 依赖性脱乙酰酶和脱酰酶,由七个成员组成 (SIRT1-7)[5]。SIRTs 蛋白家族成员之间的差异最初归因于它们的亚细胞定位的离散模式。 图 1. 哺乳动物 Sirtuins 的细胞内定位[5]。 SIRTs 可控制重要的细胞过程,包括 DNA 损伤修复、细胞代谢、线粒体功能和炎症,被认为是细胞功能和生物体健康寿命的重要调节剂。在临床前模型中,SIRTs 表达和活性的增加可减缓疾病进展并改善心血管功能,并延缓细胞衰老的各种特征[6][7]。 20 世纪 90 年代首次发现 SIRT2 基因可以延长酵母的寿命,使 SIRTs 成为最早被发现的长寿基因家族之一[8]。2021年,A Roichman 等发现 SIRT6 过度表达会导至雄性和雌性 B6 小鼠的虚弱程度减少并延长寿命[9]。2023年,Zhang 等发现 SIRT2 缺乏会加剧人类和小鼠衰老引起的血管重塑,细胞质-线粒体轴 (SIRT2- p66Shc - mROS) 对血管衰老至关重要[10]。 同年,Fernández-Ruiz 研究确定 SIRT2 - STAT3 - CDKN2B 轴为灵长类动物生理性心脏衰老的关键调节因子,并表明 SIRT2 过表达可逆转小鼠的自然心脏衰老,这表明 SIRT2 调节可用于预防心脏衰老和衰老相关疾病[11]。 表 1. 与衰老相关的 SIRT 家族的性质和功能[12]。 衰老是细胞和组织损伤逐渐累积的系统性反应,导至稳态能力的恶化。细胞和机体通过预防病变、修复病变、移除和替换不可修复的结构以及下游补偿等,具体表现为调节机体免疫炎症、细胞新陈代谢、氧化应激、DNA 修复等多种方式延缓损伤的积累[12][13]。 图 3. SIRTs 在炎症中的作用概述[6]。
(A) SIRTs 主要通过调节炎症介质发挥抗炎作用,早期抑制 SIRT2 可以预防神经炎症,具体表现为 GFAP、IL-β、IL-6 和 TNF-α 水平降低;(B) SIRT 可以负向调节多种促炎细胞因子;(C) SIRTs 参与 NF-κB 信号通路的调节。 此外,研究表明,Sirtuin 介导的线粒体自噬在衰老和年龄相关疾病中发挥着显著作用。SIRT1 和 SIRT3 可以作用于 PINK1/Parkin 通路的上游,并通过许多其他通路激活线粒体自噬。同时,Sirtuins 调节转录因子和酶,如 HIF-1α、PGC-1α、FOXO1、PPARγ 等。Sirtuins 还可以通过与线粒体自噬蛋白(如 ATG5、ATG7 和 ATG8)相互作用和/或翻译后修饰来直接影响线粒体自噬。此外,它们还可以间接增加线粒体自噬相关蛋白的表达,如 mTORC1、PARK1、Beclin-1、BNIP3 等。越来越多的证据表明去乙酰化酶是线粒体自噬过程及其对衰老和年龄相关疾病影响的关键因素[12]。 图 4. SIRT1 介导的线粒体自噬途径[12]。
PARP1 与 SIRT1 竞争 NAD+,导至 SIRT1-PPARGC1A-UCP2 轴受到抑制,从而导至线粒体膜电位增加并抑制线粒体自噬。miR-22 抑制 SIRT1/PGC-1α 轴并降低 PINK1/Parkin 表达,抑制线粒体自噬。SIRT1 使 FOXO1/3 去乙酰化并直接或通过激活 FOXO1/3-PINK1-Parkin 轴增强线粒体自噬。SIRT1 使 MFN2 的 K655 和 K662 位点去乙酰化并增强线粒体自噬。17b-E2 增加 SIRT1 和 AMPK 表达并减少 mTOR 表达,从而增强线粒体自噬。 自从发现 Sirtuins 可以延长酿酒酵母 (Saccharomyces cerevisiae) 和秀丽隐杆线虫 (Caenorhabditis elegans) 的寿命以来,Sirtuin 延长寿命的机制以及是否可以延长其他物种的寿命已被积极研究。许多关于沉默调节蛋白激活剂的研究现已达成共识。 Sirtuin 激活剂可以通过激活 Sirtuin 诱导的多种生物功能来调节衰老和与年龄相关的疾病,并在实验模型中表现出显著的衰老延迟和疾病缓解作用 (表 2)。表 2. Sirtuins 的激活剂[12]。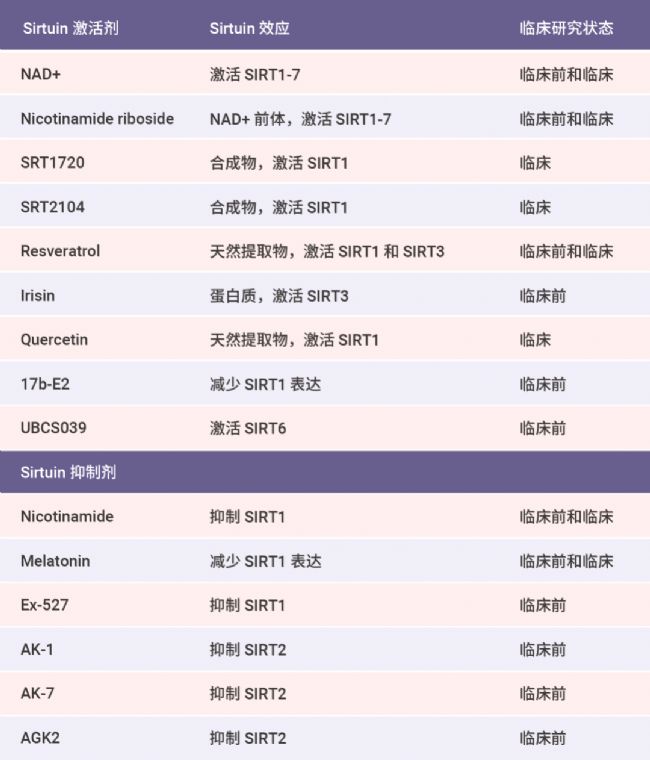 IRT1 的活性可以通过被称为 Sirtuin 激活化合物 (STACs) 的药物来增加。最早的 STACs 之一白藜芦醇是在对增加人类 SIRT1 活性并延长酵母寿命的分子进行筛选时发现的[14]。此后出现了效力和特异性不断提高的几代 STACs,包括 SRT1720 和 SRT2104[15]。此外,衰老过程中 NAD+ 水平下降会降低 Sirtuin 活性,这可能会促进衰老过程。
随着世界各地人类预期寿命的不断延长,寻求与年龄相关的疾病解决方案的人数也在不断增加。全球 8.5% 的人口(6.17 亿)年龄在 65 岁或以上,很明显,SIRTs 家族在衰老过程中发挥着重要作用,其研究有助于改善人们的生活质量。今天,小 M 为大家介绍了 SIRTs 家族与机体衰老之间的联系。  [1] Roichman A, et al. Restoration of energy homeostasis by SIRT6 extends healthy lifespan. Nat Commun. 2021 May 28;12(1):3208.[2] Lagunas-Rangel FA. SIRT7 in the aging process. Cell Mol Life Sci. 2022 May 18;79(6):297. [3] Ji Z, et al. Mitochondrial sirtuins, metabolism, and aging. J Genet Genomics. 2022 Apr;49(4):287-298. [4] Perico L, et al. Sirtuins in kidney health and disease. Nat Rev Nephrol. 2024 Feb 6. [5] Ziętara P, et al. Why Is Longevity Still a Scientific Mystery? Sirtuins-Past, Present and Future. Int J Mol Sci. 2022 Dec 31;24(1):728. [6] Wu QJ, et al. The sirtuin family in health and disease. Signal Transduct Target Ther. 2022 Dec 29;7(1):402. [7] Grootaert MOJ, et al. Sirtuins in atherosclerosis: guardians of healthspan and therapeutic targets. Nat Rev Cardiol. 2022 Oct;19(10):668-683.[8] Kaeberlein M, et al. The SIR2/3/4 complex and SIR2 alone promote longevity in Saccharomyces cerevisiae by two different mechanisms. Genes Dev. 1999 Oct 1;13(19):2570-80.[9] Roichman A, et al. Restoration of energy homeostasis by SIRT6 extends healthy lifespan. Nat Commun. 2021 May 28;12(1):3208.[10] Zhang Y, et al. Sirtuin 2 deficiency aggravates ageing-induced vascular remodelling in humans and mice. Eur Heart J. 2023 Aug 1;44(29):2746-2759.[11] Fernández-Ruiz I. Sirtuin 2 protects against cardiac ageing. Nat Rev Cardiol. 2023 Dec;20(12):796.[12] Wan W, et al. Regulation of Mitophagy by Sirtuin Family Proteins: A Vital Role in Aging and Age-Related Diseases. Front Aging Neurosci. 2022 May 9;14:845330. [13] Moskalev A, et al. Targeting aging mechanisms: pharmacological perspectives. Trends Endocrinol Metab. 2022 Apr;33(4):266-280.[14] Howitz KT, et al. Small molecule activators of sirtuins extend Saccharomyces cerevisiae lifespan. Nature. 2003 Sep 11;425(6954):191-6.[15] Milne JC, et al. Small molecule activators of SIRT1 as therapeutics for the treatment of type 2 diabetes. Nature. 2007 Nov 29;450(7170):712-6.
|  /3
/3 