登陆有奖并可浏览互动!
您需要 登录 才可以下载或查看,没有账号?立即注册


×
芝友医疗是一家个体化用药基因诊断试剂盒和循环肿瘤细胞检测设备的提供商。公司个体化用药基因诊断试剂盒中有6款已上市,另有8款产品在研,其中4款产品已于2015年获批。公司的CTC产品已于2016年取得CFDA注册证,并于2016年上市。目前,公司处于战略亏损阶段,2016年上半年营业收入和扣非后净利润分别为1249.98万元和-815.09万元,收入同比增速为296.83%。2016年7月13日,公司在新三板挂牌上市。 分子诊断市场是蓝海,行业有望迎来大爆发。(1)中国体外诊断行业基数小、增速高:我国体外诊断产品市场在全球体外诊断产品占比偏低,2010年仅为3.8%,与人口比重不符。近三年,我国体外诊断行业高速增长,复合增长率达20.79%;(2)体外诊断行业中,分子诊断子行业增长最快,复合增速达26.5%。分子诊断触角已延伸至多种疾病、不同领域,成为精准医疗发展的基石。 高研发支出助力公司技术领先,三大技术平台支撑新品研发。近年公司研发投入逐年增加,2016年上半年研发投入645.93万元,同比增加147.19%,过去3年研发占营收比重达68.89%。持续研发投入下,公司建立了ARMS—PCR荧光定量PCR平台、多重荧光定量PCR平台、ISET技术平台,共获批12项发明专利,为明星产品循环肿瘤细胞检测仪提供了良好的知识产权保护。新产品方面,公司自主研发的肿瘤靶向药物分子诊断、心脑血管疾病检测试剂盒将为精准医疗提供临床诊断依据。 CTC产品和分子诊断产品将推动芝友医疗收入端快速成长。在产品线上,公司的分子诊断产品和CTC产品形成高低搭配,伴随公司销售渠道的扩展,公司总体收入水平料将保持50%以上的增速,预计未来三年公司试剂盒产品将实现3150万元左右的收入。(1)公司CTCBIOPSY检测技术是国内首家获得CFDA II类注册证的动化CTC检测设备,预测2017年CTC检测设备可销售80台,将实现销售收入1000万元。(2)目前公司共有10个基因检测试剂盒上市,2016年上半年诊断试剂盒销售收入592.53万元,按照产品的成长逻辑测算,2017年诊断试剂收入将突破1000万元,公司整体将扭亏为盈。 风险因素。(1)新产品注册审批风险;(2)核心技术失密风险;(3)市场竞争加剧的风险;(4)持续亏损风险;(5)实际控制人不当控制风险。 估值分析。以2017年2月23日收盘价为参考,可比公司平均市值125.9亿元,2015/TTM的PS为13X/11X;2015/TTM的PE为107X/93X。2015年芝友医疗收入和净利润分别为940.27/-990.93万元(扣非后净利润-1068.79万元),公司处于协议转让状态,暂不给予定价。  

目录  公司概述:个体化医疗领域的创新型企业 主营业务:个体化用药基因诊断试剂和诊断设备提供商 武汉友芝友医疗科技股份有限公司成立于2011年7月。公司主要为肿瘤及心血管疾病病人提供个体化用药基因诊断试剂和设备的研发、生产和销售服务。公司现有8款基因诊断试剂产品,包括肿瘤靶向药物检测类、心血管药物检测类以及代谢检测类等。此外,公司研发的CTC(循环肿瘤细胞)检测平台,已经于2015年获取批件,现通过销售仪器获取收入。2016年上半年公司营业收入和净利润分别为1249.98万元和-776.48万元(扣非后净利润-815.09万元),收入同比增长296.83%%。2016年7月13日,公司在新三板挂牌上市。  业务一:诊断试剂销售业务贡献主要收入源。公司现有8款试剂盒,涵盖了肿瘤和心血管疾病领域。公司肿瘤靶向药物分子诊断试剂产品主要用于非小细胞肺癌患者和结直肠癌患者,包括EGFR基因突变检测试剂盒、KRAS基因突变检测试剂盒、BRAF基因突变检测试剂盒等。公司心血管药物分子诊断产品主要用于华法林类抗凝药物、氯吡格雷类抗血小板药物以及他汀类降脂药物的用药指导,包括CYP2C9和VKORC1基因突变检测试剂盒、CYP2C19基因检测试剂盒、SLCO1B1和ApoE基因突变检测试剂盒。2016年上半年,公司个体化基因检测产品共实现收入592.53万元,同比增长114.04%,占比47.40%。 业务二:循环肿瘤细胞检测产品收入快速增长,营收占比不断攀升。公司循环肿瘤细胞检测产品共3种,包括CTCBIOPSY异常细胞分离染色仪(2012年获批上市)、循环肿瘤细胞快速染色液(2015年获批上市)、CTCBIOPSY®细胞过滤器(2016年获批)。随产品陆续进入市场,2016年上半年公司CTC产品实现收入643.43万元,同比大幅增长1994.00%,营收占比达51.48%。   财务分析:公司2016年上半年收入和扣非后净利润为1249.98/-815.09万元 芝友医疗目前处于战略亏损状态。2016年上半年公司营业收入和净利润分别为1249.98万元和-776.48万元(扣非后净利润-815.09万元),收入同比增长296.83%。营业收入增加主要因为公司基因检测产品收入达到592.53万元,同比增长114.04%;循环肿瘤细胞检测产品收入643.43万元,同比增长1994.00%。净利润下降的原因主要是公司加大产品研发投入以及开拓市场所带来的销售费用的增加。2016年上半年公司研发投入达645.93万元,,销售费用投入702.54万元,同比增长223.02%。公司的毛利率不断提升,2016年上半年达到82.27%。2016年上半年销售费用率和管理费用率不断下降,分别为56.20%/91.58%。流动比率和速动比率分别达到4.35和3.85,偿债能力较好。    分子诊断市场是蓝海,基因诊断是亮点 临床诊断指医生给病人检查疾病,对病人疾病的病因、发病机制做出分类鉴定,以此作为制定治疗方案的重要依据。临床诊断分为体外诊断与体内诊断,其中体外诊断指在机体外,通过实验方法对包括但不限于“血液、体液、分泌物、组织、毛发”等机体成分以及附属物进行检测,从而获取疾病预防、诊治、监测、预后判断、健康及机能等数据的行为。临床上有80%以上的疾病诊断依靠体外诊断完成。 按检验原理或检验方法,现应用广泛且技术含量较高的体外诊断技术主要包括生化诊断、免疫诊断、分子诊断。其中分子诊断是应用分子生物学的方法,检测受检个体的遗传物质或携带的病毒、病原体的基因结构与类型,进而从基因层面对遗传病、传染性疾病、肿瘤等疾病进行检测诊断。  分子诊断行业基数小、增速高 基础科学进步带动生物药产业向国际领先水平看齐。根据南方所公布,2014年,生物医药领域2014年实现收入和利润分别为:27.4亿和3.2亿,增速分别为:15.12%和14.29%,成为为数不多的远超GDP增速的行业之一。近年来,国家不断加大对生物医药产业的支持力度,国务院出台的《“十二五”国家战略性新兴产业发展规划》将生物产业定为七大战略性新兴产业之一。分子诊断行业料将明显受益于行业相关政策和资金扶持。 目前中国分子诊断行业仍处于发展初期,随着人口老龄化、医疗模式的转变,市场对分子诊断的需求将不断增加。中讯咨询此前预计,2014 年我国分子诊断领域市场规模将达18.3 亿元,同比增速22.13%。随着国家政策的扶持和需求的增长,未来几年市场年均有望维持高达20%以上的增速。   从技术上分,分子诊断技术包括聚合酶链式反应(PCR)、等温核酸扩增(INAAT)、杂交、DNA测序和NGS、芯片等。在这些技术中,聚合酶链式反应(PCR)是最成熟、应用最广泛的技术,在2013年占据分子诊断技术市场的最大份额,达40%。三甲医院的检验科和中心实验室都有配备,且检验技术人员熟悉其技术操作,因此基于PCR技术的诊断试剂盒能在销售终端和客户无缝连接,分享成熟的医院PCR技术平台。  分子诊断触角延伸,应用领域拓展至多种疾病、多项领域。分子诊断产品应用在临床疾病如肿瘤、感染、遗传等诊断领域占到70%以上,体检中心、技术服务中心、第三方检测机构及微生物快速检测市场也有应用。由于分子诊断试剂的便利和速度优势,该技术未来可扩展至牲畜的检验检疫、边防海关的检验检疫等领域。分子诊断推动精准医疗发展。利用分子诊断技术检测不同患者基因突变的种类从而制定个体化治疗方案,能避免药物的误用和滥用,真正做到精准医疗。  竞争格局分析:分子诊断市场格局尚未确立,公司处于第二梯队 体外诊断行业集中度较高,分子诊断市场割据。从20世纪70年代开始,全球体外诊断市场随着技术发展而成长,目前已形成数百亿美元的巨大市场。行业现阶段发展成熟,技术壁垒高,聚集了一批著名跨国企业,包括罗氏、西门子、雅培、强生、伯乐等,行业巨头不断收购新公司和新技术,从而形成寡头垄断的竞争格局。现阶段,我国的诊断试剂生产厂家众多,但年销售额过亿元的企业较少,约20家,其中以试剂厂商居多。在分子诊断市场竞争格局尚未确立的情况下,芝友医疗处于行业第二梯队。 分子诊断市场国产设备为主、进口为辅。国内分子诊断市场目前以国内企业为主,主要企业包括达安基因、科华生物、复星医药等。由于中国的市场准入问题,国外企业中只有少部分企业,诸如罗氏、雅培、凯杰等公司有部分产品进入中国市场。从而形成了国产为主、进口为辅的产业格局,其中罗氏和达安基因市场占比最大分别为15.8%和12.50%。在国内分子诊断产品同质化和价格战愈演愈烈的情况下,创新型的分子诊断检测手段的出现,将能够帮助芝友医疗从红海市场脱颖而出。   亮点一:高研发支出助力技术领先,明星产品瞄准市场痛点 高研发支出布局分子诊断市场,多项核心专利构筑技术壁垒 公司拥有厚实的科研团队,持续研发支出丰富产品种类,研发实力深厚。目前共有研发人员51名,占员工总数的41.46%,其中硕士和博士以上学历的人员占据30%,核心技术团队保持稳定,核心人员共5名,其中2人为公司高管和“3551人才”,同时中基层研发团队成员60%以上为重点大学硕士学历。其中周宏灏院士是芝友医疗个体化医学研究中心主任,周鹏飞博士在免疫学及肿瘤治疗方面多有建树。近年公司研发投入逐年增加,2016年上半年研发投入645.93万元,同比增加147.19%,过去3年研发占营收比重达68.89%。    持续的研发支出下,公司技术端创新稳步提升。截止2016年上半年,公司已经申请27项专利(其中2项PCT专利),共获得授权专利12 项,其中公司自主研发的循环肿瘤细胞捕获系统(CTCBIOPSY)已获得授权专利11项。这些专利的取得,为公司打造了三大核心技术平台:ARMS-PCR的荧光定量PCR平台、多重荧光定量PCR平台、和ISET技术平台。    技术平台一:ARMS-PCR的荧光定量PCR平台。ARMS技术可检测出样品中含量低至0.1~1.0%的突变基因,具有高度的灵敏性;而且该检测方法可以最大限度的缩短目标产物的长度,解决石蜡包埋组织标本提取的DNA大部分片段化而无法得到准确检测结果的问题;此方法结合实时PCR平台实现闭管操作,操作简单,不需要产物后处理,最大限度的避免扩增产物的污染。公司主要利用该平台研发肿瘤靶向药物分子诊断产品,用于非小细胞肺癌、甲状腺癌、结石肠癌等的治疗。通过采用ARMS引物和阻断探针进行双重阻断技术,有效提高检测的特异性;同时通过闭管操作,采用内标系统和UNG酶系统防止假阳性和假阴性。   技术平台二:多重荧光定量PCR平台。多重荧光定量PCR平台可以实现多个目标基因的同时检测,可根据目标基因的各个单核苷酸多态性位点,设计特异性引物和分别针对单核苷酸多态性位点并连接不同荧光标记(通常对应荧光定量PCR仪的FAM和VIC荧光通道)的TaqMan探针,实现在同一个反应管中扩增,完成检测结果的定性分析。公司主要利用该平台研发出的心脑血管基因检测产品有CYP2C9 和 VKORC1基因突变检测试剂盒、CYP2C19基因突变检测试剂盒、SLCO1B1和ApoE基因突变检测试剂盒,可分别用于华法林类药物、氯吡格雷类抗血小板药物、他汀类降脂药物用药指导。  技术平台三:ISET技术平台。ISET(Isolation by Size ofEpithelial Tumor Cells)技术是根据循环肿瘤细胞CTC与血细胞在大小、形变能力等物理特征上的差异进行CTC分离,并利用CTCs典型的染色特征对其染色从而可轻易区分细胞体积较大的正常细胞和CTCs。ISET技术具有四大技术优势:1)利用物理特性差异,不需要任何蛋白或分子标记,从而不会丢失一些重要的上皮标记物,可以有效捕获循环肿瘤微栓;2)准确率高、特异性强、节约检验标本;3)分离染色一步完成,检测速度快,30分钟内完成分离富集和染色,2小时内完成阅片,1个工作日内出具检测报告。公司现已经建成一套较全面的CTC产业线,包括CTCBIOPSY异常细胞分离染色仪、循环肿瘤细胞快速染色液、CTCBIOPSY®细胞过滤器3类产品,其中核心产品CTCBIOPSY异常细胞分离染色仪突破了市面上现有的CTCs检测技术依赖于特定的细胞表面标记物这一局限,利用不同细胞的物理和形态学差异进行分离染色,提供了直观可靠并且可随时复检的检测结果。该产品已于2016年初上市,随着销售渠道的拓展有望凭借产品优势时间大规模的销售增长。 自动化CTC检测设备 CTCBIOPSY®有望推动公司业务快速增长 对于肿瘤患者,个体化治疗具有重大意义。肿瘤是机体在各种致癌因素作用下,局部组织的某一细胞在基因水平上失去对其生长的正常调控,导至细胞异常增生形成的新生物。对男性而言,发病率最高的是肺癌,其次是胃癌、肝癌,对女性而言,乳腺癌是第一杀手。现阶段恶性肿瘤的治疗方法主要有手术治疗、放射治疗、化学治疗、生物治疗、物理治疗、中医治疗等。医生通过这些治疗手段来提高肿瘤患者的5年生存率是首要目标。由于人类个体化差异,不同病人对于不同治疗方法耐受性不同,因此采用个体化靶标检测技术,将有助于对不同病患制定出针对其个人致癌位点精准治疗措施是未来大趋势。个体化靶标检测技术将收益于日益增大的肿瘤个体化医疗检测服务需求。     与传统检测相比,CTC检测样本获取简便,且在肿瘤周期的各个时段都可以检测,具有广阔的市场空间。据测算,中国每年新增肿瘤检测约500万,以每人每年按季度检测4次测算,至2018年,CTCs市场容量将达到3亿元。公司作为CTCs技术的开拓者将直接受益。   CTCBIOPSY®是国内首家获得CFDA II类注册证的自动化CTCs检测设备,通过使用创新工艺的高分子材料微孔滤膜过滤装置,根据细胞形态学差异和物理特性的不同,结合先进的机械、电子、流控等技术快速将外周血中的CTCs从正常血液细胞中分离及富集,并利用专利技术(201210471758.4)进行染色鉴定。细胞形态学和物理特性分离CTCs与血液细胞的原理:1.红细胞直径5-9um、粒细胞直径10-15um、淋巴细胞和单核细胞直径分别为7-18um、12-20um,CTCs直径大于16um;2.相比较而言,CTCs因为含有角蛋白等形成的复杂结构,相对较硬,不易变形,易于被截留;3.CTCs具有典型的染色特征。因此该技术可以轻易区分细胞体积大的正常细胞和CTCs。   当前,全球个体化医疗检测市场主要分布于北美、欧洲、日本等经济发达国家,在中国等新兴经济体国家仍属于新兴行业。友芝友医疗自2011年7月成立以来,以肿瘤的个体化医疗为战略方向,专门从事个体化用药基因诊断试剂和诊断设备研发、生产和销售。2015年4月,公司研发生产的循环肿瘤细胞检测设备CTCBIOPSY®获得CFDA注册证上市。友芝友作为独家设备供应商参与到循环肿瘤细胞相关国家数字诊疗装备研发试点专项科研项目中,持续完善CTC检测产品,不断推进科研合作,目前已与9家高校及研究生建立合作关系。  学术代理模式销售助力销售翻番。公司循环肿瘤细胞检测仪主要通过学术代理的模式销售,结合自身的学术推广能力和代理商的推广渠道,2016年销量突破50台。2016年上半年循环肿瘤细胞检测收入高达643.43万元,,预计2017年将销量增长30台,实现销售收入1000万元。  亮点二:八大靶向类产品将帮助公司提升个体化肿瘤治疗市场份额 2016年,芝友医疗8个基因诊断类试剂盒产品提交注册报备,进入临床试验阶段及注册审评阶段,其中四大肿瘤靶向基因检测试剂盒:人类NRAS基因突变检测试剂盒(PCR-荧光探针法)、人类EML4-ALK融合基因检测试剂盒(PCR-荧光探针法)、人类ROS1基因融合检测试剂盒(PCR-荧光探针法)、人类PIK3CA基因突变检测试剂盒(PCR-荧光探针法)顺利获批国家食品药品监督管理总局(CFDA)三类注册证,加上此前获批的6类试剂盒产品,芝友医疗的肿瘤靶向基因检测试剂盒产品,已经能够提供非小细胞肺癌、结直肠癌、乳腺癌等多种癌症的分子病理学基因检测完整解决方案。 NRAS突变对西妥昔单抗、帕尼单抗治疗具有重要的指导意义,市场应 成神经细胞瘤鼠肉瘤癌基因(Neuroblastoma ras viral oncogene homolog,NRAS)属于Ras基因家族。在细胞的讯息传递路径上,Ras主要为活化控制基因转录的激酶,调节细胞的增殖与分化。NRAS基因的突变主要位于第2、3、4外显子上,导至多种恶性肿瘤,在结直肠癌患者中的突变率为1-6%,是人体肿瘤中常见的致癌基因。目前, NRAS基因检测已被欧美地区列为大肠癌患者内科治疗前必做的常规检查、美国癌症综合网络(NCCN)的《NCCN结肠癌临床实践指南》与《NCCN直肠癌临床实践指南》列为临床用药必检项目。NRAS突变对西妥昔单抗、帕尼单抗在结直肠癌患者的治疗具有重要的指导意义。  公司的基因突变检测试剂盒结合ARMS&LNA技术设计源头保证检验结果的可靠性,引进UNG酶防污染系统确保结果可信,具有1%的灵敏度,仅需少量肿瘤标本即可检测,操作简单快捷,在国内处于领先地位。该产品主要利用公司已有的销售渠道经销到各大医院和第三方检测机构,根据公司2016年半年报数据,公司产品已从年初不足40家医院陆续进入全国150余家大中型医院,市场需求强劲。   除了芝友医疗外,目前市场上NRAS基因突变检测试剂盒的其他提供商主要有厦门艾德生物医药科技有限公司、北京雅康博生物科技股份有限公司等。根据行业代表性企业艾德生物KRAS系列产品近年销售额和市场上的需求分析,预计2017年人类NRAS基因突变检测试剂盒将为芝友医疗带来400万元左右收益增长。  EML4-ALK融合基因检测试剂盒可有效检测非小细胞肺癌,受患者关注 EML4-ALK融合是非小细胞肺癌(NSCLC)中多见的融合类型,可导至ALK的酪氨酸激酶持续高表达,从而激活下游的信号通路,进而促使表达这些蛋白的肿瘤细胞增殖和存活。临床研究表明,克唑替尼在肿瘤细胞株中对ALK和c-Met在细胞水平检测的磷酸化具有浓度依赖性抑制作用,对表达EML4-ALK或NPM-ALK融合蛋白或c-Met的异种移植荷瘤小鼠具有抗肿瘤活性。在NSCLC患者中,ALK重排的阳性率约为3%-5%,在腺癌、从未吸烟或少量吸烟的患者中EML4-ALK融合的几率高。晚期ALK阳性NSCLC患者中,克唑替尼的客观缓解率可达50%-61%。目前CFDA已批准克唑替尼(赛可瑞)用于ALK阳性局部晚期或转移性NSCLC患者治疗。  公司的人类EML4-ALK融合基因突变检测试剂盒具有结果可靠、灵敏度高、简便快捷等优点。除了芝友医疗外,目前市场上人类EML4-ALK融合基因突变检测试剂盒的其他提供商主要有厦门艾德生物医药科技有限公司、北京雅康博生物科技股份有限公司等。根据市场上人类EML4-ALK融合基因突变检测试剂盒主要提供者艾德生物销售规模和市场上的需求分析,我们预测未来三年人类NRAS基因突变检测试剂盒有望为芝友医疗带来300万元以上收益增长,并随着市场替代实现销售额的进一步提升。 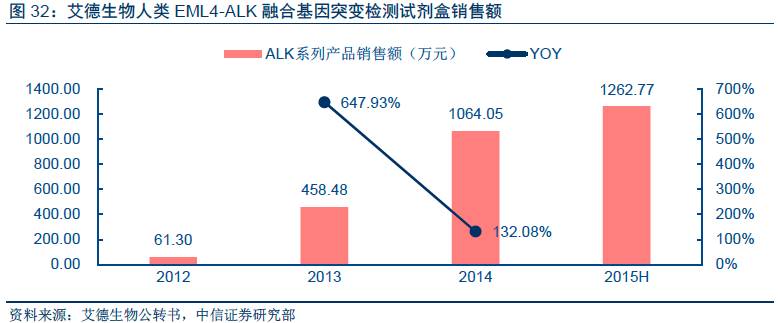 ROS1基因融合是预测靶向药物克唑替尼的重要标志物,市场需求多 ROS1基因编码一种受体酪氨酸激酶,当与SLC34A2、CD74等基因发生融合后,会持续激活ROS1酪氨酸激酶区及下游JAK/STAT、PI3K/AKT、RAS/MAPK等信号通路,进而引起肿瘤的发生。ROS1基因融合在非小细胞肺癌中的发生率约2-4%,主要发生于年轻、非吸烟的腺癌患者。美国国立综合癌症网络(NCCN)临床实践指和欧洲肿瘤内科学会(ESMO)肺癌共识均明确指出,ROS1基因融合是预测靶向药物克唑替尼等ROS1抑制剂疗效的重要生物标志物,ROS1阳性的非小细胞肺癌患者可以从ROS1抑制剂治疗中获益。 最新权威指南推荐非小细胞肺癌患者使用靶向药物前进行EGFR/ALK/ROS1基因检测。芝友医疗人类ROS1基因融合检测试剂盒可达到1%的灵敏度,并且在90分钟内快速完成检测,产品优势明显。目前市场上人类ROS1基因突变检测试剂盒的其他提供商主要有厦门艾德生物医药科技有限公司、北京雅康博生物科技股份有限公司、武汉海吉力生物科技有限公司等。根据历史数据和市场上的需求,我们预测2017年人类ROS1基因突变检测试剂盒将为芝友医疗带来300万元以上收益增长,并随着市场替代实现销售额的进一步提升。   PIK3CA基因检测结果是乳腺癌患者合理用药的参考依据,市场潜力大 PIK3CA基因是由Volinia在1994年利用原位杂交技术检测到的,研究发现约30%的人类实体瘤存在PIK3CA基因的突变,导至PI3K信号途径在不同水平发生调控异常。功能和遗传学研究显示,PIK3CA是一个致癌基因,在肿瘤细胞中,其激酶活性增强,能持续刺激下游AKT(蛋白激酶B),使细胞不依赖生长因子增殖,增加细胞侵袭和转移能力。 研究发现,有PIK3CA突变的肿瘤细胞使用针对EGFR或ERBB2通路的靶向药物拉帕替尼(Lapatinib)会产生耐药性。PIK3CA基因发生突变的患者,爱必妥(治疗结肠癌的一种药物)治疗有效率低。此外还有研究表明,选择性针对HER2(乳腺癌预后判断因子)的靶向治疗药物赫赛汀(Herceptin)对PIK3CA基因突变的人群疗效欠佳,因此PIK3CA基因检测结果也是乳腺癌患者合理用药的参考依据,未来市场将有较大的需求。 目前市场上除了芝友医疗之外,人类PIK3CA基因突变检测试剂盒的提供商还包括厦门艾德生物医药科技有限公司、北京雅康博生物科技有限公司、益善生物技术股份有限公司等。芝友医疗的人类PIK3CA基因突变检测试剂盒(流式荧光杂交法)乃自主开发,可以有效地检测PIK3CA基因是否发生突变,可以为结肠癌的治疗用药提供指导,根据芝友医疗的历史数据及人类PIK3CA基因突变检测的市场需求情况,预计公司人类PIK3CA基因突变检测试剂盒上市后,每年将贡献300万元以上的收入。 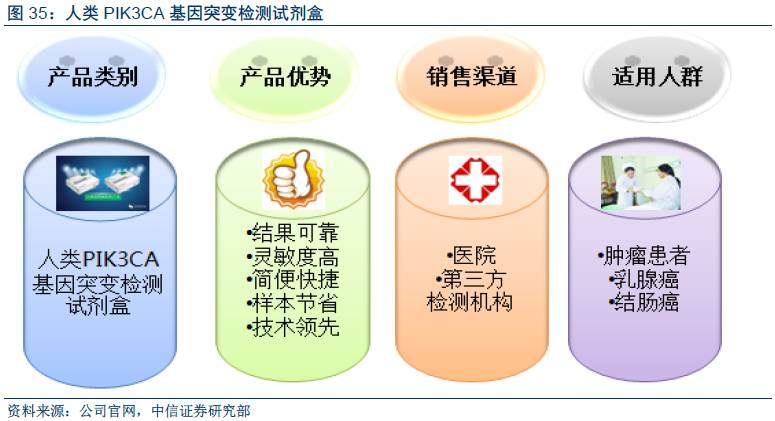 公司个体化基因诊断产品中肿瘤靶向药物分子诊断产品已经比较成熟,2015年营收占比接近50%,心脑血管药物分子诊断产品正在不断投放市场。2016年上半年公司基因诊断产品实现销售收入592.53万元,同比增长114.04%,预计2016年实现收入1400万元左右,同比增长160%,并预计未来三年保持50%以上的增速,至2019年实现销售收入3150万元左右。另考虑公司CTC产品销量的提升,公司在2017年年底有望扭亏为盈。  风险因素 (1)新产品注册审批风险;(2)核心技术失密风险;(3)市场竞争加剧的风险;(4)持续亏损风险;(5)实际控制人不当控制风险。 估值比较 估值横向比较。芝友医疗专注于肿瘤和其他重大疾病的个体化医学诊疗领域,未来有望通过提供一体化精准医疗服务,实现业绩快速增长。我们选取达安基因、科华生物、迪安诊断和新开源作为估值参考,以2017年2月23日收盘价为参考,可比公司平均市值125.9亿元,2015/TTM的PS为13X/11X;2015/TTM的PE为107X/93X。2015年芝友医疗收入和净利润为940.27万元和-990.93万元(扣非后净利润-1068.79万元)。  附注 历史沿革:成立6年的个体化医疗服务提供商 2011年7月28日,武汉友芝友生物制药有限公司成立,注册资本500万。经过三次增资,三次股转,2016年1月25日,公司完成股改,公司名称由“武汉友芝友生物制药有限公司”变更为“武汉友芝友医疗科技股份有限公司”。2016年7月13日,公司在新三板挂牌,采用协议转让方式转让股票。2016年12月22日,公司定向增发股票,发行数量为362.32万股,发行价格为17.94元/股,募集资金6500.00万元,募资后估值为6.5亿元,由北京北陆药业股份有限公司全部认购。  股权结构:袁谦为实际控制人 截至2016年12月22日,袁谦直接持有公司45.71%的股权,间接持有0.80%的股权,合计持有46.51%股权,同时担任公司董事长,因此,袁谦是公司的实际控制人,对公司的经营和决策做出判断。  来源:中信新三板
|  /3
/3 