登陆有奖并可浏览互动!
您需要 登录 才可以下载或查看,没有账号?立即注册


×
血液中大部分成分是白细胞和红细胞,CTC所占的比例相对较少。每10mL血液中,含有1亿个白细胞和500亿个左右红细胞,而CTC的数目可能仅有几个到几十个。想要准确地检测CTC细胞数目依赖非常灵敏的检测手段。近年来随着现代医学研究技术的进步和CTC临床应用价值凸显,许多研究机构和研发团队都在推出不同的CTC检测技术。CTC检测技术包括CTC的富集(分离)和CTC的分析鉴定(识别)等。
(一)CTC富集(分离)
1 免疫亲和法
建立在免疫亲和原理上的CTC富集方法,利用特异性抗体与细胞表面抗原进行特异性结合来富集CTC。基于免疫亲和的方法也分为很多种:
1.1免疫磁珠法:以CellSearch®法为代表,在磁珠上包被细胞表面粘附分子EpCAM,来捕获CTC。临床研究证明该方法检测出的CTC数目与肿瘤的预后密切相关。FDA已批准CellSearch®检测的CTC数目用于预测转移性乳腺癌,前列腺癌,结直肠癌的预后。
1.2微流体法:Nagrath和Toner的团队研发了一种用于捕获CTC的微流体。上面有78,000个微柱与EpCAM的抗体相结合,可直接捕获全血中的CTC。整个微流体共有970 mm2的表面积,在2mL/hour的通量下,CTC捕获效率>60%,特异性在50%左右。在多种转移肿瘤中该方法已被证明有较高的CTC捕获效率。
1.3纳米结构基体:Wang et al等人将EpCAM抗体结合在硅质的纳米基体上,进行CTC捕获。1mL/hour的通量下,可以达到95%以上的捕获效率。一项研究利用该方法对26例前列腺癌进行检测,CTC的检出率为20/26,明显高于CellSearch®系统。
1.4微量离心管:由Hughes et al研制,在微量离心管上包被EpCAM及PSMA的抗体,4.8mL/hour的通量下,捕获率可达50%,特异性达66%。用该方法对14例转移性肿瘤患者进行CTC检测,检出率为100%,明显高于CellSearch®系统。
1.5 体内富集:将结合EpCAM的装置从前臂静脉插入病人体内,并停留30min,从而进行体内CTC富集。临床实验证明这种方法对乳腺癌和肺癌的CTC细胞均有较高的捕获效率。
1.6 白细胞去除法:属于阴性富集法。用特异性抗体CD45,CD14等与白细胞结合,从而去除全血中的白细胞。该方法比其它富集方法捕获效率更高,但特异性低于其它方法。
利用抗原抗体相互作用原理的CTC富集方法可得到较高的纯度。但捕获效率对细胞表面抗原的表达情况依赖较明显。对于依赖EpCAM的捕获方法,CTC捕获效率与细胞表皮抗原的表达情况密切相关,一些CTC可能由于EMT过程中表皮抗原发生变化而未被捕获。另外EpCAM法仅限于对上皮来源的CTC进行检测。相对于其它方法,免疫亲和法对CTC的富集效率偏低。
2 物理特性富集法 依据CTC的物理特性,如密度、大小、可变形性及表面电荷等进行富集。
2.1密度梯度离心:非常廉价高效的CTC分离方法,可将CTC与白细胞和红细胞分离。目前市场上有较多的依赖密度梯度离心进行CTC富集的试剂盒,如Ficoll-Paque®solution (PharmaciaFine Chemicals, Uppsala, Sweden) , OncoQuick®(Grenier BioOne, Frickenhausen, Germany)等。临床实验证明,密度梯度离心富集CTC比CellSearch®系统效率更高。
2.2微孔过滤:依据CTC体积大于血细胞的特性,对CTC进行捕获。该技术已在转移性肝癌,肺癌,前列腺癌,黑色素瘤等肿瘤中被证明有效。捕获效率高于CellSearch®系统。
2.3微流控芯片:最初由Tan和 Lim团队研发,针对CTC的体积和可变形性,CTC的捕获率和特异性均可达到80%以上。在Tan和 Lim研究的基础上,研究者们又发展了不少改进型的微流控芯片。
2.4介电电流:由于CTC与血细胞所携带的电荷不同,在双向电泳的条件下,可将CTC有效捕获(95%)。目前该技术主要对细胞株进行研究,临床标本的研究相对较少。
物理特性富集法操作简单,成本低廉,不依赖细胞表面抗元的表达,捕获效率较高,但相比其它方法,所富集的CTC纯度较低。
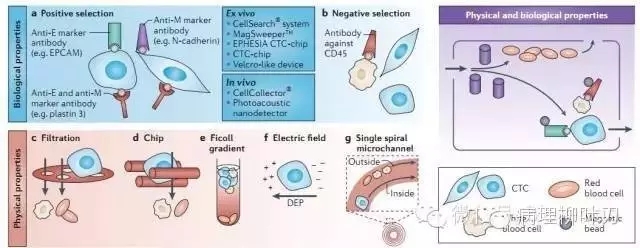
CTC分离、富集及检测
下面为目前文献已发表CTC分离机富集技术总结:
(二)CTC分析鉴定 利用免疫亲和或物理特性法可富集到CTC,这只是研究CTC的第一步,还需要结合有效的下游分析方法。一方面由于目前CTC捕获技术不能保证百分之百的纯度,需要对所得到的细胞进行鉴定,以进一步确定CTC细胞的数目,以减少CTC数目判定的假阳性率和假阴性率。另一方面在肿瘤的发生发展过程中,不仅CTC的数目在动态的变化,CTC所携带的分子标志物也在变化,通过对CTC表面标志物检测,能够反应肿瘤发生发展的动态变化,是研究肿瘤发生发展机制的有效策略,并能很好地指导临床治疗。常用的CTC分析鉴定技术如免疫荧光、PCR、FISH及高通量测序等。
1 免疫荧光法(IF) IF可用于检测CTC表面分子标志物的表达情况。CellSearch®系统应用了免疫荧光对CTC进行鉴定。EpCAM +、CK +、DAPI+、CD45 -的细胞被判定为CTC,而EpCAM+、CK +、DAPI+、CD45 +的细胞不被判定为CTC。在科研方面有非常多的免疫荧光法结合CTC的研究案例。Baccelli等在各自的研究中对富集的CTC进行干细胞相关标志物CD44,CD24,CD133,ALDH1等的检测。Armstrong等在各自的研究中对富集的CTC进行表皮间质细胞相关标志物,TWIST, AKT2,PIK3α,N-cadherin and vimentin等进行检测。Ignatiadis等用IF检测了乳腺癌CTC中HER2的表达。Shaffer 等分别检测了前列腺癌中EGFR和AR基因的表达。
2 荧光原位杂交(FISH) FISH技术亦可以与CTC非常好的结合,不仅可以检测CTC表面标志物,亦可以检测CTC细胞内部的标志物及核型等。I-FISH CTC检测系统利用白细胞去除法富集CTC后,用FISH法对细胞的核型进行判断,将异倍体阳性,表面EpCAM阳性,和DAPI阳性的细胞定义为CTC。AttardG等对89例乳腺癌患者进行研究,在治疗过程中每个月提取一次CTC,并用FISH技术检测TMPRSS2-ERG融合基因,AR和PTEN拷贝数变化,该研究发现CTC表面标志物与组织活检有高度的一致性,并最终分析出在前列腺癌治疗过程中,上述基因的动态变化。另一个典型的例子是Pailler E等7发表在J Clin Oncol上的一项研究。研究对象是18例组织检测ALK融合基因阳性和14例组织检测ALK融合基因阴性的肺癌患者。结果表明组织检测ALK融合基因阳性患者体内可检测到ALK融合基因阳性的CTC,这些ALK融合基因阳性的CTC在融合位点方面有很强的异质性,各种类型的CTC所占比例在crizotinib治疗过程中动态变化。
3 基于PCR的检测方法 CTC富集结合RT-PCR可同时对若干个基因的表达进行检测。Sieuwerts等对50例转移性乳腺癌患者进行研究,术前采集CTC,其中CTC数目的大于5的患者为32例。接下来用RT-PCR法检测55个mRNA和10个miRNA,依据这些基因的表达情况,将转移性乳腺癌患者分成四类,每类患者的恶性程度和预后是不同的。这种分类方法比依赖HER2和ER进行分类能更好地指导临床。ChangK等对75例前列腺癌患者进行研究,统计外周血中CTC的数目,并检测CTC所含的干细胞相关基因(ABCG2,PROM1,PSCA)和EMT相关基因(TWIST1和vimentin)的表达情况,经统计分析发现,CTC中干细胞相关基因的表达情况可作为前列腺癌的预后指标。位点特异性PCR技术可用于检测CTC携带的驱动基因的突变情况。例如,MaheswaranS等对接受酪氨酸激酶抑制剂(TKI)治疗的非小细胞肺癌患者进行CTC检测,在统计CTC的数目的同时,对CTC携带的EGFR激活突变进行检测,统计结果表明,携带T790M突变CTC的患者表现出明显的TKI耐药,且无进展生存期明显低于不携带T790M突变CTC的患者(7.7months vs 16.5months, p<0.001)。
4 高通量单细胞测序 随着新一代测序技术的发展,对单个CTC细胞进行测序具有了可行性。CTC单细胞测序首先依赖于单细胞扩增技术。比较有代表性的是哈佛大学谢晓亮团队研发的多重退火和成环循环扩增技术(MALBAC)。该技术能从一个细胞的基因组中,分离出来自单细胞的DNA,然后添加称作引物的短DNA分子。这些引物可与DNA的随意部分互补,从而使得它们能够附着到DNA链上,充当DNA复制起点。MALBAC可以有效地降低PCR扩增偏倚,使得单细胞中93%的基因组能够被测序。这种方法使得检测单细胞中较小的DNA序列变异变得更容易,因此能够发现个别细胞之间的遗传差异。这样的差异可以帮助解释癌症恶化的机制,生殖细胞形成机制,甚至是个别神经元的差异机制。另一种常用的单细胞扩增技术被称作多重置换扩增(MDA)。该方法随机设计引物,让这些引物与基因组广泛结合,同时使用特定的聚合酶,这种聚合酶能够转换与它自身附着在同一模板上的DNA链片段,形成一种反复分支结构,扩增出大段DNA。单细胞扩增技术保证了足够量的DNA进行高通量的检测。目前不少课题组都发表了CTC单细胞高通量测序的相关文章,证明了CTC单细胞测序方法的可行性和有效性。例如HeitzerE等对来自6例结直肠癌的37个CTC进行单细胞测序,Ni X等对来自11例肺癌病人的24个CTC进行全基因组测序。 本文部分内容转载自公众号宝藤生物 来源:病理柳叶刀
|  /3
/3 