金桔
金币
威望
贡献
回帖0
精华
在线时间 小时
|
2024年,8月28日

这个是北京中关水木医疗,三方公司,他们的视频号培训挺多,在招人
国产器械注册 进口器械注册
岗位职责:
1.国内外医疗器械的产品注册、备案申报工作,保证注册流程顺利进行并及时获取注册证;
2.按照相关国内外法律法规的要求起草产品申报资料,解决注册/备案申报过程中遇到的困难和问题;
3.与相关政府部门或机构联系和沟通,跟踪项目审评审批情况;
4.与检验机构联系并保持良好关系,跟进检测进度;
5.与国内外客户RA或技术人员交流,获得良好的技术支持;
6.归档并维护产品注册资料;
7.完成领导安排的其他任务。
任职资格:
1.生物医学工程、临床医学、理工科专业,本科及以上学历;
2.有1-3年同岗位工作经验优先,可接受应届毕业生;
3.英文阅读能力强,能够阅读英文专业文献,口语基本能沟通;
4.有良好的职业道德和职业素养,沟通能力和协调能力以及学习能力,有团队合作精神,较强的抗压能力。
#医疗器械注册 #我的北漂生活 #NMPA认证
注册专员日常分享,看你是否从中找到学习的方法,欢迎咨询,我也可以教学
2024年
昨天下班和网友吃饭了。网友是做医疗器械可用性的。


他推荐了小吾金榜这个餐厅,选了个靠窗位置,我们点了招牌脆皮鸡,很好吃。散会后,又回到小区陪朋友吃了个汉堡 ,朋友竟然用咸鱼下单买汉堡,便宜一半,我学会了。朋友让我请我们吃麦旋风,应为我写的专利受理了,发了1000奖金。
最近主要工作是负责产品变更注册。专标和电气安全70工作日。电磁兼容50个工作日,如果是大的设备60工作日。环境实验看具体要测哪些项目,进箱费四五千,其他按项目算。
一类医疗器械备案,从23年提前联系我,到现在厂家委托合同签订好,这家公司是委托生产。所以还协助他们改合同,发现一个客户很粗心的问题,委托方和受托方的章盖反了。非常感谢客户的信任,
23年的时候我才刚工作2年。没有过多的质疑,当时我也比较忙,让我上海的朋友帮他们做,这位领导还挺信任我,前期有和他们讨论分类编码的事情,就说让我做就放心。于是我就同意了。
一类备案准备的资料不多。主要的是负责细心。
1.产品说明书,标签,产品照片
2.技术要求
3.检测报告
4.营业执照,委托生产合同或质量协议
5.授权人文件
6.生产制造信息。#有需要注册或者备案的老板吗?
#医疗器械注册 #我的北漂生活 #医疗器械注册专员
端午去哪里逛逛呢?抖音刷到汪雨橦来北京上班了。
#医疗器械注册工程师 #医疗器械注册 #我的北漂生活 #NMPA认证 #端午节
2023年11月30
这周第一件事情是公司13485审核,开了不合格项,在审核中风险提了很多问题,风险的识别,分析不正确,有遗漏,应该从,设计,过程,应用,三方面分析。附录的第一个产品的预期用途,第一条之前写的否,一上来就被质问,为什么否,然后补充了信息危害和操作危害。
产品英文说明书,没人审核,一直放着,制度不规范。
帮领导修改三类有源设备的送检资料,说明书依据专标补充检测提出的,同时写了me设备可接触部分的最高温度(外壳,按钮,电源线),依据GB9706.1 中的超温的要求,什么材料,多长时间。
完善一类备案的说明书,技术要求,自检报告,注册申请表,生产信息文件等。
调研立项新产品冲洗器,已取证的厂家,查看他们的产品,和专利,了解产品的分类。
和将离职的同事对接项目培训,要讲什么,不了解产品,所以让他自由发挥,培训法规,产品标准,原理,性能等。

非常充实的一周,周五放松的一天,领导去天检所出差,上午没到公司就开始催时间节点文件,调研一天竞品,看他们的专利,发现有个公司很新的产品,但是没有申请专利,或者还没公开,很迷惑。
不想做无意义的工作,但是开展新业务的时候,反而会心理压力,很矛盾。#你觉得注册工作累不累
2024年1月31日
最近在学习新产品,发现
符合的标准和法规如下:
EN 60601-1/A1:2014
AAMI ES 60601-1 3rd Edition + A1:2012
CAN/CSA-C22.2 No.60601-1:2014
According to 60601 this device is Type BF, Class 1, IP22 rating.According to MDD93/42/EEC, Annex IX, Rule 11, this device is classified as aClass Ila device. For all other accessories refer to the accompanying DFUs for moreinformation.
DualWave 关节镜泵是一种集成的流入和流出流体管理系统,也可用作简单的仅流入泵。
DualWave 泵是一种安全、可靠、用户友好的系统,可在关节镜手术的所有阶段保持对关节内冲洗和膨胀压力的恒定、非脉冲控制。它旨在提供连续的无脉冲流动,可立即对关节内压力的变化做出反应,因此即使在拔出量高或二次流出的情况下,关节扩张也可以持续。用户定义的流入压力和流出速率设置可通过触摸屏面板或遥控器上的控件进行调节。
#医疗器械注册 #欧盟医疗器械注册 #我的北漂生活 #关节内窥镜 #医用冲洗器
24年2月2日更新
Welcome to CDRH Learn! [赞R]CDRH Learn is our multi-media educational resource, featuring learning modules that address medical device and radiation emitting product laws, regulations, guidances, and policies, across the entire product life cycle.
[向右R]These modules provide industry with information that is comprehensive, interactive, and easily accessible.
Modules are provided in various formats, including videos, audio recordings, and slide presentations.


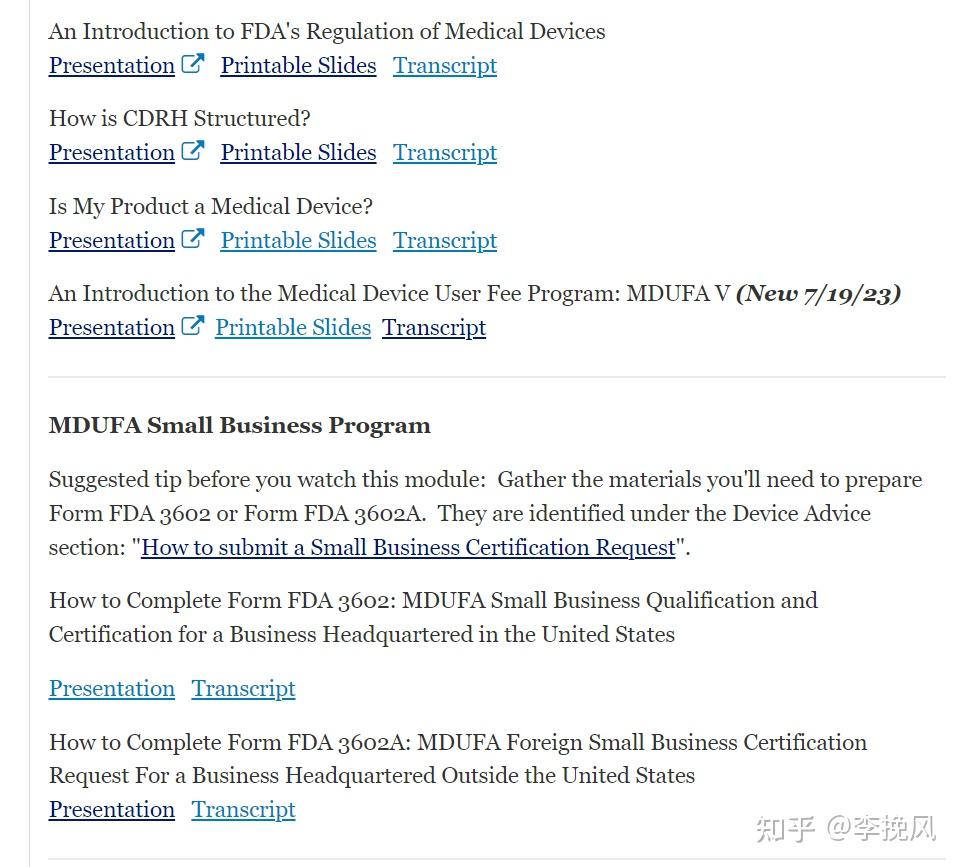

培训讲解视频,ppt,pdf.指南文件,从基础开始,CDRH结构,医疗器械的定义与分类,美国 本国的产品注册与列名,美国 国外的产品列名,510k上市前通知,上市前批准,里面的还有对应文件法规的二维码,甚至还有手把手教你申请美国在小企业免费用申请步骤演讲视频。
CDRH Learn的presentation感觉做的比国内好多了,演讲很正式。国内的演讲都没有ppt下载链接,而且是以前那种大会议的录屏,有时候画质和音质也不清晰。
#医疗器械注册 #我的北漂生活 #fda认证 #医疗器械国际注册 #医疗器械 #美国医疗器械注册 #你想学哪个国家的注册呢? |
|
 /3
/3 