在液相系统分析过程中,有没有遇到过色谱峰前延现象?为什么有时候同一个样品减小进样量色谱峰就变的很好看?日常的分析工作中,分析员通常将更多精力集中在流动相和仪器方法的选择上,忽视了样品进样溶剂的重要性。如果溶剂选择不当则会产生“溶剂效应”,使分析工作者在定性和定量分析中产生误判,影响分析结果。因此,了解“溶剂效应”产生的原因及掌握避免“溶剂效应”的基本方法对分析工作者是十分必要的。今天就跟大家分享一下,液相分析过程中“溶剂效应”的哪些事。溶剂效应亦称“溶剂化作用”。指液相反应中,溶剂的物理和化学性质影响反应平衡和反应速度的效应。可能造成色谱峰展宽、分叉、保留时间漂移、峰面积变化,双峰等现象。与此同时,较早洗脱的峰出现前沿或分叉,较晚洗脱的峰峰形正常。- 分裂峰在正常色谱峰的前面,而且出峰时间越早的化合物分裂越明显,出峰时间越晚的化合物甚至不会受影响。
- 色谱柱损坏(如筛板堵塞)导至的峰裂分,分叉峰出现在正常峰的右边,而且这种影响会波及所有化合物,前后峰型不正常。
- 减少样品进样体积(如0.5μL),若峰形恢复正常就可以断定为“溶剂效应”。
当然并不是所有的前沿分裂峰都是因溶剂效应引起的,也有可能是色谱柱过载其一,流动相溶解目标物,多见于一种或极性相近的几种目标物测定;其二,非流动相溶解目标物,比如天然提取物中未知物探索、极性差别较大的多种目标物分析、某些液体物质直接进样(比如酒类成分分析、水中污染物分析)等。流动相或初始比例流动相溶解样品可以看作样品处理的理想状态,只要未发生体积过载(注:进样体积超过柱体积的1%时,即存在体积过载风险)或浓度过载,一般可以得到完美的结果。当样品溶剂与流动相的洗脱强度差别较大时,液相色谱的表现则会遭遇一些麻烦。由于进样时样品分子是由样品溶剂夹带着到达色谱柱的,并非所有样品分子同时达到,有一个先后次序,因此后达到色谱柱的样品溶剂在局部范围内就变成了先到达样品分子的流动相,样品溶剂对色谱分离的影响主要就来源于上述第二个作用上,即在进样瞬间起到流动相的作用,这个作用时间虽然很短,但此时样品浓度大,样品溶剂在短暂时间内对样品在色谱柱中的浓度分布产生较大影响,造成色谱峰前延,展宽,甚至分叉。第一阶段:样品刚被注入系统,进入色谱柱后,流动相氛围中的目标物以正常速度被洗脱。因强溶剂洗脱,移动速度快。样品在空间上开始慢慢分裂。
第二阶段:在一定时间内,溶剂氛围中的目标物移动始终快一些,前后两部分距离扩大。但移动快的目标物所处氛围逐渐被流动相稀释(注:因为溶剂和流动相均不保留),其移动速度会逐渐降至正常流速。直到前面目标物的氛围完全被流动相替代,前后两部分的距离稳定下来。因而,样品溶剂与流动相洗脱强度差距越大,两部分目标物最终的距离拉的越大。 第三阶段:所有目标物在色谱柱中正常移动,但分裂已不可逆转。经过检测器,同一目标物给出了两个色谱峰。其中进柱前即扩散进入流动相的那部分目标物组成了后面的色谱峰,它的保留时间与目标物的真实保留时间基本吻合。简单概括,强洗脱溶剂不均衡地参与了目标物的洗脱,使色谱峰保留时间整体提前,而样品在柱前的不充分扩散导至了峰形扭曲。这种影响轻则导至峰展宽,严重时甚至导至峰裂分,给定性定量带来灾难。
溶剂效应若想造成巨大灾难的一个前提条件是:样品溶剂的洗脱强度应明显强于流动相,否则,即使抵达柱头时目标物溶解在两种溶剂中,但由于洗脱强度接近,它们在随后的洗脱过程也不会拉开距离,也就不会裂分,甚至不会展宽。 样品抵达柱头的过程中,均存在样品向周围流动相扩散的过程,出于抑制柱外展宽的目的,分析者希望抑制这种扩散。如果目标物溶解在流动相或与流动相强度相近的溶剂中,抑制柱外扩散能提高柱效利于分离。二者洗脱强度差别大时,如不能让目标物完全扩散至流动相,溶剂效应很可能发生。 溶剂强度,在反相色谱系统中溶剂强度的顺序为水(最弱)<甲醇<乙腈<乙醇<四氢呋喃<丙醇<二氯甲烷(最强)。溶解样品的溶剂强度大于该样品出峰时流动相强度,样品溶剂可以看成流动相的一部分,一部分样品溶解于溶剂中会被迅速洗脱出色谱柱,而一部分样品溶解于流动相,被流动相洗脱出,这样会造成色谱峰的展宽或者分叉。进样体积,进样体积造成的溶剂效应是一般与溶剂种类有关的。流动相作为溶剂时,增加进样体积后,目标分析物色谱峰不会发生迁移,保留时间基本稳定。使用强度大于该样品出峰时流动相强度的溶剂,增加进样体积后,目标分析物色谱峰会向前迁移,直至裂分,并且峰高变小峰宽变大。这是因为进样体积较小时,扩散至流动相的目标分析物占绝大多数,除了保留时间略微提前,峰形以及峰宽与流动相溶解时基本一致。体积增大到一定程度,扩散至流动相氛围的目标物与留在溶剂氛围的目标物在数量上相当时,色谱峰分叉明显。当样品体积进一步增大,绝大多数目标物进入色谱柱时是溶解在溶剂中的,目标分析物的色谱峰已经明显向前迁移了。溶剂与流动相的兼容性,有些样品采用流动相或者流动相中的有机相溶解难度较大,分析工作者会采用氯仿、乙酸乙酯、苯等溶剂,这些溶剂与流动相兼容性不佳,直接包裹溶质跳过色谱初期的保留过程,待溶剂的分配平衡建立起来后溶质过于展宽,甚至直接部分冲出色谱柱。其实在色谱柱中的流动相只有50%是动态,其余50%在死体积、载体间隙处于静止状态。溶质被固定相吸附先通过50%的“静止区”,若溶剂及流动相不兼容,则影响溶质在溶剂与流动相之间的传递,从而影响被固定相吸附而导至峰形变差。 溶剂pH值,易于解离的化合物对流动相的pH值较敏感。该化合物处理解离状态下极性发生显著变化,导至固液分配系数发生较大变化。该影响经常表现为保留时间的漂移而不是多个峰或者峰分叉等峰形差现象。 柱前管路,柱前管路内径越大、管路越长,越利于目标物向流动相扩散,而且使用更粗的管路比更长的管路有效(注:假设死体积相同)。虽然粗的管路加剧了等度条件下的柱外展宽,对柱效有危害,然而相较于峰分叉的危害而言,前者尚能接受。 这就是为什么有时候会发现,HPLC的液相(管路死体积大)比UPLC的液相(管路死体积小)色谱峰型好
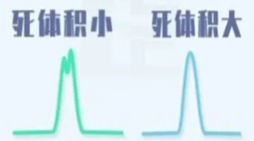
其实,这不是仪器不好,恰恰是这个系统对管路控制的太好了,才会让溶剂效应导至的峰形变形更明显!
其他影响因素,还有很多再此就不做详细叙述
应该尽量使用流动相作为溶剂(梯度采用初始比例),以及用弱洗脱强度的溶剂稀释样品,比如反相色谱法下,向有机溶剂中加水,可以极大减弱或消除溶剂对色谱行为的影响。溶剂中的有机相比例略低于流动相有机相比例时峰形更好。 当样品浓度响应较大,可以采用减少进样体积减弱溶剂的影响。但要酌情而定,比如在有关物质测定时,减少进样量常常会牺牲灵敏度。 当溶剂因标准或者待测成分性质不能改变时,可适当提高流动相比例,使其强度尽量与溶剂接近,从而消除影响。然而这种方法可能会危害化合物的分离。 吸样后,针不回针座,悬停空中,计量泵吸-排-吸-排数次,使目标物完全扩散至流动相。 对于梯度洗脱而言,在不影响分离度的情况下,可以改用较粗内径的柱前管路。(注意:假如是等度洗脱,此方法会降低柱效;假如是梯度洗脱,基本不影响柱效)。
小知识:
在梯度洗脱模式下,溶剂效应不明显,如果真的存在,也只是影响出峰较早的色谱峰。这是因为梯度洗脱下,初始比例流动相无法洗脱目标物,而且强洗脱溶剂也无法让其快速移动,它们会富集在柱头,等流动相洗脱强度提高到一定程度,化合物才会逐渐被洗脱。对于某些保留弱的化合物,它的洗脱强度与初始比例流动相越接近,就越容易受溶剂效应影响。因而,为了照顾出峰较早的目标物,即使使用了梯度洗脱,也不要采用强洗脱溶剂来溶解(假如低洗脱强度溶剂能完全溶解所有目标物)。
(1)强洗脱溶剂造成的溶剂效应主要是保留时间提前,峰裂分时,裂分峰在左。低洗脱强度溶剂造成的溶剂效应主要是保留时间延后,但延后幅度较小,即使发生裂分,前后两峰均能保持良好峰形。
(2)改用流动相溶解样品或减小进样体积可以消除溶剂效应;低强度溶剂稀释样品或梯度洗脱也是抑制溶剂效应的好办法;柱前改用粗内径管路或进样前进行预混合可以将目标物扩散至流动相中,能够挽救峰形,如果是梯度洗脱,这甚至不影响柱效。但假如是等度洗脱,这会增大目标物的柱前展宽,危害柱效,所以这两个办法是最后的选择。
参考文献 Lee H K , Hoffman N E . INJECTION SOLVENT EFFECT ON PEAK HEIGHT INION-EXCHANGE HPLC[J]. Journal of Chromatographic Science, 1992,30(10):415-421.
Hoffman N E , Chang J H Y . Injection Solvent Enhancement of Peak Heightin Reversed-Phase Liquid Chromatography[J]. Journalof Liquid Chromatography,1991, 14(4):651-658.
谢孟峡, 杨力力.酚类化合物的反相高效液相色谱研究(I)[J].北京师范大学学报:自然科学版,1991(2):211-216.
Castells C B , Castells R C . Peak distortion inreversed-phase liquidchromatography as a consequence of viscosity differences between sample solventand mobile phase[J]. Journal of Chromatography A, 1998,805(1–2):55-61.
|  /3
/3 