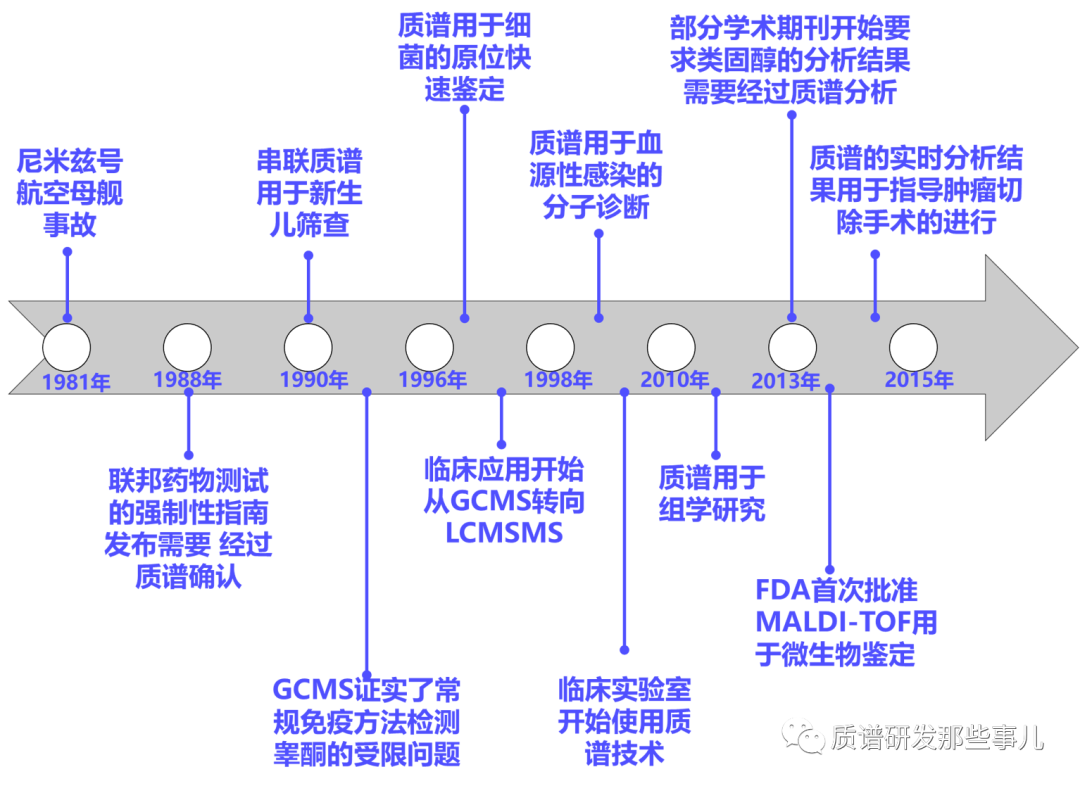
1981年5月26日,美国一架训练归航的EA-6B“徘徊者”电子战飞机在“尼米兹”号核动力航母进行着舰时一头冲向右侧停机区的3架F-14“雄猫”战斗机,随后引发一枚巨大的“不死鸟”导弹爆炸。瞬间,“尼米兹”号的甲板上就发生了大爆炸,火光冲天,飞行员、地勤人员瞬间死亡。最讽刺的是由于美军装备过于先进,在最初的撞击中,有几枚没有当场爆炸,因此现场产生了二次爆炸。事故中共造成14人死亡,45人受伤,11架战斗机严重受损,“尼米兹”号航母也暂时失去了战斗力,不得不回港接受大修。 此次事故造成了极其严重的损失。事后调查指出肇事EA-6B的飞行员违反规定服用抗组织胺药物,以致于降落作业中摇晃不稳,此外由于辅降系统没有完整运作,加上天候气象因素,使得航空管制人员在EA-6B第二次降落时,未能及时察觉偏离航道。而当时夜间辅降系统的大部分灯光都是熄灭的,以致于指引功能大受影响。当时的损管系统也不能发挥完整作用,舰上18个消防泵中只有12个正常工作。更重要的是,事后基于免疫分析对舰上人员进行了尿液检测,发现6名航管人员的大麻代谢物检测结果呈阳性。自此里根总统开始了对军队中滥用药物的零容忍态度。同时,“尼米兹”号航母事故也开启了质谱进入临床应用的大门。大多数药物滥用都是非法的,但由于症状和迹象并不明确,所以在临床标准界限之外的药物滥用很难判断。传统上是用免疫方法进行药物监测,这类方法快速、简便,但可能很昂贵(试剂花费),通常测定的是化合物组,不能测定具体分析物。同时由于缺乏特异性,免疫方法有可能会出现大量的假阳性结果。通常阳性结果必须要用气相色谱质谱GCMS进行确证。1988年,FDA发布了《联邦工作场所药物测试计划的强制性指南》,规定了药物测试结果一定要经过质谱确认。由于质谱的使用,在随后的10年里药物测试结果的阳性率从 18% 下降到 8%。使用GCMS进行确认的强制要求推动了质谱在毒理学实验室的发展,并开始了质谱用于治疗药物的监测。随着GCMS在临床实验室越来越常见,免疫法在类固醇测定中的局限性变得越来越明显,尤其是在测定妇女和儿童低浓度睾酮时明显受限。目前,质谱分析方法已经被确定为激素测定的金标准,它解决了既往方法的低阈值低低灵敏度问题,也可以为睾酮提供试剂盒以及为激素水平的测定提供标准参照。目前,世界上已有3个实验室获得批准进行建立LCMS的标准RMP(Reference Measurement Procedure)测定方法测定睾酮。其中2个在欧洲,使用同位素稀释气象色谱串联质谱法(ID-GC-MSMS),另一个在美国NIST(National Institute of Standards and Technology)实验室,使用基于同位素稀释液相色谱串联质谱法(ID-LC-MSMS)为常规测定方法提供试剂盒、测量参考标准和高水平校准。GC-MS 的主要限制是分析物需要具有挥发性,因此大多数临床分析需要多个提取/纯化步骤以及化学衍生化,以使分析物具有足够的挥发性以进行分析。由于低通量和高成本,GC-MS 分析所需的大量样品制备方案限制了质谱在临床实验室中进一步的广泛应用。不过,大气压电离技术,尤其是电喷雾电离 (Electrospray Ionization, ESI),与高性能的LC-MS/MS的完美结合,让质谱成为常规临床实验室的基础平台已经逐渐变成了现实。ESI LC-MS/MS 消除了对挥发性分析物的要求,因此简化了样品制备流程,继而提高了样品分析通量,并降低了成本。GC-MS 分析的限速步骤是样品制备时间,而 LC-MS/MS 中的限速步骤通常是LC的分析时间。因此,为了进一步提高质谱分析的通量,降低成本,可以将多个LC(2~4个)连接到同一个MS上。这种情况下,最适合用于单一分析物的分析,不同LC的进样是交错的,而MS始终测量同一色谱目标峰。多路复用之所以有效的基本原理是,单次LC的运行时间通常会持续几分钟或更久,然而目标峰通常只在几秒钟的时间内洗脱完毕。如果没有多路复用,大部分时间里MS都在“等待”目标峰的到来和洗脱。通过交错进样,使用4个LC的多路复用系统就可以将MS的生产率提高几倍。2002年,MALDI-TOF质谱技术获得了诺贝尔化学奖,以表彰该技术在解决生物大分子分析难题上的突破性进展。2013年,美国FDA(食品和药物管理局)首次批准了基于MALDI-TOF质谱的微生物快速鉴定产品,从而开启了质谱技术进入临床检验的新时代。今天,MALDI-TOF质谱可以用于微生物的快速鉴定已经不是新鲜事了。在此之前,微生物实验室里通常是依赖革兰氏染色、培养、生化测试和敏感性测试来完成微生物的鉴定。与传统技术相比, MALDI-TOF质谱方法将鉴定的平均时间缩短了 1.45 天。据估计,与标准培养技术相比,实施 MALDI-TOF 将节省 50% 以上的试剂和劳动力成本。梅里埃BioMerieux和 布鲁克Bruker Daltonics 的MALDI-TOF产品是最早一批获得FDA批准用于临床微生物分析的产品。随着微生物鉴定技术的不断发展,人们也逐渐意识到MALDI-TOF或许并不是十全十美的技术,其他技术,诸如16S rRNA基因测序技术、以及其他质谱与PCR的结合技术,也都在一些细分领域里取得了一定的技术优势地位。但这些并不妨碍MALDI-TOF质谱技术在临床应用的地位,同时MALDI-TOF还开拓出了诸如质谱成像(Mass Spectrometry Imaging)等新的临床应用。在病理学研究和实践中,基于MALDI-TOF 的质谱成像技术已被用于识别组织中的蛋白质、肽、药物或代谢物、脂质和其他分析物。具体而言,质谱成像允许对组织切片中的各种分子进行无标记、多重测量,同时质谱成像分析过后的样本仍可用于常规的组织学染色分析。这种组合方法既可以得到组织内各空间位点的质谱信息(物质组成),又可以得到单个分子或者单组分子在组织内的空间分布。使用质谱对临床样本进行代谢组学、脂质组学和蛋白质组学以及其他组学分析是近些年最令人兴奋的研究领域,未来会对临床实验室具有广泛的影响。这些技术的目标是首先使用非靶向方法从几百到上千种生物分子中找到几种生物标记物,然后用靶向方法针对性地获得这些生物标记物的信息。因此,非靶向方法通常用于生物标记物发现阶段,依靠比较来自 两个不同人群(例如,健康和患病)的组学样本。一旦确定了区分这两个群体的生物分子(生物标记物),就可以使用有针对性的方法(靶向方法)来进一步表征和监测这些生物标志物变化在健康和疾病状态中的意义。先天性代谢缺陷 (Inborn Errors Metabolomics, IEM) 源于人体内的酶、辅因子或转运蛋白的缺陷或异常,这些缺陷或异常通常与生化通路中的某些特定代谢步骤有关,比如它们可能控制着DNA的复制、蛋白质的合成,亦或是保持细胞完整性所需要的特定化合物。而先天性代谢缺陷则可能造成特定代谢产物的不断积累,或者是缺乏正常代谢过程所需要的反应物,亦或是两者兼而有之,由来带来的后果就是破坏了正常的新陈代谢途径。先天性代谢缺陷IEM 是儿童发病和死亡的一个重要原因,尽管每一种代谢缺陷疾病都很罕见,但它们在儿童遗传病中占据了非常大的比例。目前,已知的新生儿出生缺陷超过了8000种,同时每年新发现的遗传病超过50种。1961年,美国Guthrie建立了细菌抑制法进行血液中苯丙氨酸的半定量测定,并建立了干血斑采集技术,易于储存和运输,适用于大规模人群的筛查,从此新生儿苯丙酮尿症PKU筛查得以实施。然而,单一筛选试验仅能用于检测单一疾病。1990年Millington首次提出使用三重四极杆串联质谱进行干血斑检测,一个样本可以同时筛选一组分析物,检测多种代谢疾病。时至今日,美国、日本、韩国等发达国家使用三重四极杆串联质谱进行新生儿代谢疾病筛查的比率已经接近100%,同样在中国用于新生儿筛查的质谱技术也正处于加速发展的阶段。 通过以上,我们能够发现质谱技术之所以逐渐在检验医学中发挥出越来越重要的作用,是受到很多驱动因素的影响。比如,相比免疫方法,质谱方法有更好的特异性和灵敏度,并且能够覆盖非常宽的待测物浓度范围。另外,追求更低的检测成本同样是推动质谱在临床实践中发展的一个重要动力。尽管质谱的一次性成本投入会更高,然而质谱方法有能力针对同一样本同时进行多种目标物的检测,因此极大节省了检测时间、人力以及检测费用。与此同时,质谱技术在临床应用中的发展同样面临着很多挑战,包括对使用者操作技能的要求相对更高,相对而言缺乏自动化设备,以及某些新兴领域里政策法规的不确定性等。然而,既有巨大的临床市场的诱惑,又有质谱技术自身发展的不断驱动,临床质谱的发展必将是会极大推动整个临床医学的进步。现有临床质谱技术在不断打磨和巩固现有应用领域的同时,一些新的市场也在不断被发掘和拓展,比如质谱原位检测技术用于指导肿瘤切除手术过程、小型化质谱在POCT领域里的应用、质谱流式技术在高通量的单细胞分析中的应用、呼出气质谱在疾病早筛中的应用,等等等。。。 临床市场同样是质谱技术可以大展拳脚的星辰大海,而我们并不仅仅是旁观者。同样,我们也不应该仅仅满足于追随者的坐享其成,更应该有勇气和智慧去成为引领者和创造者。与诸君共勉![1] https://www.sohu.com/a/190618090_99983438 [2] https://www.federalregister.gov/documents/2017/01/23/2017-00979/mandatory-guidelines-for-federal-workplace-drug-testing-programs [3] https://www.agilent.com/cs/library/applications/5989-1541CHCN%20low.pdf [4] Peat MA. Financial viability of screening for drugs of abuse. Clin Chem 1995;41:805– 8. [5] Clinical Chemistry, 62:1, 92–98 (2016) [6] https://www.antpedia.com/news/28/n-2323428.html [7] http://www.bioyong.com/cloum/detail/84.html [8] Gregory S. Makowski. Advances in Clinical Chemistry. 2017. Volume 79. 1-252 [9] Maier, T., Klepel, S., Renner, U. et al. Fast and reliable MALDI-TOF MS–based microorganism identification. Nat Methods 3, i–ii (2006). [10] InternationalJournal of Mass Spectrometry, Volume 377, 2015, Pages 672-680
| 
 /3
/3 