金桔
金币
威望
贡献
回帖0
精华
在线时间 小时
|
先看下手机端百度搜索“药品注册招聘”,直接查看来自智联招聘的信息,查看相关待遇还是很靠谱的,见下图:
第一张图,坐标上海,其他条件均不设限
再看第二张图,坐标还是上海,条件限制公司性质为欧美外资
我们可以看到,药品注册的待遇范围差别太大了,为什么会这样?
无非就是工作年限、工作经验、能力水平、当然还有英语水平,下面一一道来,看看药品注册究竟是一个什么样的工作,是否有前途?需要掌握哪些知识和技能水平?具体主要负责什么工作?工作环境如何?
<hr/>Perspective 前景
Because the quantity and quality of the drug registrar&#39;s work are closely related to the working life, experience and social relationship, and the treatment level is directly linked to the work performance, so salaries vary widely. 由于药品注册专员工作完成的数量与质量和从业者的工作年限、就业经验、社会关系等紧密相关,而待遇水平与工作效绩直接挂钩,故薪酬浮动范围相对较大。
前途肯定是有的,而且含金量越来越高
The persons who handle the application for drug registration shall have professional knowledge and be familiar with the laws and regulations on, and the technical requirements for, drug registration. 《药品注册管理办法》(2007年)第二章第十条 办理药品注册申请事务的人员应当具有相应的专业知识,熟悉药品注册的法律、法规及技术要求。
《药品注册管理办法》(2017年修订稿)第二章第三十二条 申请人应当确定药品注册专员负责办理药物研制及药品上市许可申请相关事务,并给予其充分授权。
2017年新出的《北京市药品注册专员登记办法》对这个职业给出的官方定义是:熟悉药品注册的管理法律法规和各种规定要求,熟练掌握药品注册申报程序的、从事药品注册申报工作的专业人员,即药品注册专员。
对药品注册感兴趣,想了解注册法规技术最新资讯,又想把英语水平练上来,微信关注“药事谷”,有很多对大家有用的资源,大家也可以积极加入这个团队,共同进步。
<hr/>药品注册有哪些等级呢?
Level 等级
Entry level 入门级,刚毕业的,或工作刚一年半载的。这个时候主要就是积累经验,熟悉流程,纯小白,要学习的东西会很多。待遇一般
Mid or senior level 中级或高级,工作至少3年以上,还要有很强的学习能力。可以当主管、经理了,待遇可观。
Professionals 专业级,到这个级别,得很有几把刷子,不仅仅是工作经验了,还有各种人脉关系的积累。这个时候你已经可以当上副总级别了,根据公司不同,年薪三五十万,上百万的也不稀罕。
<hr/>那么你要问了,药品注册具体做什么的?What RA do?做什么
Monitor regulation 监测法规
Drug registration specialist shall have the corresponding professional knowledge, be familiar with the laws, regulations and technical requirements for registration of pharmaceuticals, understand the specific information of application products; have the ability to organize, implement and review the authenticity, integrity and normative of the application materials. 药品注册专员应当具有相应的专业知识,熟悉药品注册的法律、法规及技术要求,掌握申报品种的具体信息;有能力组织实施申报资料真实性、完整性和规范性审查。
- Drug Administration Law 《药品管理法》
- Drug Registration Regulation 《药品注册管理办法》
- Regulations on the Implementation of Drug Administration Law 《药品管理办法实施条例》
Registration of pharmaceutical product 药品注册
Drug registration refers to the process of review and approval on which the State Food and Drug Administration, in accordance with the official procedures, evaluates the safety, efficacy and quality of the drugs applied for marketing, and decides whether or not to approve such an application.
药品注册,是指国家食品药品监督管理局根据药品注册申请人的申请,依照法定程序,对拟上市销售药品的安全性、有效性、质量可控性等进行审查,并决定是否同意其申请的审批过程。
Do pharmaceutical, API, and excipients products require registration?
制剂、API及辅料都需要注册吗?
All drugs, APIs, and excipients manufactured outside China must be. 所有的制剂、原料药、辅料都需要注册。药品注册管理办法修订稿可以看出未来将实行关联审评审批。
Regulatory classifications for pharmaceuticals 药品注册分类
根据最新的化药注册分类要求和药品注册管理办法修订稿整理如下:
In China, drugs are classified as 3 types:
Chemical Drugs – 5 classes 化药有5类
Biological Drugs – 5 classes 生物制品会参考化药分类也是5类,等正式稿下来应该。
Traditional Chinese Medicine/Natural Drugs – 5 classes 中药也是会参考化药分类也是5类,等正式稿下来应该。
Registration pathway 申报路径
The different types of drug applications(化学药品为例)
New drug application 新药注册申请
Generic drug application 仿制药注册申请
Imported drug application (includes foreign new drugs) 进口药品注册申请
Supplemental application 补充申请
License renewal 再注册
Documentation 资料撰写 天天跟你打交道最多的,除了你的老板,就是申报资料了,这个得慢慢看,慢慢啃,搞清楚,搞明白,搞透彻!
药品注册申报资料的体例与整理规范;化学药品研究资料及图谱真实性问题判定标准;化学药药学资料CTD格式电子文档标准(试行);化学药物综述资料撰写的格式和内容的技术指导原则;化学药物临床试验报告的结构与内容技术指导原则;抗病毒药物病毒学研究申报资料要求的指导原则;……;Product technical requirements产品技术要求 ......
<hr/>那么药品注册人员想冲击经理、总监、公司副总级别需要掌握哪些技能和储备哪些知识呢?药物开发流程这可是最基础的知识了!
RA should have total knowledge 法规人员要有全面的知识
Drug development 药物开发
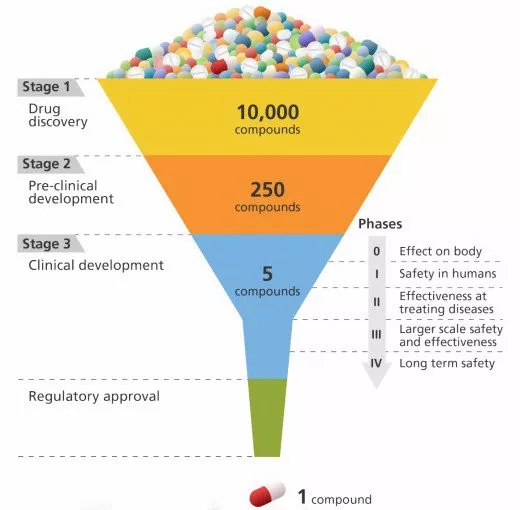
首先,药物从开发到上市的流程得熟熟的吧。
Step1 Discovery and Development
Research for a new drug begins in the laboratory.
研究一个新药从实验室开始。
Step 2 Preclinical Research
Drugs undergo laboratory and animal testing to answer basic questions about safety.
药物在实验室和动物上进行安全性试验。
Step 3 Clinical Research
Drugs are tested on people to make sure they are safe and effective.
在人体上测试以确定药物安全有效。
Step 4 CFDA Review
CFDA review teams thoroughly examine all of the submitted data related to the drug or device and make a decision to approve or not to approve it. 国家食品药品监督管理局审评团队对提交的关于药物或医疗器械的数据进行严格的检查,以决定是否批准。
Step 5 Post-Market
Post-Market Safety Monitoring已上市产品的安全性监测
<hr/>其次吧,GMP的基本原则和概念可不能少!一点GMP的意识都没有不要说在制药行业混过。
GMP principles 药品生产质量管理规范(GMP)原则
The 10 Golden Rules of GMP
Rule#1 Get the facility design right from the start 厂房设计合理
Rule#2 Validate processes 验证过程
Rule#3 Write good procedures and follow them 编写良好的程序并遵循
Rule#4 Identify who does what 确定谁做什么
Rule#5 Keep good records 保持良好的记录
Rule#6 Train and develop staff 培养和发展员工
Rule#7 Practice good hygiene 良好的卫生实践
Rule#8 Maintain facilities and equipment 厂房设施设备维护
Rule#9 Build quality into the whole product lifecycle 建立产品全生命周期的质量体系
Rule#10 Perform regular audits 执行定期审计
<hr/>Skills requirements 技能要求
Exceptionally organized 非凡的组织能力
Strong subject knowledge 扎实的专业知识
Good communication skills 良好的沟通技能
Computer skills 电脑技能
<hr/>Work environment 工作环境
A great deal of paper work 大量的文字工作
Manage deadline 管理期限
Fast paced work atmosphere 快节奏工作环境
Exposure in regulatory working暴露于监管工作
Work closely with Export/marketing department
与出口/市场部门紧密合作
Liaise with production, QA, QC, purchase and product management
沟通联络产品生产, QA, QC, 采购和产品管理部门
<hr/>就回答这么多,如果说想了解更多相关知识,获得最新的政策动态,欢迎加入我们。推荐一下我的公众号:药事谷。大家瞅瞅绝对有不一样的地方。
 |
|
 /3
/3 