近日,国家卫健委临检中心发布了全国新型冠状病毒核酸快速检测第二次室间质量评价结果报告,本次质评中,共计收到 1221 家实验室回报的有效结果(即使用合适的试剂检测并回报结果完整、在截止日期内回报的结果)。EQA/PT 成绩合格的实验室 1209 家(99.0%),不合格实验室 12 家(1.0%)。 据临检中心要求: (1)新型冠状病毒核酸快速检测是指:核酸提取、扩增检测均在同一封闭、便携式仪器上完成;样本上机后至结果报告过程,无需任何手工操作,且全流程时间不超过 90 分钟。截至目前,国家药品监督管理局(National Medical Products Administration, NMPA)批准的新型冠状病毒核酸快速检测试剂如表 1。 请实验室选择正确的仪器和试剂进行新型冠状病毒核酸快速检测。 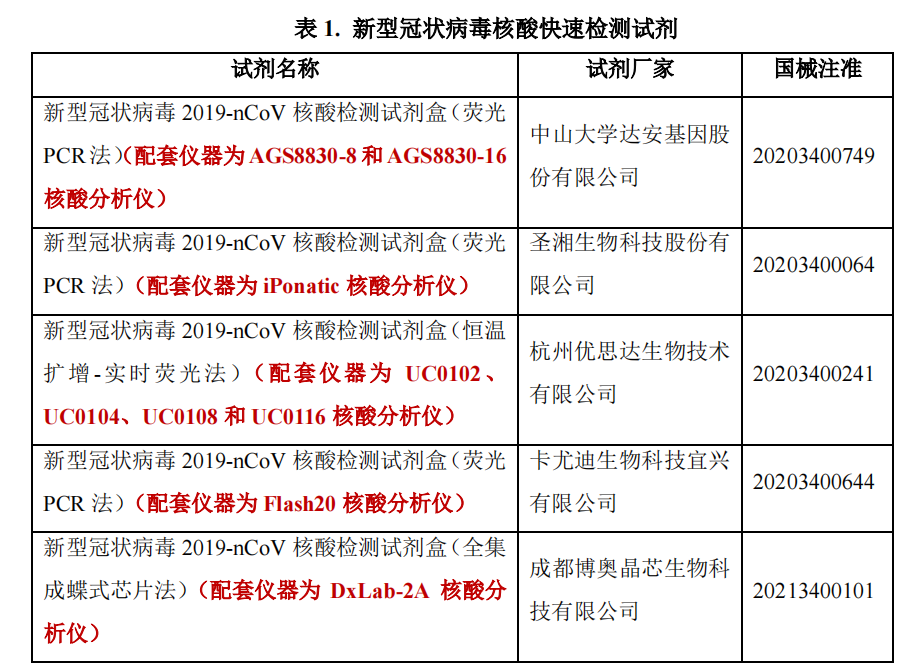
(2)样本信息 本次共发放 5 个质评样本,编号分别为 202121、202122、202123、202124、202125。本次质评样本为基因工程方法制备的噬菌体病毒样颗粒模拟样本,无生物传染危险性。 
(3)结果统计 
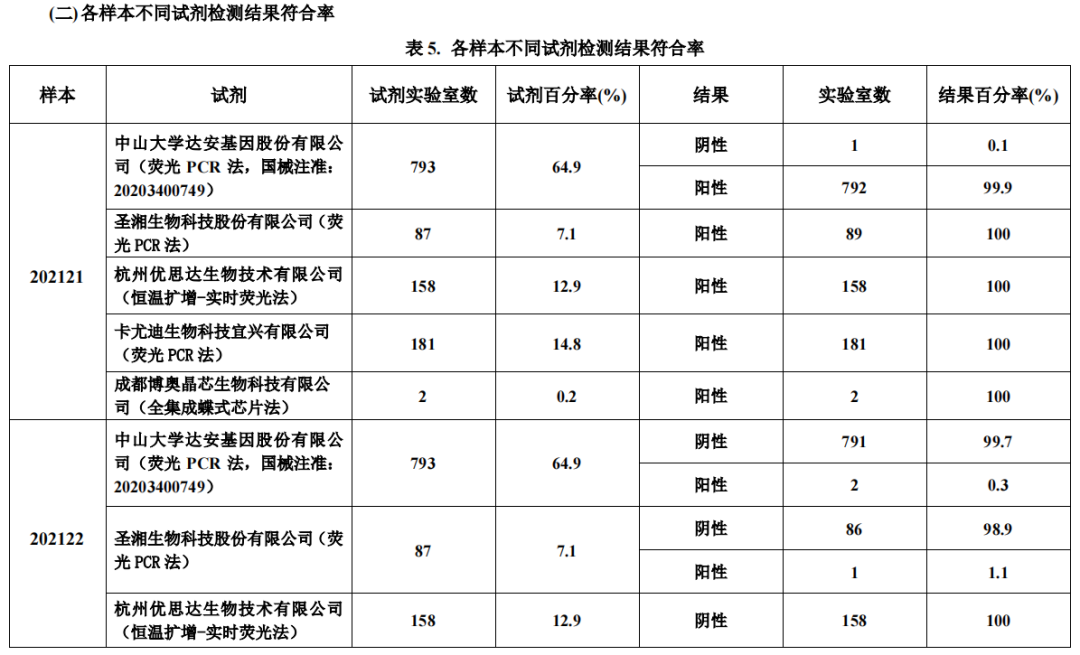


(4)结果分析
本次室间质评主要针对新型冠状病毒核酸快速检测展开,涉及达安基因、卡尤迪、优思达和博奥晶芯四家IVD公司产品,全国参与实验室共计1221家,其中使用达安基因试剂作为考核试剂的实验室为793家,占比达到64.9%!卡尤迪生物排在第二位,参与实验室为181家,占此次考核实验室的14.8%!优思达排在第三位,参比实验室158家,占比为12.9%!圣湘生物仅排第四,参比实验室为87家,占比为7.1%。
本次质评的202123、202124号样本为本次质控品中的低浓度样本,在各家试剂表现较为不好的两个标本;本次质控活动中优思达和博奥晶芯的新冠核酸快检产品在5个样本中均以100%的符合率通过!其中博奥晶芯的参与实验仅有2家,仅供参考。
来源 | 国家卫健委临检中心发布了全国新型冠状病毒核酸快速检测第二次室间质量评价结果报告 |  /3
/3 