CRISPR/Cas9、Cas12、Cas13已被开发成多种分子诊断策略用于各种病原体,包括细菌和病毒的核酸检测,尤其是利用Cas12、Cas13的附属切割活性开发出的SHERLOCK系列、HOLMES系列和DETECTR等检测平台,为感染性疾病的快速诊断提供了新的契机。
1.基于CRISPR/(d)Cas9 的感染性疾病核酸检测平台:CRISPR/Cas9由于具有精确的靶标序列识别和切割的能力,因此具有开发成分子诊断工具的潜力。Pardee等[7]在2016年结合Cas9和NASBA(核酸依赖性扩增检测技术),借toehold生物传感器开发出一种恒温可视化的检测平台,用于肉眼检测寨卡病毒,并利用其识别单核苷酸多态性的能力用于美洲寨卡和非洲寨卡的基因分型。Huang等[8]开发了一种CAS-EXPAR平台,将Cas9切割后的产物作为引物,利用指数扩增反应(exponential amplification reaction, EXPAR)进行扩增,之后对产物进行荧光显色(图1A)。该平台能够在1 h内检测李斯特菌,并且具有阿摩尔级别(10-18/L)的灵敏度和单碱基分辨的特异度。
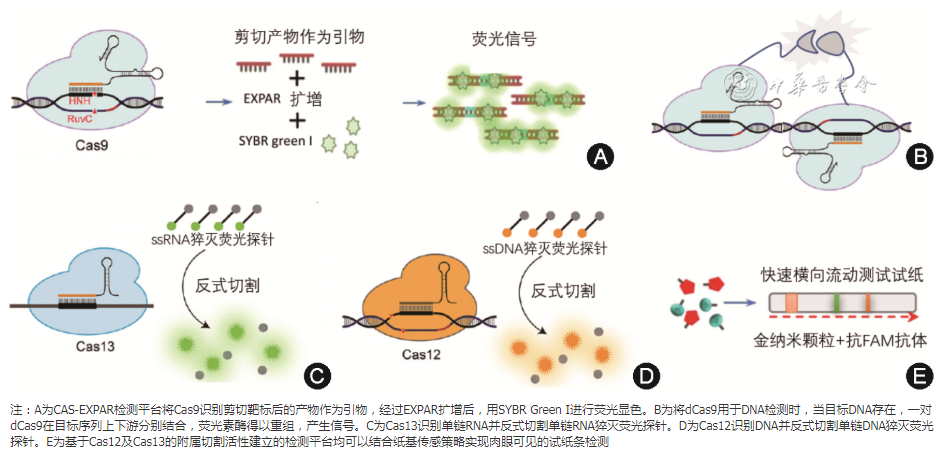
图1 CRISPR/Cas系统用于检测原理示意图
此外,没有切割活性的cas9(dCas9)仍然有识别结合靶序列的能力,这一特点也可以被巧妙利用于生物传感,例如将两个dCas9分别连接上分离荧光素酶的N端和C端,这两个dCas9的sgRNA被设计为识别结核分枝杆菌DNA上下游的序列片段。如果目标DNA存在,一对dCas9在目标序列上下游分别结合,荧光素酶得以重组,发出荧光信号用于检测(图1B)[9]。Guk等[10]在2017年报道了一种利用dCas9对靶标的高度亲和性检测耐甲氧西林金黄色葡萄球菌mecA基因的方法,给dCas9蛋白连接磁球,当dCas9捕捉结合靶标后,磁性分离出dCas9并用SYBR-GreenⅠ显色其结合的双链DNA,这种将CRISPR/Cas9与DNA荧光原位杂交联用的方法简单快速,并展现出相当好的灵敏度。
2.基于CRISPR/Cas13的感染性疾病核酸检测平台:Ⅵ型CRISPR系统包含一个名为Cas13a的“效应器”蛋白,其识别靶标类型是单链RNA而非DNA(图1C)。张锋团队利用其附属切割的特点建立起的第一个检测平台称为SHERLOCK[6]。在这个平台中,首先对靶标进行重组酶聚合酶扩增(recombinase polymerase amplification, RPA)或逆转录重组酶聚合酶扩增(reverse transcription-recombinase polymerase amplification, RT-RPA),然后再进行T7转录,靶标被扩增的同时也使得检测的靶标类型不局限于RNA。他们利用SHERLOCK成功对大肠埃希菌、铜绿假单胞菌、结核分枝杆菌、肺炎克雷伯菌和金黄色葡萄球菌进行了鉴定,并且区分出了肺炎克雷伯菌不同的耐药基因。基于SHERLOCK的检测方式检测耗时在2 h内,并且单次检测的成本低廉,为核酸检测开启了新篇章。在此基础上,张锋课题组还开发出了SHERLOCKv2[11],即SHERLOCK的二代版本,将Cas13a与Csm6(一种辅助的CRISPR Ⅲ型核酸酶)联用,两者协同作用使得信号得以增强,使检测灵敏度较一代提高了3.5倍。通过用稀释的等温扩增引物进行非饱和反应,从一代的定性检测变为相对定量检测。通过应用带有抗FAM抗体和金纳米粒子的纸基传感器,开发出了便携式试纸条。此外,通过将筛选出的在附属切割上有序列偏好的3种Cas13蛋白和1种Cas12a蛋白在一个体系中应用,实现了一个体系同时检测4种病原体。这4点性能的提升和突破使得SHERLOCK在感染性疾病检测上变得更加灵敏、实用、便携和高效,例如在医疗条件相对落后地区,不论是DNA、RNA还是细菌感染导至的肺炎都可以用这种方式进行检测,还可以进行人类免疫缺陷病毒滴度监测以指导抗病毒治疗等。从这些优势中足以预见这种新型分子诊断平台在感染性疾病诊断上有着极佳的前景。之后,张锋团队又将一种通过加热和化学还原的方式裂解病毒颗粒和灭活核糖核酸酶的样本预处理方法(HUDSON)添加到SHERLOCK样本处理步骤中,使得SHERLOCK可以直接用于从临床样本中检测病毒核酸,而省去提取和纯化的样本预处理步骤[12]。这进一步缩短了样本周转时间,简化了步骤,这对于将CRISPR/Cas用于病原体的实时快速检验有非常重要的意义。
3.基于CRISPR/Cas12的感染性疾病核酸检测平台:Ⅱ类V-A型Cas12蛋白也被发现具有反式切割活性,但与Cas13不同,Cas12靶向DNA并附属切割单链DNA(图1D)。利用Cas12首先开发出的平台包括HOLMES和DETECTR。Li等[5]用HOLMES检测DNA/RNA病毒,可在1 h内从细胞系或临床样本中检测病毒基因型和人类单核苷酸多态性(single nucleotide polymorphism, SNP),并且灵敏度也可达到阿摩尔级。之后的HOLMESv2利用Cas12b具有很宽的反式切割活性温度范围特点,将其与环介导的等温扩增方式相结合,实现了一个集靶标扩增和信号转化的“一锅式”核酸检测系统,支持定量检测靶DNA[13]。这是迄今为止用于RNA检测的最简单的CRISPR生物传感平台。Chen等[14]利用DETECTR快速准确地鉴定了各种亚型的HPV病毒。与SHERLOCK类似的是,HOLMES或是DETECTR都可以通过剪切荧光报告探针实现荧光信号检测或结合纸基传感策略实现肉眼可见的试纸条检测(图1E)。
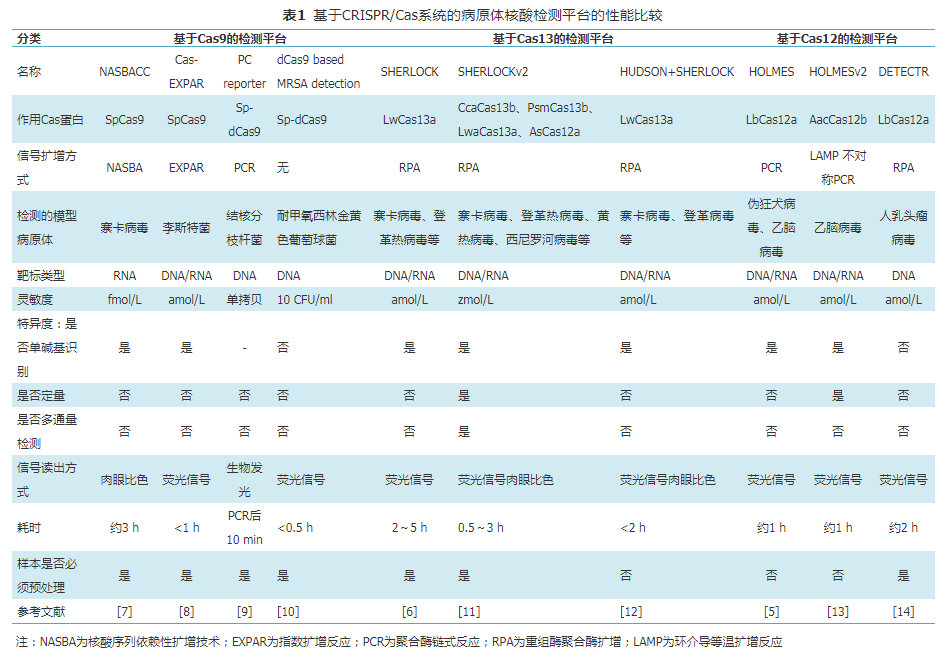
2019年,James课题组提出了一种对传统材料进行分子编程后用于生物传感的策略。他们将Cas12a-gRNA复合物嵌入连有单链DNA的晶格结构中制成水凝胶[15]。当水凝胶系统暴露于靶标DNA存在的环境中时,Cas12a被激活,其对周围单链DNA的反式切割使得水凝胶的骨架被剪切破坏,从而造成水凝胶的塌陷。在生物传感方面,用此策略检测了葡萄球菌的mecA基因片段,激活的Cas12剪切将淬灭荧光基团连接于凝胶骨架的单链DNA,导至荧光信号产生。他们还将水凝胶嵌入微流控纸质设备中,开发了一种可以对埃博拉病毒进行实施快速检测的试纸条,这种试纸条在实战中表现出相当好的灵敏度和可重复性。新颖的组合方式使得老材料用了新用法,这种创新的思路可以催生更多新颖的生物传感策略[16]。表1比较了上述具有代表性的基于CRISPR/Cas系统的病原体检测分子诊断平台的性能。
 /3
/3 