新型冠状病毒感染的肺炎疫情发生后,卫健委、药监局等相关部门密集出台有关法规政策。据统计,国家卫健委已出台各类通知通告44条,新型冠状病毒感染的肺炎诊疗方案已更新至第五版,各地药监局迅速启动医疗器械应急审批程序,加快相关产品供应,及时应对疫情。
国家药品监督管理局
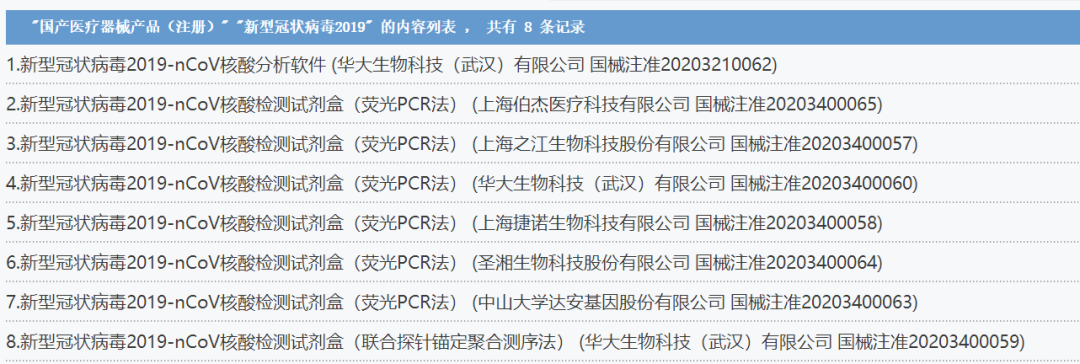
新型冠状病毒感染的肺炎疫情发生后,国家药监局立即启动医疗器械应急审批程序,按照“统一指挥、早期介入、随到随审、科学审批”的原则和确保产品安全、有效、质量可控的要求,全力加快审评审批速度。目前,已应急批准新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法)和2019新型冠状病毒核酸测序系统等8个产品。同时已要求省级药监部门加强对上述产品生产企业的监督检查,确保产品质量安全。
国家药监局将继续对疫情防控所需的药品医疗器械采取特殊审批程序,争取相关产品尽快上市。
为积极应对新型冠状病毒感染的肺炎疫情,各地药监局也迅速启动应急审批程序。对于应急审批的医疗器械,在简化申请资料,缩短审批时间等方面都给予了绿色通道。
● 山西省药品监督管理局关于对防控疫情用医疗器械实行应急审批的通告(2020年1月27日)
● 安徽省药品监督管理局关于启动疫情防控药械应急审评审批工作的公告(2020年1月27日)
● 云南省药品监督管理局关于紧急进口未在中国注册医疗器械的公告(2020年1月31日)
● 重庆市药品监督管理局关于紧急进口未在中国注册医疗器械的公告(2020年2月1日)
●甘肃省药品监督管理局关于对新型冠状病毒感染的肺炎疫情防控药械实施应急审批管理的公告(2020年2月1日)
● 广东省药品监督管理局关于印发广东省防控新型冠状病毒感染的肺炎疫情所需药品医疗器械行政许可应急审批程序的通知(2020年2月1日)
● 上海市药品监督管理局关于对防控疫情用医疗器械实行应急审批的通告(2020年2月2日)
●黑龙江省药品监督管理局关于对疫情防控急需药品和医疗器械应急审评审批相关工作的通知(2020年2月2日)
此外,浙江、江苏、山东、湖南、河南、吉林等地药监局也启动了医疗器械应急审评审批程序,在标准不降低、程序不减少的情况下,完成审评审批工作。
国家卫生健康委员会
●新型冠状病毒感染的肺炎诊疗方案 ●
声明:
1、凡本网注明“来源:小桔灯网”的所有作品,均为本网合法拥有版权或有权使用的作品,转载需联系授权。2、凡本网注明“来源:XXX(非小桔灯网)”的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。其版权归原作者所有,如有侵权请联系删除。
3、所有再转载者需自行获得原作者授权并注明来源。




 /3
/3 





 浙公网安备33010802005999号
浙公网安备33010802005999号


